名校
1 . 物质的量是联系宏观和微观的桥梁,请回答下列问题:
(1)将NaOH、 的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示,回答下列问题:
的体积(标准状况)关系如图所示,回答下列问题:
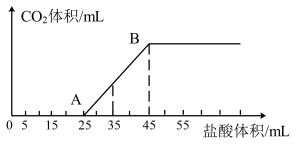
①AB段发生反应的离子方程式为_______ 。
②当加入35mL盐酸时,产生 的体积(标准状况)为
的体积(标准状况)为_______ mL。
③原混合溶液中NaOH与 的物质的量之比为
的物质的量之比为_______ 。
(2)用质量分数为98%的浓硫酸(密度为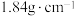 )配制成
)配制成 的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:
的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:
①经计算,浓硫酸的浓度为_______  。
。
②本实验必须用到的仪器有量筒、烧杯、玻璃棒、_______ 、_______ 。
③若出现以下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
Ⅰ.没有用蒸馏水洗涤烧杯和玻璃棒_______ 。
Ⅱ.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线_______ 。
(1)将NaOH、
 的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入
的固体混合物完全溶解于水,配制成溶液,然后向该溶液中逐滴加入 的盐酸,所加盐酸的体积与产生
的盐酸,所加盐酸的体积与产生 的体积(标准状况)关系如图所示,回答下列问题:
的体积(标准状况)关系如图所示,回答下列问题:
①AB段发生反应的离子方程式为
②当加入35mL盐酸时,产生
 的体积(标准状况)为
的体积(标准状况)为③原混合溶液中NaOH与
 的物质的量之比为
的物质的量之比为(2)用质量分数为98%的浓硫酸(密度为
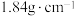 )配制成
)配制成 的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:
的稀硫酸。现实验室仅需要这种硫酸220mL,试回答下列问题:①经计算,浓硫酸的浓度为
 。
。②本实验必须用到的仪器有量筒、烧杯、玻璃棒、
③若出现以下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
Ⅰ.没有用蒸馏水洗涤烧杯和玻璃棒
Ⅱ.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
名校
解题方法
2 . 纯碱和小苏打在工业、生活中有着广泛的应用。现有 和
和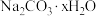 的混合物,为了测定x的值,某同学采用如图所示的装置进行实验(无水
的混合物,为了测定x的值,某同学采用如图所示的装置进行实验(无水 、碱石灰均足量)。
、碱石灰均足量)。
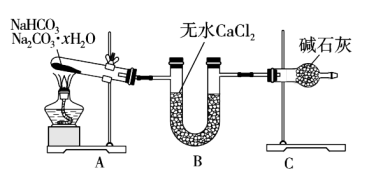
已知:碱石灰是氢氧化钠和氧化钙的固体混合物。请回答下列问题:
(1)C装置中装有碱石灰的仪器名称是___________ 。
(2)加热A装置,混合物分别发生反应的化学方程式为___________ 、___________ 。
(3)无水氯化钙的作用是___________ 。
(4)若在装置A的试管中装入 和
和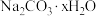 的混合物
的混合物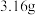 ,用酒精灯加热至反应完全,此时B装置增重
,用酒精灯加热至反应完全,此时B装置增重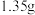 ,C装置增重
,C装置增重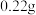 ,则ⅹ的值为
,则ⅹ的值为___________ 。
(5)该装置还不是很完善,可能使测定结果偏小,应如何改进?___________ 。
 和
和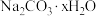 的混合物,为了测定x的值,某同学采用如图所示的装置进行实验(无水
的混合物,为了测定x的值,某同学采用如图所示的装置进行实验(无水 、碱石灰均足量)。
、碱石灰均足量)。
已知:碱石灰是氢氧化钠和氧化钙的固体混合物。请回答下列问题:
(1)C装置中装有碱石灰的仪器名称是
(2)加热A装置,混合物分别发生反应的化学方程式为
(3)无水氯化钙的作用是
(4)若在装置A的试管中装入
 和
和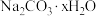 的混合物
的混合物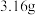 ,用酒精灯加热至反应完全,此时B装置增重
,用酒精灯加热至反应完全,此时B装置增重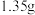 ,C装置增重
,C装置增重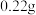 ,则ⅹ的值为
,则ⅹ的值为(5)该装置还不是很完善,可能使测定结果偏小,应如何改进?
您最近一年使用:0次
2021-12-31更新
|
264次组卷
|
2卷引用:黑龙江省齐齐哈尔市2021-2022学年高一上学期期末考试化学试题
名校
解题方法
3 . 纯碱是重要的生活用碱和化工原料,用途广泛。请同学们按要求回答问题。
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。
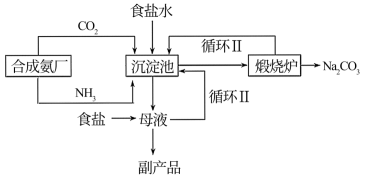
(1)请写出煅烧炉中发生反应的化学方程式:___________ 。
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为___________ ,循环Ⅰ中物质的主要成分是___________ 。(本小题涉及到的物质均写化学式)
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。
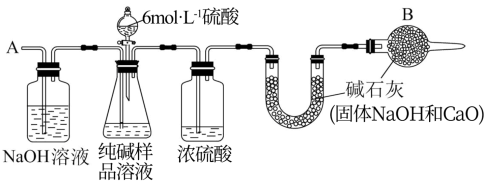
主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是___________ 。
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将___________ (填“偏高”、“偏低”或“不变”)。
(5)步骤⑤的目的是___________ 。
(6)步骤⑦的目的是___________ 。
(7)该样品中纯碱的质量分数的计算式为___________ 。
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是___________ 。
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
Ⅰ.纯碱生产:我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下。

(1)请写出煅烧炉中发生反应的化学方程式:
(2)侯氏制碱的创新之处:根据NH4Cl在常温时的溶解度比NaCl大,而在低温下却比NaCl溶解度小的原理,在5℃~10℃时,向母液中加入食盐细粉,而使NH4Cl单独结晶析出供做氮肥,大大提高了原料利用率、降低了生产成本,为世界制碱业做出了巨大贡献。依据上述信息可知,副产品的成分为
Ⅱ.产品纯度的测定:上述生产中获得的纯碱产品中含有少量NaCl杂质,为测定该样品中纯碱的质量分数,可用如图所示的装置进行实验。

主要实验步骤如下:
①按如图所示装置来组装仪器,并检查装置的气密性;
②将a g纯碱样品放入锥形瓶中,加入适量蒸馏水溶解,得到纯碱样品溶液;
③称量盛有碱石灰的U形管的质量为b g;
④通过分液漏斗滴入6 mol·L-1的硫酸,直到不再产生气体为止;
⑤从导管A处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的U形管的质量为c g;
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g.
请回答下列问题:
(3)装置中干燥管B的作用是
(4)从A处通入的空气如果不经过NaOH溶液,测量结果将
(5)步骤⑤的目的是
(6)步骤⑦的目的是
(7)该样品中纯碱的质量分数的计算式为
(8)如果所得产品中除含有少量NaCl杂质外还含有少量NaHCO3杂质,下列实验方案中能测定出产品中纯碱的质量分数的是
A.取a g产品充分加热,质量减少b g。
B.取a g产品与足量Ba(OH)2溶液反应,过滤、洗涤、干燥,得到b g固体。
C.取a g产品与足量BaCl2溶液反应,过滤、洗涤、干燥,得到b g固体。
您最近一年使用:0次
名校
解题方法
4 . 向100 mL NaOH溶液中通入一定量的CO2气体,经充分反应后,再向所获得的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断不正确的是
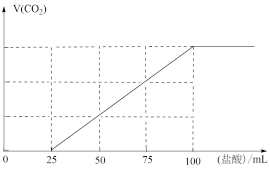

| A.原NaOH溶液的物质的量浓度为0.1 mol·L-1 |
| B.通入CO2的体积为224 mL |
C.V(盐酸)=0~25 mL的范围内发生的离子反应为:CO +H+=HCO +H+=HCO |
| D.所得溶液的溶质成分为Na2CO3和NaHCO3且物质的量之比为1∶2 |
您最近一年使用:0次
名校
5 . 下列试验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量CaCl2溶液反应,过滤、洗涤、烘干得到bg固体 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg |
您最近一年使用:0次
2021-12-04更新
|
1011次组卷
|
7卷引用:黑龙江省鹤岗市第一中学2022-2023学年高一上学期11月期中化学试题
黑龙江省鹤岗市第一中学2022-2023学年高一上学期11月期中化学试题湖南省石门县第一中学2021-2022学年高一上学期期中段考化学试题(已下线)专题36 碳酸钠质量分数测定的实验探究-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江西省宜春市铜鼓中学2021-2022学年高一下学期开学考化学试题陕西省西安中学 2023 届高三上学期第二次质量检测化学试题河南省顶级名校2023届高三上学期10月月考化学试题宁夏回族自治区银川一中2023-2024学年高一上学期期中考试化学试题
名校
6 . 纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)实验室中需0.2mol/L的 溶液980mL,配制时应选用容量瓶的规格和称取
溶液980mL,配制时应选用容量瓶的规格和称取 的质量分别是_______。
的质量分别是_______。
(2)碳酸钠和碳酸氢钠的鉴别与稳定性探究。
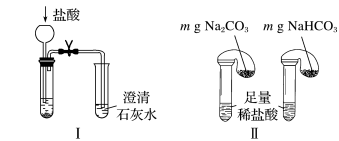
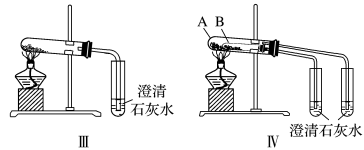
①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是_______ (填装置序号)。
②图Ⅲ、Ⅳ中_______ 能更好说明二者的稳定性(填装置序号)。Ⅳ中受热处发生反应的化学方程式:_______ 。
(3)利用图Ⅲ的装置加热 和
和 的混合物,剩余固体成分会随二者物质的量不同而发生变化。当
的混合物,剩余固体成分会随二者物质的量不同而发生变化。当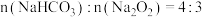 充分混合后,加热至完全反应,试管内剩余的固体是
充分混合后,加热至完全反应,试管内剩余的固体是_______ (填化学式)。
(1)实验室中需0.2mol/L的
 溶液980mL,配制时应选用容量瓶的规格和称取
溶液980mL,配制时应选用容量瓶的规格和称取 的质量分别是_______。
的质量分别是_______。| A.500mL;21.2g | B.900mL;20.1g | C.1000mL;20.1g | D.1000mL;21.2g |


①只根据图Ⅰ、Ⅱ所示实验,能够达到鉴别目的的是
②图Ⅲ、Ⅳ中
(3)利用图Ⅲ的装置加热
 和
和 的混合物,剩余固体成分会随二者物质的量不同而发生变化。当
的混合物,剩余固体成分会随二者物质的量不同而发生变化。当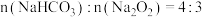 充分混合后,加热至完全反应,试管内剩余的固体是
充分混合后,加热至完全反应,试管内剩余的固体是
您最近一年使用:0次
2021-12-02更新
|
444次组卷
|
2卷引用:黑龙江省大庆实验中学2021-2022学年高一上学期期中考试化学试题
名校
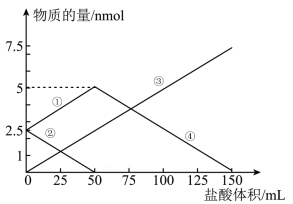
7 . 将一定物质的量的 、
、 组成的混合物溶于水配成1L溶液,取出50mL溶液,然后滴加一定物质的量浓度的盐酸与它反应,得到的图象如图所示。下列说法错误的是
组成的混合物溶于水配成1L溶液,取出50mL溶液,然后滴加一定物质的量浓度的盐酸与它反应,得到的图象如图所示。下列说法错误的是
 、
、 组成的混合物溶于水配成1L溶液,取出50mL溶液,然后滴加一定物质的量浓度的盐酸与它反应,得到的图象如图所示。下列说法错误的是
组成的混合物溶于水配成1L溶液,取出50mL溶液,然后滴加一定物质的量浓度的盐酸与它反应,得到的图象如图所示。下列说法错误的是
| A.图象中③线代表的物质是NaCl |
B.④线发生的离子反应: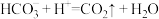 |
| C.盐酸的物质的量浓度是0.05 mol/L |
D.原混合物中 与 与 的物质的量之比为1:2 的物质的量之比为1:2 |
您最近一年使用:0次
名校
8 . 下列关于Na2CO3、NaHCO3的叙述正确的是
| A.Na2CO3溶液、NaHCO3溶液可以用澄清石灰水鉴别 |
| B.分别向Na2CO3溶液和NaHCO3溶液中滴加少量盐酸,产生CO2气体较快的为Na2CO3溶液 |
| C.充分加热agNa2CO3和NaHCO3的混合固体,根据固体质量减重bg,可以计算出混合固体中Na2CO3的质量分数 |
| D.溶解度:Na2CO3<NaHCO3 |
您最近一年使用:0次
名校
解题方法
9 . 向四只盛有一定量 溶液的烧杯中,分别通入不同量的
溶液的烧杯中,分别通入不同量的 气体,再向所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的
气体,再向所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的 气体与
气体与 的量的关系如图所示(忽略
的量的关系如图所示(忽略 的溶解和
的溶解和 的挥发,n代表物质的个数)则下列分析不正确的是
的挥发,n代表物质的个数)则下列分析不正确的是

 溶液的烧杯中,分别通入不同量的
溶液的烧杯中,分别通入不同量的 气体,再向所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的
气体,再向所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的 气体与
气体与 的量的关系如图所示(忽略
的量的关系如图所示(忽略 的溶解和
的溶解和 的挥发,n代表物质的个数)则下列分析不正确的是
的挥发,n代表物质的个数)则下列分析不正确的是
A.Ⅰ图对应溶液中溶质为 |
B.Ⅱ图对应溶液中溶质为 |
C.Ⅲ图对应溶液中溶质为 和 和 ,且 ,且 和 和 的个数比为1:2 的个数比为1:2 |
D.Ⅳ图对应溶液中溶质为 和 和 ,且 ,且 和 和 的个数比为1:1 的个数比为1:1 |
您最近一年使用:0次
2021-11-14更新
|
1094次组卷
|
3卷引用:黑龙江省大庆铁人中学2023-2024学年高一上学期10月月考化学试题
名校
10 . 侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法。具体工艺流程图如下:
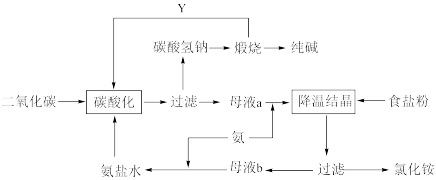
Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是___________
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)___________
(3)侯氏制碱法副产品的一种用途为___________ 。
(4)Y物质是___________ 。
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
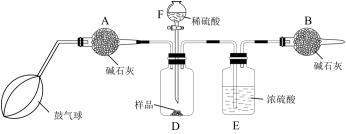
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量( )。
)。
③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质( )。
)。
⑧计算
(5)操作⑥中,鼓入空气的作用是___________ ;
(6)根据题干所给的数据列出样品中 的质量分数表达式
的质量分数表达式___________ 。
(7)经实验发现最终所得的 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是___________ 。

Ⅰ.根据以上流程回答下列问题:
(1)与索尔维制碱法相比,侯氏制碱法最突出的优点是
A.原料利用率高 B.设备少 C.生产方便
(2)碳酸化这一步的原理是(用化学方程式表示)
(3)侯氏制碱法副产品的一种用途为
(4)Y物质是
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少的NaCl,现欲测定某碳酸钠样品中
 的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
的质量分数,某探究性学习小组取样品b g设计了如下实验方案。
该实验的操作步骤如下:
①如图连接装置(除B外)并加入所需药品。
②称量并记录B的质量(
 )。
)。③按动鼓气球,持续约1分钟。
④连接上B。
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录B的质(
 )。
)。⑧计算
(5)操作⑥中,鼓入空气的作用是
(6)根据题干所给的数据列出样品中
 的质量分数表达式
的质量分数表达式(7)经实验发现最终所得的
 的质量分数超过100%,其可能的原因是
的质量分数超过100%,其可能的原因是
您最近一年使用:0次



