名校
解题方法
1 . 将1.12g铁粉加入25mL2mol∙L-1的FeCl3溶液中,充分反应后,其结果正确的是
| A.铁粉有剩余,溶液呈浅绿色,Cl-的量保持不变 |
| B.往溶液中滴入KSCN溶液,溶液不显红色 |
| C.Fe2+和Fe3+的物质的量之比为1:6 |
| D.氧化产物和还原产物的物质的量之比为1:2 |
您最近一年使用:0次
2 . 沈阳市位于辽宁省东北部,是中国重要的工业城市之一、随着城市的不断发展和人口的增加,污水处理厂的作用也愈加重要。在垃圾清理、路面施工以及工厂废水排放等方面都会产生大量的废水。某Y形河流上游两旁有甲、乙两个化工厂,其位置如图所示。经某化学课外活动小组检测,已知它们排放的工业废水中,共含 ,
, 、
、 ,
, ,
, ,
, 六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
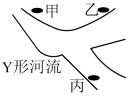
(1)经该小组检测,甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是___________ (填离子符号)。
(2)该小组认为,乙厂的废水中含有另外三种离子,如果加适量的___________ (填“活性炭”“硫酸亚铁”或“铁粉”),不但可以回收其中的一种金属,达到变废为宝的目的,还可以降低重金属离子污染,这个过程用离子方程式表示为___________ 。
(3)该小组有一个设想,建议甲厂和乙厂联合起来,把废水按适当比例混合,这样可以使废水中的___________ (填离子符号)结合转化为沉淀。再在丙地建立一个灌溉站,将过滤后的河水用来浇灌农田。他们的理由是经过滤后的废水主要含___________ (填化学式),可以促进农作物的生长,你认为他们的方案是否可行,并写出理由:___________ 。
 ,
, 、
、 ,
, ,
, ,
, 六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
六种离子。若甲、乙两厂分别含有不同的三种离子,请回答下列问题:
(1)经该小组检测,甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是
(2)该小组认为,乙厂的废水中含有另外三种离子,如果加适量的
(3)该小组有一个设想,建议甲厂和乙厂联合起来,把废水按适当比例混合,这样可以使废水中的
您最近一年使用:0次
3 . 下表所列各组物质中,物质之间按如图所示箭头方向无法通过一步反应实现转化的是
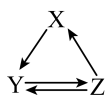

| 选项 | X | Y | Z |
| A | CaO |  |  |
| B | Fe |  |  |
| C |  |  |  |
| D | CuO |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列反应的离子方程式正确的是
A.溴与冷的NaOH溶液反应: |
B.少量 通入 通入 溶液中: 溶液中: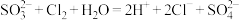 |
C.向血红色 溶液中加入过量铁粉至溶液褪色: 溶液中加入过量铁粉至溶液褪色: |
D.向含氯化铁的氯化镁溶液中加入氧化镁: |
您最近一年使用:0次
名校
5 . 向盛有5mL0.005mol/LFeCl3溶液的试管中加入5mL0.015mol/LKSCN溶液,观察现象。将上述溶液平均分装在a、b、c三支试管中,向试管b中加入少量铁粉,向试管c中滴加vmLxmol/LKSCN溶液,观察试管b、c中溶液颜色的变化,并均与试管a对比。下列说法正确的是
| A.FeCl3溶液和KSCN溶液可以产生红色沉淀 |
| B.b试管中的现象说明:当其他条件不变时,增大生成物浓度平衡向逆反应方向移动 |
| C.为了证明其他条件不变时,增大反应物的浓度平衡向正反应方向移动,则x应该尽可能的大,而v应该尽可能的小 |
| D.若向试管a中加入4滴1mol/L的KCl溶液,溶液颜色会变深 |
您最近一年使用:0次
2023-11-09更新
|
142次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高二上学期期中考试化学试题
2023高三·全国·专题练习
解题方法
6 . 以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
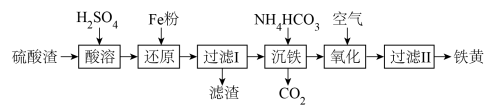
(1)“酸溶”中加快溶解的方法为_______ (任意写出一种)。
(2)“还原”过程中的离子方程式为_______ 。
(3)写出“滤渣”中主要成分的化学式:_______ 。
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为_______ 。
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中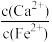 =
=_______ 。[已知Ksp(CaCO3)=2.8×10-9,Ksp(FeCO3)=2×10-11]
(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是_______ 。

(1)“酸溶”中加快溶解的方法为
(2)“还原”过程中的离子方程式为
(3)写出“滤渣”中主要成分的化学式:
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中
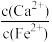 =
=(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是
您最近一年使用:0次
解题方法
7 . 认识物质的转化关系能更好地制备物质。某化学学习小组研究发现在合适条件下有多种元素及其化合物的转化符合如图所示的转化关系,下列说法错误的是


| A.若化合物甲具有特殊香味,X为氧气,则甲与丙反应可生成有香味的液体 |
| B.若甲为常见非金属单质,丙的浓溶液能与铜发生氧化还原反应,则甲一定是氮气 |
| C.若甲是常见的简单氢化物,丙与水反应后溶液显酸性,则乙可能是氧化物 |
| D.若甲为黄绿色气体,则2mol乙与足量X反应可生成3mol丙 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验过程不涉及氧化还原反应的是
| A.用刀切开金属钠,新切开的钠的表面很快变暗 |
B.向含 的溶液中加入铁粉,溶液颜色变浅 的溶液中加入铁粉,溶液颜色变浅 |
| C.露置在潮湿空气中的钢铁制品,表面产生红色物质 |
D. 溶液和 溶液和 溶液混合,产生刺激性气味 溶液混合,产生刺激性气味 |
您最近一年使用:0次
9 . 除去下列括号内的杂质,所选用的试剂或方法正确的是
A.FeSO4 溶液  :加入过量的铁粉,过滤 :加入过量的铁粉,过滤 |
B. :加入过量的NaOH溶液,过滤 :加入过量的NaOH溶液,过滤 |
| C.CO2(CO):通入氧气,点燃 |
D.NaCl溶液(  :加入过量的 BaCl2溶液,过滤 :加入过量的 BaCl2溶液,过滤 |
您最近一年使用:0次
名校
10 . 基础知识填空
(1)目前用途最广、使用量最大的合金是___________ 。
(2)重晶石的化学式为___________ 。
(3)除去 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为___________ 。
(4)实验室中制备气体 的化学方程式为
的化学方程式为___________ ; 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为___________ 。
(5)规范叙述-用实验方法证明某种白色晶体是
___________ 。
(6)将适量铁粉放入 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是___________ 。
(1)目前用途最广、使用量最大的合金是
(2)重晶石的化学式为
(3)除去
 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为(4)实验室中制备气体
 的化学方程式为
的化学方程式为 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为(5)规范叙述-用实验方法证明某种白色晶体是

(6)将适量铁粉放入
 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次



