名校
解题方法
1 . 工业废水处理是我国环保产业的重要分支。一种处理钢厂酸洗废水(含Fe3+、Fe2+、Al3+等)的工艺流程如下图所示:
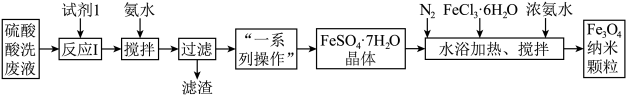
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)反应I的离子方程式为___________ 。
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为___________ 。
(3)通入N2的目的是___________ 。
(4)制备Fe3O4纳米颗粒的离子方程式为___________ 。
(5)如何检验硫酸酸洗废液中是否含有Fe2+?___________
(6)纳米Fe和Fe3O4均可将Cr(Ⅵ)还原为Cr(Ⅲ)从而降解含Cr2O 的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O
的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O 的效果更佳,结合下图,分析其原因:
的效果更佳,结合下图,分析其原因:___________ 。
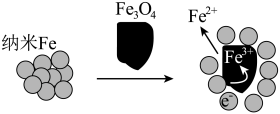
(7)将酸洗废液进行如下实验,检测废液中铁元素含量是否符合国家排放标准。
实验步骤:取100 ml酸洗废液,向其中滴加过量H2O2,微热;用淀粉作指示剂,滴加足量碘化钾至溶液变蓝;最后滴加 0.002 mol/L的硫代硫酸钠溶液至无色,消耗硫代硫酸钠溶液体积为12.7 ml。
已知:I2+2S2O =S4O
=S4O +2I-。废液中铁元素的物质的量浓度为
+2I-。废液中铁元素的物质的量浓度为 ___________ (保留至小数点后两位)。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应I的离子方程式为
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为
(3)通入N2的目的是
(4)制备Fe3O4纳米颗粒的离子方程式为
(5)如何检验硫酸酸洗废液中是否含有Fe2+?
(6)纳米Fe和Fe3O4均可将Cr(Ⅵ)还原为Cr(Ⅲ)从而降解含Cr2O
 的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O
的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O 的效果更佳,结合下图,分析其原因:
的效果更佳,结合下图,分析其原因:
(7)将酸洗废液进行如下实验,检测废液中铁元素含量是否符合国家排放标准。
实验步骤:取100 ml酸洗废液,向其中滴加过量H2O2,微热;用淀粉作指示剂,滴加足量碘化钾至溶液变蓝;最后滴加 0.002 mol/L的硫代硫酸钠溶液至无色,消耗硫代硫酸钠溶液体积为12.7 ml。
已知:I2+2S2O
 =S4O
=S4O +2I-。废液中铁元素的物质的量浓度为
+2I-。废液中铁元素的物质的量浓度为
您最近半年使用:0次
名校
2 . 室温下,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向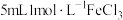 溶液中滴加 溶液中滴加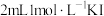 溶液,充分反应后,滴加KSCN溶液,观察现象 溶液,充分反应后,滴加KSCN溶液,观察现象 | 该反应是否为可逆反应 |
| B | 用pH计分别测定的 溶液和 溶液和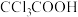 溶液的pH 溶液的pH | 探究键的极性对羧酸酸性的影响 |
| C | 向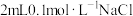 溶液中滴加2滴 溶液中滴加2滴 ,观察现象。振荡试管,再滴加2滴 ,观察现象。振荡试管,再滴加2滴 溶液,观察现象 溶液,观察现象 | 比较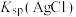 与 与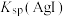 的大小 的大小 |
| D | 向CO还原Fe2O3所得到的产物中加入稀盐酸,滴加KSCN溶液,观察颜色变化 | Fe2O3全部被还原 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-17更新
|
500次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高三下学期阶段练习化学试题
3 . 研究性学习小组对 及其化合物的相关性质进行探究。
及其化合物的相关性质进行探究。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。
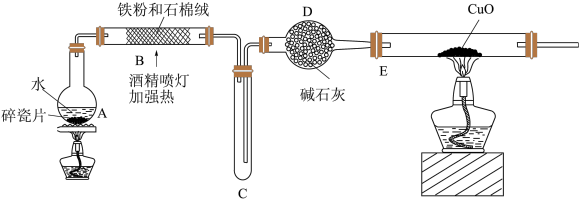
(1)A中放碎瓷片的目的是_______ 。
(2)硬质玻璃管b中发生反应的化学方程式为:_______ 。
(3)装置D的作用是_______ 。
探究二:确定探究一反应后硬质玻璃管B中黑色固体的成分。
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,进行如下实验,请将下表补充完整:
探究三:利用如下图所示装置制备 。
。
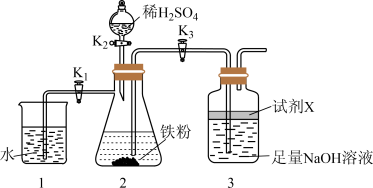
(5)试剂X可选用植物油,其主要作用是_______ 。
(6)实验开始时,打开分液漏斗塞子,关闭 ,依次打开
,依次打开 、
、 的目的是
的目的是_______ 。一段时间后关闭 ,打开
,打开 ,可观察到的现象是
,可观察到的现象是_______ 。
 及其化合物的相关性质进行探究。
及其化合物的相关性质进行探究。探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。

(1)A中放碎瓷片的目的是
(2)硬质玻璃管b中发生反应的化学方程式为:
(3)装置D的作用是
探究二:确定探究一反应后硬质玻璃管B中黑色固体的成分。
(4)将硬质玻璃管中反应后的固体混合物全部取出置于烧杯中,加入足量的盐酸溶解并过滤,进行如下实验,请将下表补充完整:
| 步骤 | 现象 | 解释(用离子方程式表示) | 结论 |
I.取少量滤液,滴加 溶液 溶液 | 溶液不变红,为浅绿色 | 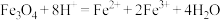 ① | 滤液中的阳离子为③ |
Ⅱ.取少量滤液,滴加 溶液 溶液 | 刚开始无明显现象,一段时间后先出现白色沉淀,迅速变为灰绿色,最终变为红褐色 | ② (白色); (白色);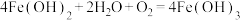 |
探究三:利用如下图所示装置制备
 。
。
(5)试剂X可选用植物油,其主要作用是
(6)实验开始时,打开分液漏斗塞子,关闭
 ,依次打开
,依次打开 、
、 的目的是
的目的是 ,打开
,打开 ,可观察到的现象是
,可观察到的现象是
您最近半年使用:0次
23-24高一下·全国·课后作业
名校
4 . 下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比)化学反应的产物并不改变的是
| A.Li和O2 | B.NaOH和CO2 | C.Fe和稀硝酸 | D.木炭(C)和CuO |
您最近半年使用:0次
2024-03-12更新
|
227次组卷
|
4卷引用:5.2.3硝酸和酸雨的防治课后作业基础篇
解题方法
5 . 下列除杂方法不正确的是
| 选项 | 物质 | 杂质 | 方法 |
| A |  |  | 加入过量NaOH溶液,充分反应,过滤、洗涤、干燥 |
| B |  |  | 将气体通入饱和食盐水中,再通过浓硫酸 |
| C |  固体 固体 |  固体 固体 | 将混合物充分加热 |
| D |  溶液 溶液 |  | 向溶液中加入过量Fe粉,充分反应,过滤 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 在FeCl3腐蚀铜电路板后的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
| A.溶液中一定不含Cu2+ | B.溶液中一定含Fe2+ |
| C.加入KSCN溶液一定不变红色 | D.剩余固体中一定含Cu |
您最近半年使用:0次
7 . 将一定量的Fe、 、CuO的混合物放入100mL
、CuO的混合物放入100mL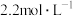 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
 、CuO的混合物放入100mL
、CuO的混合物放入100mL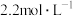 的
的 溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有
溶液中,充分反应后生成896ml。气体(标准状况下),得到不溶固体1.28g,过滤后,滤液中的金属离子只有 (假设滤液体积仍为100mL)。向滤液中滴加
(假设滤液体积仍为100mL)。向滤液中滴加 NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是
NaOH溶液,直至40mL时开始出现沉淀。下列说法错误的是| A.CuO的质量为1.6g |
B.未滴加NaOH溶液前滤液中 的物质的量浓度为 的物质的量浓度为 |
C.溶液中 和 和 消耗铁的物质的量之比为2:1 消耗铁的物质的量之比为2:1 |
| D.Fe在溶液中共参与了三个反应 |
您最近半年使用:0次
名校
解题方法
8 . 下列离子方程式书写正确的是
A.氯气与水反应: |
B. 与 与 反应: 反应: |
C. 与 与 溶液反应: 溶液反应: |
D.小苏打溶液中加入过量的石灰水: |
您最近半年使用:0次
名校
9 . 下列除去杂质(括号中的物质为杂质)的方法中,正确 的是
A. 气体(HCl):通过饱和 气体(HCl):通过饱和 溶液洗气后干燥 溶液洗气后干燥 |
B. 溶液( 溶液( ):加入适量铁粉 ):加入适量铁粉 |
C. 溶液( 溶液( ):通入足量 ):通入足量 |
D. 固体( 固体( ):加入足量的盐酸,过滤 ):加入足量的盐酸,过滤 |
您最近半年使用:0次
2024-03-05更新
|
155次组卷
|
2卷引用:安徽省合肥市六校联盟2023-2024学年高一上学期1月期末化学试题
10 . 下列实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 淀粉和稀硫酸的混合溶液加热发生水解反应一段时间后,取样、冷却,加足量NaOH溶液中和,并滴加碘水 | 滴加碘水后,溶液并未变蓝色 | 说明淀粉已经水解完全 |
| B | 将适量氯气通入Na2S溶液中 | 淡黄色沉淀生成 | 非金属性:Cl>S |
| C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有+3价铁 |
| D | 向某溶液中先加入适量Ba(NO3)2溶液,后再加足量盐酸 | 先产生白色沉淀,后沉淀并不溶解 | 原溶液中一定有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



