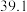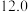解题方法
1 . (1)中国化学家研究出一种新型复合光催化剂(C3N4/CQDs),能利用太阳光高效分解水,原理如图所示。

已知化学键键能如下表:
①反应I的化学方程式为___________________________ 。
②写出反应II的热化学方程式________________________________________ 。
③设总反应反应热为△H,反应I反应热为△H1,则△H____ △H1(填“>”“<” 或“=”)。
(2)已知 H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2。H3PO2水溶液中存在H3PO2分子。H3PO2易被氧化为H3PO4磷酸。
①写出次磷酸的电离方程式______________________________ 。
②常温下,NaH2PO2溶液的pH__________ 。
A.>7 B.<7 C.=7 D.不能确定
③向H3PO2溶液中逐滴加入等浓度的NaOH溶液至过量,其导电性变化图象为_____ ;
向稀NaOH溶液中逐滴滴加浓H3PO2溶液至恰好中和,其导电性变化图象为_____ 。

④常温下磷酸和氢氧化钠溶液反应获得含磷各物种的分布分数与pH的关系如图所示。
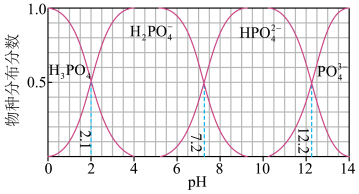
由图分析:H3PO4的Ka1=______ ;利用图中数据计算推测Na2HPO4溶液的酸碱性______________________________ 。

已知化学键键能如下表:
| 共价键 | O—H | O—O | O=O |
| 键能/(kJ∙mol-1) | 464 | 146 | 498 |
①反应I的化学方程式为
②写出反应II的热化学方程式
③设总反应反应热为△H,反应I反应热为△H1,则△H
(2)已知 H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2。H3PO2水溶液中存在H3PO2分子。H3PO2易被氧化为H3PO4磷酸。
①写出次磷酸的电离方程式
②常温下,NaH2PO2溶液的pH
A.>7 B.<7 C.=7 D.不能确定
③向H3PO2溶液中逐滴加入等浓度的NaOH溶液至过量,其导电性变化图象为
向稀NaOH溶液中逐滴滴加浓H3PO2溶液至恰好中和,其导电性变化图象为

④常温下磷酸和氢氧化钠溶液反应获得含磷各物种的分布分数与pH的关系如图所示。

由图分析:H3PO4的Ka1=
您最近一年使用:0次
名校
2 . 近年来我国大力加强温室气体 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
(1)已知:


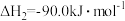
写出 催化氢化合成甲醇的热化学方程式
催化氢化合成甲醇的热化学方程式_____ 。
(2)为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是______ (填序号)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由 催化氢化合成
催化氢化合成 ,如图为不同投料比
,如图为不同投料比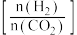 时某反应物X的平衡转化率的变化曲线。
时某反应物X的平衡转化率的变化曲线。
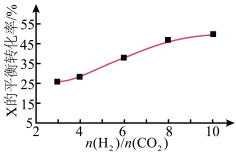
反应物X是___ (填“ ”或“
”或“ ”)。
”)。
(4)250℃时,在体积为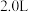 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。
①前10min内 的平均反应速率
的平均反应速率
____  。
。
②化学平衡常数
________ 。
③催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下四组实验数据:
根据上表所给数据,用 生产甲醇的最优条件为
生产甲醇的最优条件为___ (填实验编号)。
 催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:
催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。回答下列问题:(1)已知:



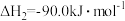
写出
 催化氢化合成甲醇的热化学方程式
催化氢化合成甲醇的热化学方程式(2)为提高
 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是a.高温高压 b.低温低压 c.高温低压 d.低温高压
(3)250℃时,在恒容密闭容器中由
 催化氢化合成
催化氢化合成 ,如图为不同投料比
,如图为不同投料比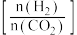 时某反应物X的平衡转化率的变化曲线。
时某反应物X的平衡转化率的变化曲线。
反应物X是
 ”或“
”或“ ”)。
”)。(4)250℃时,在体积为
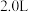 的恒容密闭容器中加入
的恒容密闭容器中加入 、
、 和催化剂,10min时反应达到平衡,测得
和催化剂,10min时反应达到平衡,测得 。
。①前10min内
 的平均反应速率
的平均反应速率
 。
。②化学平衡常数

③催化剂和反应条件与反应物的转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,得到如下四组实验数据:
实验编号 | 温度/K | 催化剂 |
| 甲醇的选择性/% |
A | 543 |
|
|
|
B | 543 |
|
|
|
C | 553 |
|
|
|
D | 553 |
|
|
|
根据上表所给数据,用
 生产甲醇的最优条件为
生产甲醇的最优条件为
您最近一年使用:0次
2020-10-10更新
|
339次组卷
|
8卷引用:鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨 高效手册
鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化——工业合成氨 高效手册人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控四川省成都新津为明学校2020-2021学年高二上学期期中测试化学试题甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)湖北省沙市中学2022-2023学年高二上学期第二次月考化学试题广东省揭阳华侨高级中学2021-2022学年高二上学期期中考试化学试题广东省江门市新会区陈经纶中学2022-2023学年高二上学期第5段月考化学试题(已下线)化学反应速率与化学平衡——课时7化学反应的调控
解题方法
3 . 氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。回答下列问题:
(1)氧化还原法消除NOx的转化如下:
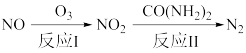
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为_______________ 。
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。
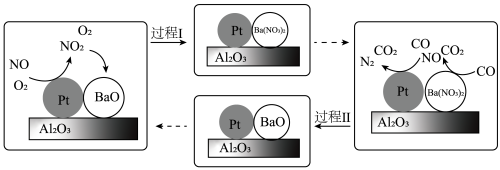
①BaO吸收NO2的化学方程式是______________ 。
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是_______________ 。
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
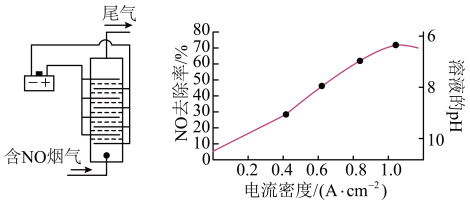
①NO被阳极产生的氧化性物质氧化为 反应的离子方程式为
反应的离子方程式为_______________ 。
②溶液的pH对NO去除率影响的原因是_______________ 。
(1)氧化还原法消除NOx的转化如下:
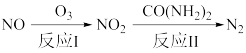
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。

①BaO吸收NO2的化学方程式是
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
①NO被阳极产生的氧化性物质氧化为
 反应的离子方程式为
反应的离子方程式为②溶液的pH对NO去除率影响的原因是
您最近一年使用:0次
2020-09-25更新
|
442次组卷
|
2卷引用:湖北省黄冈市2021届高三9月质量检测化学试题
名校
4 . 设NA为阿伏加 德罗常数的值。下列有关叙述正确的是 ( )
| A.25℃时,pH=8的NaHCO3溶液中含有OH-的数目为10-6NA |
| B.粗铜的电解精炼过程中,若阳极质量减少10g,则阴极质量一定增加10g |
| C.常温常压下,4.6 g NO2所含的氮原子数目为0.1NA |
| D.向1L 1mol/L (CH3COO)2Ba溶液中加入醋酸至中性,混合液中CH3COO-数目为NA |
您最近一年使用:0次
2020-09-25更新
|
1803次组卷
|
8卷引用:辽宁省六校协作体2021届高三第一次联考化学试题
辽宁省六校协作体2021届高三第一次联考化学试题辽宁省开原市中固镇第二中学2021届高三上学期9月月考化学试题辽宁省大连市普兰店区第三十八中学2021届高三上学期第四次考试化学试题武汉市第六中学2022-2023学年高二上学期第二次月考化学试题(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点02 物质的量 气体摩尔体积-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第6周 晚练题-备战2022年高考化学周测与晚练(新高考专用)(已下线)微专题03 破解“七陷阱”突破NA-备战2023年高考化学一轮复习考点微专题
名校
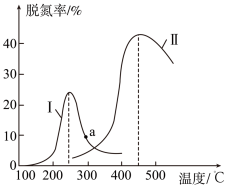
5 . 某研究小组探究催化剂对CO、NO转化的影响。将含NO和CO的尾气以一定的流速通过两种不同的催化剂进行反应:2NO(g)+2CO(g)  N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
 N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
| A.①③⑥ | B.①③④ | C.②③④ | D.①③⑤ |
您最近一年使用:0次
6 . 以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
I.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。
(1)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g) 2I(g)(慢反应)
2I(g)(慢反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(快反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
下列表述正确的是___________
A.N2O浓度越高其分解速率越快 B.第一步对总反应速率起决定作用
C.第一步活化能比第三步大 D.IO为反应的催化剂
II.1,2-二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
①CH2=CHCH3(g)+Cl2(g) CH2ClCHCICH3(g)ΔH1=-134kJ∙mol-1
CH2ClCHCICH3(g)ΔH1=-134kJ∙mol-1
②CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g)ΔH2=-102kJ∙mol-1
CH2=CHCH2Cl(g)+HCl(g)ΔH2=-102kJ∙mol-1
请回答下列问题:
(2)已知CH2=CHCH2C(g)+HCl(g) CH2ClCHClCH(g)的活化能Ea(正)为132kJ∙mol-1,则该反应的活化能Ea(逆)为
CH2ClCHClCH(g)的活化能Ea(正)为132kJ∙mol-1,则该反应的活化能Ea(逆)为__________ kJ∙mol-1。
(3)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①、②,容器内气体的压强随时间的变化如下表所示。
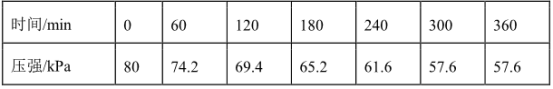
若用单位时间内气体分压的变化来表示反应速率,即v=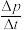 ,则前120min内平均反应速率v(CH2ClCHClCH3)=
,则前120min内平均反应速率v(CH2ClCHClCH3)=________ kPamin-1(保留小数点后2位)。
(4)某研究小组向密闭容器中充入一定量的CH2=CHCH3和Cl2分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH2ClCHClCH3的产率与温度的关系如图所示。下列说法错误的是__________ (填代号)。
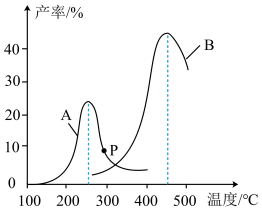
a.使用催化剂A的最佳温度约为250℃
b.相同条件下,改变压强会影响CH2ClCHClCH3的产率
c.p点是对应温度下CH2ClCHClCH3的平衡产率
d.提高CH2ClCHClCH3反应选择性的关键因素是控制温度
(5)在四个恒容密闭容器中充入相应量的气体(如图):

发生反应2N2O(g) 2N2(g)+O2(g)ΔH,容器I、II、II中N2O的平衡转化率如图所示:
2N2(g)+O2(g)ΔH,容器I、II、II中N2O的平衡转化率如图所示:
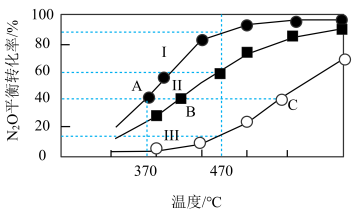
容器I、IV的体积为1L,容器IV中的物质也在470°C下进行反应,起始反应速率:
①v正(N2O)_____ v逆(N2)。(填“>”“<”或“=”)
②图中A、B、C三点处容器内密度最小点是__________ (填“A”“B”或“C”)。
I.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。
(1)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)
 2I(g)(慢反应)
2I(g)(慢反应)第二步I(g)+N2O(g)→N2(g)+IO(g)(快反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
下列表述正确的是
A.N2O浓度越高其分解速率越快 B.第一步对总反应速率起决定作用
C.第一步活化能比第三步大 D.IO为反应的催化剂
II.1,2-二氯丙烷(CH2ClCHClCH3)是一种重要的化工原料,工业上可用丙烯加成法制备,主要副产物为3-氯丙烯(CH2=CHCH2Cl),反应原理为:
①CH2=CHCH3(g)+Cl2(g)
 CH2ClCHCICH3(g)ΔH1=-134kJ∙mol-1
CH2ClCHCICH3(g)ΔH1=-134kJ∙mol-1②CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl(g)+HCl(g)ΔH2=-102kJ∙mol-1
CH2=CHCH2Cl(g)+HCl(g)ΔH2=-102kJ∙mol-1请回答下列问题:
(2)已知CH2=CHCH2C(g)+HCl(g)
 CH2ClCHClCH(g)的活化能Ea(正)为132kJ∙mol-1,则该反应的活化能Ea(逆)为
CH2ClCHClCH(g)的活化能Ea(正)为132kJ∙mol-1,则该反应的活化能Ea(逆)为(3)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①、②,容器内气体的压强随时间的变化如下表所示。

若用单位时间内气体分压的变化来表示反应速率,即v=
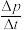 ,则前120min内平均反应速率v(CH2ClCHClCH3)=
,则前120min内平均反应速率v(CH2ClCHClCH3)=(4)某研究小组向密闭容器中充入一定量的CH2=CHCH3和Cl2分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH2ClCHClCH3的产率与温度的关系如图所示。下列说法错误的是

a.使用催化剂A的最佳温度约为250℃
b.相同条件下,改变压强会影响CH2ClCHClCH3的产率
c.p点是对应温度下CH2ClCHClCH3的平衡产率
d.提高CH2ClCHClCH3反应选择性的关键因素是控制温度
(5)在四个恒容密闭容器中充入相应量的气体(如图):

发生反应2N2O(g)
 2N2(g)+O2(g)ΔH,容器I、II、II中N2O的平衡转化率如图所示:
2N2(g)+O2(g)ΔH,容器I、II、II中N2O的平衡转化率如图所示:
容器I、IV的体积为1L,容器IV中的物质也在470°C下进行反应,起始反应速率:
①v正(N2O)
②图中A、B、C三点处容器内密度最小点是
您最近一年使用:0次
7 . 推动煤炭清洁高效利用是未来煤炭利用的发展方向,其中煤制天然气(主要成分甲烷)能对燃气资源有重要补充作用。
在催化剂作用下,其涉及的主要反应如下:
CO(g) +3H2(g)⇌CH4(g)+H2O(g)△H1Ⅰ
CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2═-41.2 kJ∙mol−1Ⅱ
CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)△H3Ⅲ
其副反应(积碳反应)如下:
2CO(g)⇌CO2(g)+C(s) △H4═-172.0kJ•mol﹣1Ⅳ
CO2(g)+2H2(g)⇌2H2O(g)+C(s) △H5═-90.0kJ•mol﹣1Ⅴ
CO(g)+H2(g)⇌H2O(g)+C(s) △H6═-131.0kJ•mol﹣1Ⅵ
(1)荷兰埃因霍温大学学者结合实验与计算机模拟结果,研究了在催化剂钴表面上反应Ⅰ的反应历程,如图所示,其中吸附在钴催化剂表面上的物种用*标注。
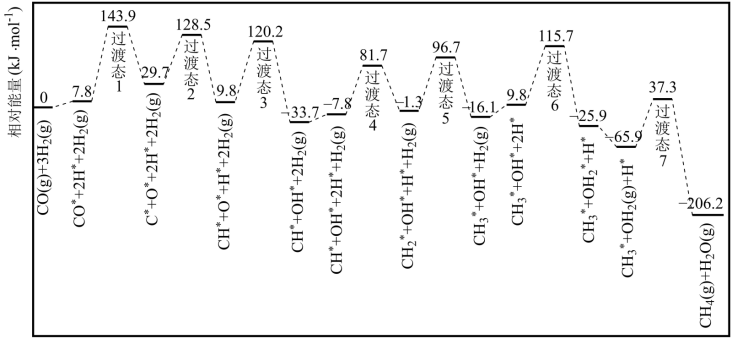
①该历程中最大能垒E正=_____ kJ∙mol−1,写出该步骤的化学方程式_____ 。
②△H3=_____ kJ∙mol−1。
(2)若原料气n(H2):n(CO)=3:1,且反应容器中只考虑主要反应。
①在催化剂作用下合成天然气,平衡时各组分的体积分数随温度、压强变化如图2、图3所示。根据图象分析,反应Ⅰ在_____ 温(填“高”或“低”)、_____ 压(填“高“或“低”)条件下有利于反应进行。
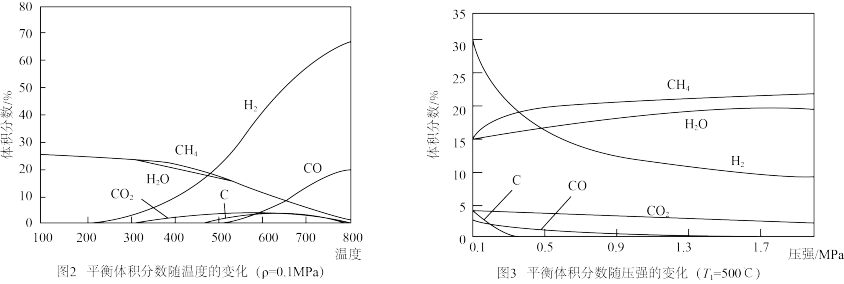
②T2℃,0.1MPa恒压条件条件下,平衡时反应体系平衡组成如表所示。
该条件下CO的总转化率表达式α=_____ 。Kp、Kx分别是以分压、物质的量分数表示的平衡常数,反应Ⅰ的Kx=_____ 。(以Kp和p总表示)
(3)若反应容器中考虑主、副反应。维持p总=0.1MPa恒定,平衡时CO转化率和积碳的选择性(积碳的选择性=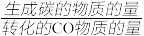 ×100%)随温度和进料气中水蒸气量的变化如图4和图5所示。其中n(H2):n(CO):n(H2O)=3:1:X,代表原料气中H2、CO和H2O三者的物质的量之比,X为一变量,下列说法正确的是
×100%)随温度和进料气中水蒸气量的变化如图4和图5所示。其中n(H2):n(CO):n(H2O)=3:1:X,代表原料气中H2、CO和H2O三者的物质的量之比,X为一变量,下列说法正确的是_____ 。

A图4中,随着X的增大,CO转化率略有降低,可能原因是反应式Ⅰ中H2O为生成物,增加水蒸气的量会促使平衡向逆反应方向移动
B图5中,X较低时,在800~850℃积碳选择性减小的原因可能是副反应为放热反应,温度较高,积碳反应平衡逆向移动
C图5中,X较高时,在550~800℃积碳选择性较低的主要原因是水蒸气的稀释作用使积碳反应速率减小
D总体上说,X较高,温度低于450℃利于降低积碳,减少积碳对催化剂的影响
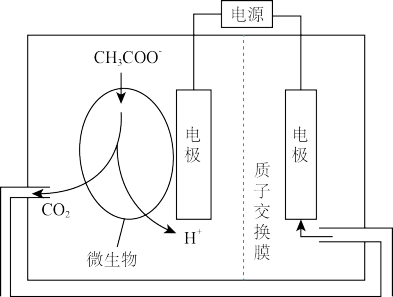
(4)生物电化学系统还原CO2是另一种产生甲烷的方法,装置如图所示,请写出电解时阴极的电极反应式_____ 。
在催化剂作用下,其涉及的主要反应如下:
CO(g) +3H2(g)⇌CH4(g)+H2O(g)△H1Ⅰ
CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2═-41.2 kJ∙mol−1Ⅱ
CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)△H3Ⅲ
其副反应(积碳反应)如下:
2CO(g)⇌CO2(g)+C(s) △H4═-172.0kJ•mol﹣1Ⅳ
CO2(g)+2H2(g)⇌2H2O(g)+C(s) △H5═-90.0kJ•mol﹣1Ⅴ
CO(g)+H2(g)⇌H2O(g)+C(s) △H6═-131.0kJ•mol﹣1Ⅵ
(1)荷兰埃因霍温大学学者结合实验与计算机模拟结果,研究了在催化剂钴表面上反应Ⅰ的反应历程,如图所示,其中吸附在钴催化剂表面上的物种用*标注。

①该历程中最大能垒E正=
②△H3=
(2)若原料气n(H2):n(CO)=3:1,且反应容器中只考虑主要反应。
①在催化剂作用下合成天然气,平衡时各组分的体积分数随温度、压强变化如图2、图3所示。根据图象分析,反应Ⅰ在

②T2℃,0.1MPa恒压条件条件下,平衡时反应体系平衡组成如表所示。
| 组分 | CH4 | H2O | H2 | CO2 | CO |
| 体积分数x | a | b | c | d | e |
(3)若反应容器中考虑主、副反应。维持p总=0.1MPa恒定,平衡时CO转化率和积碳的选择性(积碳的选择性=
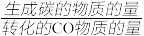 ×100%)随温度和进料气中水蒸气量的变化如图4和图5所示。其中n(H2):n(CO):n(H2O)=3:1:X,代表原料气中H2、CO和H2O三者的物质的量之比,X为一变量,下列说法正确的是
×100%)随温度和进料气中水蒸气量的变化如图4和图5所示。其中n(H2):n(CO):n(H2O)=3:1:X,代表原料气中H2、CO和H2O三者的物质的量之比,X为一变量,下列说法正确的是
A图4中,随着X的增大,CO转化率略有降低,可能原因是反应式Ⅰ中H2O为生成物,增加水蒸气的量会促使平衡向逆反应方向移动
B图5中,X较低时,在800~850℃积碳选择性减小的原因可能是副反应为放热反应,温度较高,积碳反应平衡逆向移动
C图5中,X较高时,在550~800℃积碳选择性较低的主要原因是水蒸气的稀释作用使积碳反应速率减小
D总体上说,X较高,温度低于450℃利于降低积碳,减少积碳对催化剂的影响
(4)生物电化学系统还原CO2是另一种产生甲烷的方法,装置如图所示,请写出电解时阴极的电极反应式

您最近一年使用:0次
2020-08-21更新
|
416次组卷
|
2卷引用:湖北省武汉市华中师大第一附中高考化学押题试卷
解题方法
8 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如图所示。下列叙述正确的是( )
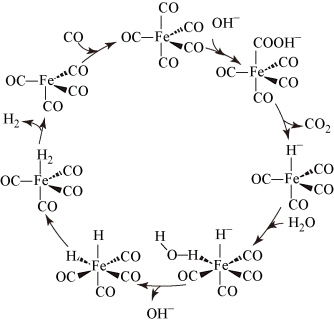

| A.该反应可消耗温室气体CO2 |
| B.OH- 作为中间产物参与了该催化循环 |
| C.该催化循环中Fe的成键数目发生了变化 |
| D.该反应可产生清洁燃料H2 |
您最近一年使用:0次
9 . “绿水青山就是金山银山”,研究碳、氮、硫等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)已知:①NO2(g)+CO(g) CO2(g)+NO(g) △H=-232.0 kJ·mol-1
CO2(g)+NO(g) △H=-232.0 kJ·mol-1
②N2(g)+O2(g) 2NO(g) △H=+180.0 kJ·mol-1
2NO(g) △H=+180.0 kJ·mol-1
③2NO(g)+O2(g) 2NO2(g) △H=-122.2 kJ·mol-1
2NO2(g) △H=-122.2 kJ·mol-1
则NO与CO反应生成无污染物气体的热化学方程式为__________ 。
(2)工业上用CO与H2制备甲醇可消除CO污染,其反应为:CO(g)+2H2(g) CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
①若P前=9.00MPa,则该反应的平衡常数Kp=_____ MPa-2(用平衡分压代替平衡浓度计算,分压=总压×体积分数);
②若平衡后再向容器中充入1 mol CO与2 mol H2,则重新平衡后CO的体积分数与原平衡相比___ (填“增大”、“不变”、“减小”)。
(3)甲醇碱性燃料电池因性能优异而被人们青睐,请写出其负极的电极反应式:_____ 。
(4)工业上常用过量浓氨水吸收硫酸工业尾气SO2,请写出其离子方程式_____ 。
(1)已知:①NO2(g)+CO(g)
 CO2(g)+NO(g) △H=-232.0 kJ·mol-1
CO2(g)+NO(g) △H=-232.0 kJ·mol-1②N2(g)+O2(g)
 2NO(g) △H=+180.0 kJ·mol-1
2NO(g) △H=+180.0 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) △H=-122.2 kJ·mol-1
2NO2(g) △H=-122.2 kJ·mol-1则NO与CO反应生成无污染物气体的热化学方程式为
(2)工业上用CO与H2制备甲醇可消除CO污染,其反应为:CO(g)+2H2(g)
 CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)。某温度下,将1 mol CO与2 mol H2充入体积为1 L的恒容密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| P后/P前 | 0.75 | 0.62 | 0.52 | 0.44 | 0.40 | 0.40 |
①若P前=9.00MPa,则该反应的平衡常数Kp=
②若平衡后再向容器中充入1 mol CO与2 mol H2,则重新平衡后CO的体积分数与原平衡相比
(3)甲醇碱性燃料电池因性能优异而被人们青睐,请写出其负极的电极反应式:
(4)工业上常用过量浓氨水吸收硫酸工业尾气SO2,请写出其离子方程式
您最近一年使用:0次
解题方法
10 . 乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)→C2H4ΔH1=—174.3kJ•mol-1 K1(300K)=3.37×1024
C2H2(g)+2H2(g)→C2H6ΔH2=—311.0kJ•mol-1 K2(300K)=1.19×1042
则反应C2H4(g)+H2(g)→C2H6的ΔH=____________ kJ•mol-1,K(300K)=____________ (保留三位有效数字)
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。

上述吸附反应为____________ (填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____________ kJ•mol-1,该步骤的化学方程式为____________ 。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g) C2H2(g)+H2(g)。
C2H2(g)+H2(g)。
①乙烯的离解率为α,平衡时容器内气体总压强为p总,则分压p(C2H4)=____________ (用p总和α表示)。
②在1000K时,该反应的Kp=2×10-3atm,平衡时容器内气体的总压强为10atm,则乙烯的离解率为____________ (精确到0.001,已知 ≈1.4)。
≈1.4)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为____________ (填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为____________ 。
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)→C2H4ΔH1=—174.3kJ•mol-1 K1(300K)=3.37×1024
C2H2(g)+2H2(g)→C2H6ΔH2=—311.0kJ•mol-1 K2(300K)=1.19×1042
则反应C2H4(g)+H2(g)→C2H6的ΔH=
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。

上述吸附反应为
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)
 C2H2(g)+H2(g)。
C2H2(g)+H2(g)。①乙烯的离解率为α,平衡时容器内气体总压强为p总,则分压p(C2H4)=
②在1000K时,该反应的Kp=2×10-3atm,平衡时容器内气体的总压强为10atm,则乙烯的离解率为
 ≈1.4)。
≈1.4)。(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为
您最近一年使用:0次

 纳米棒
纳米棒