解题方法
1 . 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量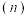 随着时间
随着时间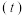 变化的曲线如图所示.下列说法正确的是
变化的曲线如图所示.下列说法正确的是

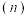 随着时间
随着时间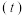 变化的曲线如图所示.下列说法正确的是
变化的曲线如图所示.下列说法正确的是
A.该反应的化学方程式为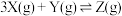 |
| B.混合气体的总质量不随时间的变化而变化,说明反应已达化学平衡状态 |
C.0到2min内用Y表示的平均反应速率为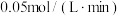 |
| D.达到平衡时X的转化率为30% |
您最近一年使用:0次
解题方法
2 . 雾霾天气多次肆虐我国中东部地区。汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
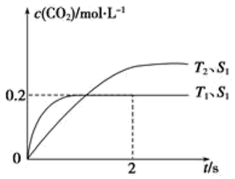
据此判断:
①该反应的ΔH___________ 0(填“>”或“<”),ΔS___________ 0(填“>”或“<”)
②在T1温度下,0~2 s内的平均反应速率v(N2)=___________ 。
③当固体催化剂的质量一定时,增大其表面积可提高化学 反应速率。若增大催化剂的表面积,则CO转化率___________ (填“增大”,“减少”或“不变”)
(2)工业上可采用CH3OH CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
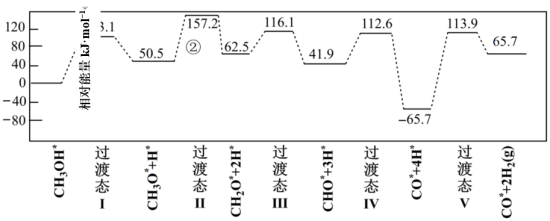
该历程中最大能垒(活化能)E正=___________ kJ·mol−1,该历程中,放热最多的步骤的化学方程式为___________ 。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)
 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如下图所示。
据此判断:
①该反应的ΔH
②在T1温度下,0~2 s内的平均反应速率v(N2)=
③当固体催化剂的质量一定时,增大其表面积可提高化学 反应速率。若增大催化剂的表面积,则CO转化率
(2)工业上可采用CH3OH
 CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
CO + 2H2的方法来制取高纯度的CO和H2。我国研究人员采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物种用 * 标注。下图为计算机模拟的各步反应的能量变化示意图:
该历程中最大能垒(活化能)E正=
您最近一年使用:0次
3 . 一定条件下在容积不变的容器中充入 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:

ⅰ.起始投料比 均为2:3;
均为2:3;
ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
 和
和 发生如下反应:
发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。已知:
与时间的关系如图所示。已知:
ⅰ.起始投料比
 均为2:3;
均为2:3;ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确的是
| A.Ⅰ、Ⅱ曲线证明催化剂比表面积对上述反应有影响 |
B.Ⅱ中 的平衡转化率为50% 的平衡转化率为50% |
C.在Ⅲ的条件下,该反应的平衡常数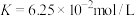 |
D. min,Ⅲ中平均反应速率 min,Ⅲ中平均反应速率 |
您最近一年使用:0次
4 . 化石燃料的燃烧、汽车尾气的排放和硝酸工业尾气中普遍含有的NOx是污染大气的主要成分之一,需要回收处理并加以利用。
(1)为减轻汽车尾气中NO和CO对环境的污染,可在汽车排气管上安装催化转化器,主要发生的反应是:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH。
N2(g)+2CO2(g) ΔH。
已知断裂1mol相应化学键需要的能量如表:
则ΔH为___________ 。
(2)已知:CH4(g)+4NO2(g)=CO2(g)+2H2O(l)+4NO(g) ΔH=-654kJ·mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(l)+2N2(g) ΔH=-1240kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
CH4将NO2还原为N2并生成水蒸气的热化学方程式为___________ 。
(3)燃煤烟气脱硝的反应之一为 2NO2(g) + 4CO(g) N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
0~2 min内该反应的平均速率为v(N2)=___________ , 8分钟时反应达到平衡,则NO2的平衡转化率=___________ ;n值可能为___________ (填字母)。
A.3.2 B.3.36 C.3.3 D.3.1
(4)NH3催化还原氮氧化物技术(SCR)是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示:
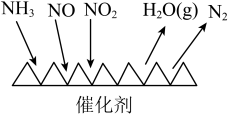
用Fe作催化剂时,在氨气足量的情况下,当c(NO2):c(NO)=1:1时,脱氮率最佳,按最佳脱氮率,每生成2mol N2,转移电子数目为___________ 。
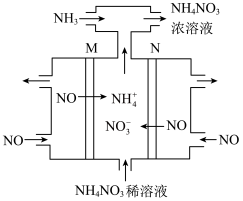
(5)除上述方法外,还可用电解法将NO转变为NH4NO3,其工作原理如下图,N极的电极反应式为___________ ,通入NH3的主要原因是___________ 。
(1)为减轻汽车尾气中NO和CO对环境的污染,可在汽车排气管上安装催化转化器,主要发生的反应是:2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH。
N2(g)+2CO2(g) ΔH。已知断裂1mol相应化学键需要的能量如表:
| 化学键 | C≡O | N≡O | N≡N | C=O |
| 键能/(kJ·mol-1) | 1072 | 630 | 946 | 799 |
(2)已知:CH4(g)+4NO2(g)=CO2(g)+2H2O(l)+4NO(g) ΔH=-654kJ·mol-1
CH4(g)+4NO(g)=CO2(g)+2H2O(l)+2N2(g) ΔH=-1240kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
CH4将NO2还原为N2并生成水蒸气的热化学方程式为
(3)燃煤烟气脱硝的反应之一为 2NO2(g) + 4CO(g)
 N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:
N2(g)+ 4CO2(g),在一定温度下,向2 L恒容密闭容器中充入4. 0 mol NO2,测得相关数据如下:| 时间 | 0 min | 2 min | 4 min | 6 min | 8min | 10 min |
| n(NO2)/mol | 4.0 | 3.6 | n | 3.1 | 3.0 | 3.0 |
A.3.2 B.3.36 C.3.3 D.3.1
(4)NH3催化还原氮氧化物技术(SCR)是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图所示:

用Fe作催化剂时,在氨气足量的情况下,当c(NO2):c(NO)=1:1时,脱氮率最佳,按最佳脱氮率,每生成2mol N2,转移电子数目为
(5)除上述方法外,还可用电解法将NO转变为NH4NO3,其工作原理如下图,N极的电极反应式为

您最近一年使用:0次
2024-02-13更新
|
99次组卷
|
2卷引用:宁夏银川市育才中学2023-2024学年高三上学期1月期末理科综合化学试题
5 . 二氧化碳、甲烷是地球大气中的主要温室气体,它们能吸收地面反射的太阳辐射,使地球表面变暖,因此,对二氧化碳、甲烷的高效利用有着举足轻重的作用。回答下列问题:
(1)已知下列反应
①CH4(g)+H2O(g) CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1
②CO(g)+H2O(g) CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2
则二氧化碳重整甲烷反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)△H3=
2CO(g)+2H2(g)△H3=_______ 。
(2)恒温恒容密闭容器中,反应CH4(g)+CO2(g) 2CO(g)+2H2(g)达到平衡状态的标志是
2CO(g)+2H2(g)达到平衡状态的标志是_________ 。
A.容器内的压强保持不变
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.混合气体的平均分子量保持不变
D.混合气体的颜色保持不变
E.单位时间内断裂C-H键和形成H-H键的数目之比为2:1
(3)反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的平衡常数的表达式为
2CO(g)+2H2(g)的平衡常数的表达式为__________ 。
(4)T℃时,向恒容密闭容器中投入CH4和CO2各1mol,发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
①在0~20min内,平均反应速率v(CO)=_________ kPa/min。
②若在恒温恒压密闭容器中进行上述反应,CH4的转化率将_________ (填增大、减小、不变)。
(1)已知下列反应
①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1
CO(g)+3H2(g) △H1②CO(g)+H2O(g)
 CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2则二氧化碳重整甲烷反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g)△H3=
2CO(g)+2H2(g)△H3=(2)恒温恒容密闭容器中,反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)达到平衡状态的标志是
2CO(g)+2H2(g)达到平衡状态的标志是A.容器内的压强保持不变
B.c(CH4):c(CO2):c(CO):c(H2)=1:1:2:2
C.混合气体的平均分子量保持不变
D.混合气体的颜色保持不变
E.单位时间内断裂C-H键和形成H-H键的数目之比为2:1
(3)反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的平衡常数的表达式为
2CO(g)+2H2(g)的平衡常数的表达式为(4)T℃时,向恒容密闭容器中投入CH4和CO2各1mol,发生反应CH4(g)+CO2(g)
 2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):
2CO(g)+2H2(g),测得容器内的气体压强随时间的变化如下表所示(气态物质分压=总压×气态物质的物质的量分数,不考虑其他副反应):| 时间/min | 0 | 10 | 20 | 30 | 50 | 60 |
| 总压/kPa | 100 | 118 | 132 | 141 | 148 | 148 |
②若在恒温恒压密闭容器中进行上述反应,CH4的转化率将
您最近一年使用:0次
名校
6 . 对可逆反应:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),则下列叙述中正确的是
| A.达到化学平衡时,5v正(O2)=4v逆(NO) |
| B.化学反应速率关系是:2v正(NH3)=3v正(H2O) |
| C.若NH3、O2、NO、H2O的分子数之比为4∶5∶4∶6时,反应达到化学平衡状态 |
| D.若单位时间内生成4nmolNO的同时,生成5nmolO2,则反应达到平衡状态 |
您最近一年使用:0次
2024-02-11更新
|
129次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高二上学期1月期末化学试题
名校
解题方法
7 . 在2A(g)+B(g) 3C(g)+5D(g)反应中,表示该反应速率最快的是
3C(g)+5D(g)反应中,表示该反应速率最快的是
 3C(g)+5D(g)反应中,表示该反应速率最快的是
3C(g)+5D(g)反应中,表示该反应速率最快的是| A.v(A)=0.5mol/(L•s) | B.v(B)=0.3mol/(L•s) |
| C.v(C)=0.8mol/(L•s) | D.v(D)=0.4mol/(L•s) |
您最近一年使用:0次
2024-02-11更新
|
124次组卷
|
2卷引用:宁夏石嘴山三中2015~2016学年度高二上学期期末化学试卷【解析版】
名校
解题方法
8 . 工业上采用多种还原剂NH3、CO、H2等还原NO气体。
Ⅰ.NH3还原法。已知:
①
②
(1) 的逆反应活化能与正反应活化能之差等于
的逆反应活化能与正反应活化能之差等于_______ kJ/mol。
(2)在密闭容器中充入4 mol NH3和6 mol NO,发生反应: 。平衡时NO的体积分数与温度、压强的关系如图所示。
。平衡时NO的体积分数与温度、压强的关系如图所示。
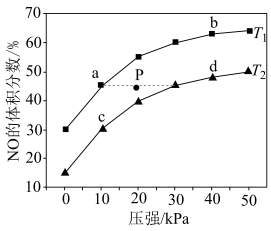
若P点对应的反应容器降温的同时扩大容器体积,重新达到平衡时可能是图中点a、b、c、d中的_______ 点。
Ⅱ.还原法。汽车尾气中的处理原理如图所示:
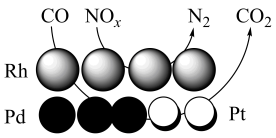
(3)当x=1时,CO和NOx反应中N2与NOx的速率之比为_______ 。其他条件相同,增大催化剂比表面积,反应速率_______ (填“增大”“减小”或“不变”)。
Ⅲ.H2还原法。在某催化剂作用下, 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(4)为了测定反应级数,测得实验数据如下:
由此推知,m=_______ ,n=_______ 。
(5)研究发现H2和NO反应分两步进行:第一步:2NO+H2=N2+H2O2 (很慢);第二步:_______ (补充反应式)(很快),其中,第_______ 步反应控制总反应速率。
(6)一定温度下,向恒容密闭反应器中充入0.4 mol NO和0.8 mol H2,发生反应: 。体系的总压强与时间的关系如图所示。
。体系的总压强与时间的关系如图所示。
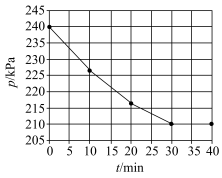
①0~30 min内用H2的分压表示的平均反应速率v(H2)为_______ kPa·min-1。
②该温度下,平衡常数Kp=_______ kPa-1 (Kp为用平衡分压计算的平衡常数,分压=总压×物质的量分数)。
Ⅰ.NH3还原法。已知:
①

②

(1)
 的逆反应活化能与正反应活化能之差等于
的逆反应活化能与正反应活化能之差等于(2)在密闭容器中充入4 mol NH3和6 mol NO,发生反应:
 。平衡时NO的体积分数与温度、压强的关系如图所示。
。平衡时NO的体积分数与温度、压强的关系如图所示。
若P点对应的反应容器降温的同时扩大容器体积,重新达到平衡时可能是图中点a、b、c、d中的
Ⅱ.还原法。汽车尾气中的处理原理如图所示:

(3)当x=1时,CO和NOx反应中N2与NOx的速率之比为
Ⅲ.H2还原法。在某催化剂作用下,
 的速率方程为
的速率方程为 (k为速率常数,只与温度、催化剂有关,m、n为反应级数)。
(k为速率常数,只与温度、催化剂有关,m、n为反应级数)。(4)为了测定反应级数,测得实验数据如下:
| 实验 |  |  | 反应速率 |
| a | 0.1 | 0.1 | v |
| b | 0.2 | 0.1 | 2v |
| c | 0.2 | 0.2 | 8v |
(5)研究发现H2和NO反应分两步进行:第一步:2NO+H2=N2+H2O2 (很慢);第二步:
(6)一定温度下,向恒容密闭反应器中充入0.4 mol NO和0.8 mol H2,发生反应:
 。体系的总压强与时间的关系如图所示。
。体系的总压强与时间的关系如图所示。
①0~30 min内用H2的分压表示的平均反应速率v(H2)为
②该温度下,平衡常数Kp=
您最近一年使用:0次
2024-02-08更新
|
82次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高二上学期1月期末联考化学试题
解题方法
9 . 反应 在四种不同情况下的反应速率如下,其中表示反应速率最快的是
在四种不同情况下的反应速率如下,其中表示反应速率最快的是
 在四种不同情况下的反应速率如下,其中表示反应速率最快的是
在四种不同情况下的反应速率如下,其中表示反应速率最快的是A. | B.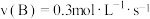 |
C. | D.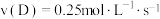 |
您最近一年使用:0次
解题方法
10 . 将 和
和 充入一容积为
充入一容积为 密闭容器中,分别在300℃、T℃发生反应:
密闭容器中,分别在300℃、T℃发生反应: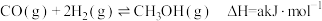 ,根据图示判断,下列说法正确的是
,根据图示判断,下列说法正确的是
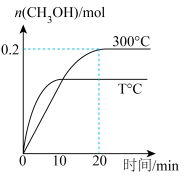
 和
和 充入一容积为
充入一容积为 密闭容器中,分别在300℃、T℃发生反应:
密闭容器中,分别在300℃、T℃发生反应: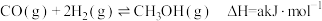 ,根据图示判断,下列说法正确的是
,根据图示判断,下列说法正确的是
A. , , |
B.300℃时,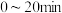 内 内 |
| C.容器内气体密度不变时,反应达到了平衡状态 |
D. 时, 时, 的平衡转化率小于 的平衡转化率小于 |
您最近一年使用:0次



