1 . 下列根据实验现象得出的结论错误的是
| 选项 | 实验目的 | 实验设计 | 实验现象和结论 |
| A | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,加稀硝酸酸化,再加入硝酸钡溶液 | 若有白色沉淀生成,则该溶液中一定含有 |
| B | 探究 和 和 对 对 分解速率的影响 分解速率的影响 | 在两支试管中分别加入2mL5% 溶液,再向 溶液,再向 溶液中分别滴入 溶液中分别滴入 和 和 溶液各1mL,摇匀(已知: 溶液各1mL,摇匀(已知: 对该反应无影响) 对该反应无影响) | 相同时间内产生气泡多的,则催化效果好 |
| C | 探究乙酸和碳酸的酸性强弱 | 用乙酸溶液浸泡水壶中的 水垢 水垢 | 水垢溶解并有气泡冒出,则乙酸的酸性比碳酸的强 |
| D | 检验某气体是否为 | 将气体通入酸性 溶液中 溶液中 | 若 溶液褪色,则该气体不一定是 溶液褪色,则该气体不一定是 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-08-08更新
|
342次组卷
|
3卷引用:河南省部分重点中学2023届高三8月联考化学试题
名校
解题方法
2 . 根据实验目的,下列操作及现象、结论都正确的是
| 实验目的 | 操作及现象 | 结论 | |
| A | 比较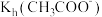 和 和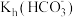 的大小 的大小 | 25℃时, 分别测浓度均为 的 的 和 和 溶液的pH,后者pH大 溶液的pH,后者pH大 | 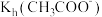 < 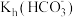 |
| B | 比较 和 和 的大小 的大小 | 将pH相同的 溶液和 溶液和 溶液均稀释10倍后,用pH计测量, 溶液均稀释10倍后,用pH计测量, 的pH大 的pH大 |   |
| C | 比较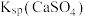 和 和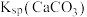 的大小 的大小 | 向饱和CaSO4溶液中滴加相同浓度的Na2CO3溶液,产生白色沉淀 | 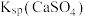 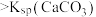 |
| D | 比较Cu2+和Fe3+对 分解的催化效果 分解的催化效果 | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4和FeCl3溶液,后者生成气体的速率快 | 催化效果 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-02-11更新
|
194次组卷
|
2卷引用:山东省淄博市2022-2023学年高二上学期期末考试化学试题
解题方法
3 . 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因_______ 。
(2)实验①和②的目的是_______ 。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是_______ 。
(3)写出实验③的化学反应方程式:_______ 。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是_______ 。
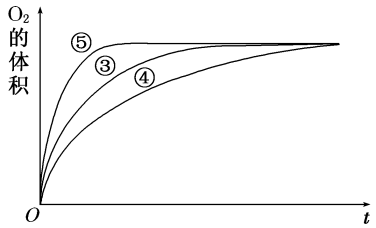
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol • L-1 FeCl3溶液 |
(2)实验①和②的目的是
(3)写出实验③的化学反应方程式:
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是

您最近半年使用:0次
解题方法
4 . 下列实验方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 探究反应物浓度对化学反应速率的影响 | 分别取10mL0.1mol·Lˉ1Na2S2O3溶液和5mL0.1mol·Lˉ1Na2S2O3溶液、5mL蒸馏水于两支试管中,然后同时加入10mL0.1mol·Lˉ1H2SO4溶液 | 前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速率 |
| B | 探究压强对化学反应速率的影响 | 在容积不变的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),向其中通入氩气,反应速率不变 2NH3(g),向其中通入氩气,反应速率不变 | 化学反应速率不受压强影响 |
| C | 探究生成物浓度对化学平衡的影响 | 向2mL0.1mol·L-1FeCl3溶液加入1滴KSCN溶液,再加入少量KCl溶液 | 若溶液先变血红色,加入KCl溶液后血红色变浅,说明增大生成物浓度,平衡逆向移动 |
| D | 探究催化剂对化学反应速率的影响 | 向两支盛有少量H2O2溶液的试管中分别加入5滴0.1mol·Lˉ1FeCl3溶液和5滴0.01mol·Lˉ1CuSO4溶液 | 加入FeCl3溶液的试管生成气体的速率比加入CuSO4溶液的快,说明FeCl3对H2O2分解的催化效果强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
5 . 下列操作中,实验现象与得出的结论不一致的是
| 选项 | 实验目的 | 操作及现象 | 结论 |
| A | 验证Mn2+在KMnO4溶液与 H2C2O4溶液反应中的催化作用 | 取两支洁净的试管各加入5 mL硫酸酸化的0.1mol·L-1KMnO4溶液,在两支试管中分别再加入:①10 mL0.1 mol· L-1 H2C2O4溶液与2 mL MnSO4 溶液;②10 mL 0.1 mol·L-1 H2C2O4溶液与2 mL蒸馏水。加入①的试管紫色先消失 | 证明Mn2+能降低该反应的活化能 |
| B | 判断Ksp(AgCl)与Ksp(AgI)的大小 | 向AgCl悬浊液中加入NaI溶液时白色沉淀转化为黄色沉淀 | Ksp(AgCl)> Ksp(AgI) |
| C | 判断CH3COO-与 水解常数的大小 水解常数的大小 | 相同温度下,分别测定浓度均为0.1 mol·L-1的CH3COONa溶液和Na2CO3溶液的pH,后者大于前者 | 水解常数: Kh(CH3COO- ) <Kh( ) ) |
| D | 判断某FeCl3溶液样品中是否含有Fe2+ | 向某FeCl3溶液样品中加入硫酸酸化的KMnO4溶液,紫色褪去 | 该样品中一定含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-08-08更新
|
740次组卷
|
2卷引用:贵州省铜仁市2021-2022学年高二下学期期末质量检测理综化学试题
名校
6 . 下列设计的实验方案不能达到实验目的的是
| A.从KClO3制O2的残留物中提纯MnO2:将残留物用适量的蒸馏水溶解,过滤、蒸馏水洗涤、干燥 |
B.检验水溶液中NH :取1 mL溶液于试管中,加入1mL NaOH稀溶液,用湿润的红色石蕊试纸放管口,观察实验现象 :取1 mL溶液于试管中,加入1mL NaOH稀溶液,用湿润的红色石蕊试纸放管口,观察实验现象 |
| C.探究FeCl3和KI溶液反应限度:向5 mL 0.1 mol·L-1KI溶液中加入0.1 mol·L -1 FeCl3溶液1 mL,振荡,加苯萃取后,向水层中加入5滴KSCN溶液,观察实验现象 |
| D.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2 mL5%H2O2和1 mL H2O,向另一支试管中加入2 mL 5%H2O2和1 mLFeCl3溶液,观察并比较实验现象 |
您最近半年使用:0次
2022高二·上海·专题练习
7 . 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因是______________________________________ 。
(2)实验①和②的目的是__________________________________ 。
实验时由于没有观察到明显现象而无法得出结论,资料显示,通常条件下H2O2较稳定,不易分解,为了达到实验目的,你对原实验方案的改进是_______________________ 。
(3)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。
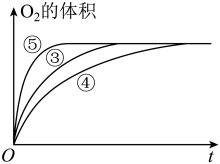
分析上图能够得出的实验结论是______________________ 。
| 实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(2)实验①和②的目的是
实验时由于没有观察到明显现象而无法得出结论,资料显示,通常条件下H2O2较稳定,不易分解,为了达到实验目的,你对原实验方案的改进是
(3)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析上图能够得出的实验结论是
您最近半年使用:0次
8 . 下列实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取5mL0.1mol/LKI溶液,滴加0.1mol/LFeCl3溶液5~6滴,充分反应,可根据溶液中既含I2又含I-的实验事实判断该反应是可逆反应 |
| B | 探究FeCl3对H2O2分解速率的影响 | 相同条件下,向一支试管中加入2mL5%的H2O2和1mLH2O,向另一支试管中加入2mL5%的H2O2和1mLFeCl3溶液,观察并比较实验现象 |
| C | 比较碳酸和硅酸的酸性强弱 | 在CaCO3中加浓盐酸,并将反应后所得气体直接通入Na2SiO3溶液中,溶液变浑浊 |
| D | 探究浓度对化学反应速率的影响 | 常温下,向相同的铁片中分别加入足量的浓、稀硝酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
9 . 下列操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究温度对2NO2(g) ⇌N2O4(g)平衡有影响 | 将充满NO2的密闭玻璃球浸泡在热水中气体红棕色加深 |
| B | 探究催化剂对H2O2分解速率的影响 | 在相同条件下,向一支试管中加入2mL 5%的H2O2溶液和1mL H2O,向另一支试管中加入2mL 10%的H2O2溶液和1mL FeCl3溶液,观察实验现象 |
| C | 证明增大反应物浓度,能加快化学反应速率 | 将两块表面积相同的鋅粒分别放入稀硫酸和浓硫酸 |
| D | 证明KCl中存在离子键 | KCl溶于水是否导电 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 下列实验操作和现象与预期实验目的或所得结论不一致的是
| 选项 | 实验操作和现象 | 预期实验目的或所得结论 |
| A | 将酸性KMnO4溶液滴入丙烯醛中,溶液的紫红色褪去 | 不能说明丙烯醛中含有碳碳双键 |
| B | 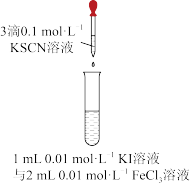 现象为溶液变红 | 证明化学反应存在一定的限度 |
| C | 相同条件下,在两支试管中各加入3mL6%的H2O2溶液,再向H2O2溶液中分别滴入1mLH2O和1mLFeCl3溶液,观察并比较H2O2的分解速率 | 探究催化剂对H2O2分解速率的影响 |
| D | 向2mL甲苯中加入3滴酸性KMnO4溶液,振荡,紫色褪去;向2mL苯中加入3滴酸性KMnO4溶液,振荡,紫色没有褪去 | 证明与苯环相连的甲基易被氧化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



