名校
1 . 化学与生活、生产、社会息息相关。下列说法错误的是
| A.冬天应将面团置于温热处发酵 |
| B.蔗糖溶于水是熵减小的过程 |
| C.工业生产中,适当增大廉价的反应物的浓度有利于降低生产成本 |
| D.“冰,水为之,而寒于水”说明等质量的水和冰相比,冰的能量更低 |
您最近一年使用:0次
2023-10-15更新
|
352次组卷
|
7卷引用:四川省内江市2023-2024学年第一中学高二上学期化学试卷
名校
2 . 一氧化二氮可以用作火箭氧化剂,在室温下稳定,易于储存和飞行使用。现利用汽车尾气中的 与
与 反应来制备
反应来制备 气体,回答下列问题。
气体,回答下列问题。
(1)已知: 的燃烧热为
的燃烧热为
①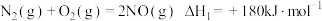
②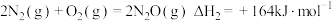
③
反应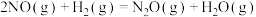 的
的
___________  。
。
(2)总反应分为两步进行;
第①步: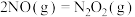
第②步:___________ 。
实验发现,第①步反应几乎不影响总反应到达平衡所用的时间,由此推断,下列关于该反应叙述正确的是___________ 。(填序号)
A.更换催化剂,可改变反应的 B.步骤①的逆反应活化能一定小于②的
B.步骤①的逆反应活化能一定小于②的
C.步骤②的有效碰撞频率小于步骤① D.反应进程中 属于中间产物
属于中间产物
(3)工业上也可用 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入 与
与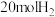 ,容器体积为2L,在催化剂作用下发生反应:
,容器体积为2L,在催化剂作用下发生反应: 。
。 的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
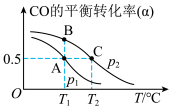
①压强为
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②在起始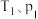 条件下,2L恒容容器中,反应的平衡常数
条件下,2L恒容容器中,反应的平衡常数
___________  。
。
(4)煤化工通常研究不同条件下CO的转化率以解决实际问题。已知在催化剂存在条件下发生反应: 中
中 的平衡转化率随投料比
的平衡转化率随投料比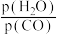 及温度变化关系如图所示:
及温度变化关系如图所示:
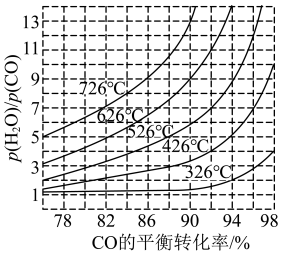
①该反应是___________ 反应(填“吸热”或“放热”);
②在以铁镁为催化剂的工业中,一般控制温度为 左右、投料比2)=3~5,采用此条件的原因可能是
左右、投料比2)=3~5,采用此条件的原因可能是___________ 。
 与
与 反应来制备
反应来制备 气体,回答下列问题。
气体,回答下列问题。(1)已知:
 的燃烧热为
的燃烧热为
①
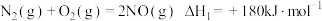
②
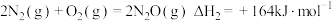
③

反应
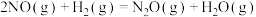 的
的
 。
。(2)总反应分为两步进行;
第①步:
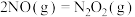
第②步:
实验发现,第①步反应几乎不影响总反应到达平衡所用的时间,由此推断,下列关于该反应叙述正确的是
A.更换催化剂,可改变反应的
 B.步骤①的逆反应活化能一定小于②的
B.步骤①的逆反应活化能一定小于②的C.步骤②的有效碰撞频率小于步骤① D.反应进程中
 属于中间产物
属于中间产物(3)工业上也可用
 生产甲醇。在一容积可变的密闭容器中充入
生产甲醇。在一容积可变的密闭容器中充入 与
与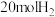 ,容器体积为2L,在催化剂作用下发生反应:
,容器体积为2L,在催化剂作用下发生反应: 。
。 的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
的平衡转化率(a)与温度(T)、压强(p)的关系如图所示。
①压强为

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②在起始
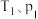 条件下,2L恒容容器中,反应的平衡常数
条件下,2L恒容容器中,反应的平衡常数
 。
。(4)煤化工通常研究不同条件下CO的转化率以解决实际问题。已知在催化剂存在条件下发生反应:
 中
中 的平衡转化率随投料比
的平衡转化率随投料比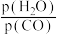 及温度变化关系如图所示:
及温度变化关系如图所示:
①该反应是
②在以铁镁为催化剂的工业中,一般控制温度为
 左右、投料比2)=3~5,采用此条件的原因可能是
左右、投料比2)=3~5,采用此条件的原因可能是
您最近一年使用:0次
3 . 下列实验设计及现象、结论合理的是
| 选项 | 实验目的 | 实验设计及现象 | 结论 |
| A | 探究 是否具有还原性 是否具有还原性 | 向一定浓度的 溶液中滴加少量酸性高锰酸钾溶液,高锰酸钾溶液紫红色褪去 溶液中滴加少量酸性高锰酸钾溶液,高锰酸钾溶液紫红色褪去 |  具有还原性 具有还原性 |
| B | 检验 气体中是否混有 气体中是否混有 | 将气体依次通过饱和 溶液和澄清石灰水,澄清石灰水变浑浊 溶液和澄清石灰水,澄清石灰水变浑浊 |  气体中混有 气体中混有 |
| C | 在 与 与 的混合液中再加入 的混合液中再加入 固体 固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 探究不同催化剂的催化效率 | 两支试管中分别盛相同温度、相同浓度、相同体积的 溶液,分别滴加相同浓度、相同体积的 溶液,分别滴加相同浓度、相同体积的 溶液与 溶液与 溶液,滴加 溶液,滴加 溶液得试管中产生气体更快 溶液得试管中产生气体更快 |  对 对 分解的催化效率更高 分解的催化效率更高 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . Ⅰ.教材采用图实验装置测定锌与稀硫酸反应的速率。

(1)检查图1装置气密性的操作方法是___________ 。
(2)分别取2 g颗粒大小相同的锌粒分别与体积均为40 mL的1 mol/L硫酸、4 mol/L硫酸反应,收集20 mL 时所需时间前者比后者
时所需时间前者比后者___________ (填“长”或“短”)。
(3)同学们在实验操作中发现,本实验设计存在明显不足,例如(举一例)___________ 。
(4)某化学兴趣小组对教材实验装置进行如图所示改进,检查装置气密性后进行的实验操作有:

a.在多孔塑料袋中装入锌粒;
b.在锥形瓶中加入40 mL 1 mol/L硫酸;
c.塞好橡胶塞,___________ (填操作)时,立即用秒表计时;
d.注射器内每增加10 mL气体时读取一次秒表。
(5)实验观察到锌与稀硫酸反应初期速率逐渐加快,其原因是___________ ,反应进行一定时间后速率逐渐减慢,原因是___________ 。
(6)测得产生 的体积与反应时间的关系曲线如下图所示,
的体积与反应时间的关系曲线如下图所示, 时间段氢气体积略有减小的原因是
时间段氢气体积略有减小的原因是___________ ;在64s内用 浓度表示的平均反应速率
浓度表示的平均反应速率
___________ (此时,溶液体积仍为40 mL,气体摩尔体积为25 L/mol)。

Ⅱ.一种新型催化剂能使NO和CO发生反应: 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
(7)表中
___________ 。
(8)能验证温度对化学反应速率影响规律的是实验___________ (填实验编号)。
(9)实验①和实验②中,NO的物质的量浓度 随时间t的变化曲线如图所示,其中表示实验②的是曲线
随时间t的变化曲线如图所示,其中表示实验②的是曲线___________ (填“甲”或“乙”)。


(1)检查图1装置气密性的操作方法是
(2)分别取2 g颗粒大小相同的锌粒分别与体积均为40 mL的1 mol/L硫酸、4 mol/L硫酸反应,收集20 mL
 时所需时间前者比后者
时所需时间前者比后者(3)同学们在实验操作中发现,本实验设计存在明显不足,例如(举一例)
(4)某化学兴趣小组对教材实验装置进行如图所示改进,检查装置气密性后进行的实验操作有:

a.在多孔塑料袋中装入锌粒;
b.在锥形瓶中加入40 mL 1 mol/L硫酸;
c.塞好橡胶塞,
d.注射器内每增加10 mL气体时读取一次秒表。
(5)实验观察到锌与稀硫酸反应初期速率逐渐加快,其原因是
(6)测得产生
 的体积与反应时间的关系曲线如下图所示,
的体积与反应时间的关系曲线如下图所示, 时间段氢气体积略有减小的原因是
时间段氢气体积略有减小的原因是 浓度表示的平均反应速率
浓度表示的平均反应速率

Ⅱ.一种新型催化剂能使NO和CO发生反应:
 。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。
。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如表所示。实验编号 | T/℃ | NO初始浓度(mol⋅L-1) | CO初始浓度(mol⋅L-1) | 催化剂的比表面积(m2⋅g-1) |
① | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
② | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
③ | 350 | a | 5.80×10-3 | 82 |
(7)表中

(8)能验证温度对化学反应速率影响规律的是实验
(9)实验①和实验②中,NO的物质的量浓度
 随时间t的变化曲线如图所示,其中表示实验②的是曲线
随时间t的变化曲线如图所示,其中表示实验②的是曲线
您最近一年使用:0次
2023-10-12更新
|
190次组卷
|
2卷引用:四川省成都外国语学校2023-2024学年高二上学期10月月考化学试题
5 . 炼油、石化等工业会产生含硫(-2价)废水,可通过催化氧化法进行处理,碱性条件下,催化氧化废水的机理如图所示。其中MnO2为催化剂,附着在催化剂载体聚苯胺的表面。下列说法错误的是
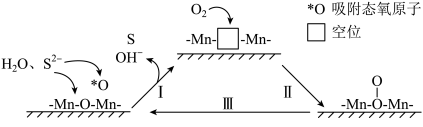
| A.转化I中Mn的化合价未发生变化 |
| B.催化氧化过程中有共价键的断裂 |
C.催化氧化过程的总反应为:O2+2H2O+2S2- 4OH-+2S 4OH-+2S |
| D.催化剂使用一段时间后催化效率会下降,原因是生成的S覆盖在催化剂表面或进入催化剂内空位处 |
您最近一年使用:0次
2023-10-10更新
|
405次组卷
|
3卷引用:四川省成都市树德中学2023-2024学年高三上学期10月阶段性测试理科综合化学试题
名校
解题方法
6 . 羰基硫(COS)是以煤、石油、天然气为原料生产的化工原料气中有机硫的主要形式。COS催化水解的反应为: ,在相同恒温恒容容器、相同投料比、相同时间内,测得不同温度及不同催化剂下
,在相同恒温恒容容器、相同投料比、相同时间内,测得不同温度及不同催化剂下 水解反应的转化率如图所示。下列说法正确的是
水解反应的转化率如图所示。下列说法正确的是

 ,在相同恒温恒容容器、相同投料比、相同时间内,测得不同温度及不同催化剂下
,在相同恒温恒容容器、相同投料比、相同时间内,测得不同温度及不同催化剂下 水解反应的转化率如图所示。下列说法正确的是
水解反应的转化率如图所示。下列说法正确的是
A.以 浓度表示的该段时间内平均反应速率: 浓度表示的该段时间内平均反应速率: |
B.线段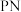 上的点均是平衡点, 上的点均是平衡点, 点较 点较 点 点 转化率降低的原因是平衡移动 转化率降低的原因是平衡移动 |
C.任何温度下, 的催化效果都比 的催化效果都比 好 好 |
D. 时,相较于 时,相较于 ,使用 ,使用 做催化剂,达平衡时 做催化剂,达平衡时 的体积分数更大 的体积分数更大 |
您最近一年使用:0次
2023-10-10更新
|
308次组卷
|
3卷引用:四川省成都市第七中学2023-2024学年高二上学期10月月考化学试题
名校
7 . 甲烷单加氧酶(s-mmo)含有双核铁活性中心,是 氧化
氧化 生成
生成 的催化剂,反应过程如图所示。下列说法不正确的是
的催化剂,反应过程如图所示。下列说法不正确的是

 氧化
氧化 生成
生成 的催化剂,反应过程如图所示。下列说法不正确的是
的催化剂,反应过程如图所示。下列说法不正确的是
| A.每一步骤都存在铁元素和氧元素之间的电子转移 |
| B.步骤③中有非极性键的断裂和极性键的生成 |
| C.该催化循环过程中,s-mmo的双核铁活性中心先被氧化后被还原 |
D.图中的总过程可表示为: |
您最近一年使用:0次
2023-10-10更新
|
175次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
8 . 某反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是
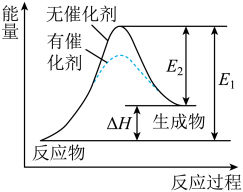

| A.该反应为放热反应 |
| B.催化剂能同时改变该反应的活化能和焓变 |
| C.使用催化剂能同时提高正逆反应速率 |
| D.该反应的ΔH=E2-E1 |
您最近一年使用:0次
2023-10-09更新
|
288次组卷
|
5卷引用:四川省绵阳南山中学2023-2024学年高二上学期10月月考化学试题
名校
9 . 反应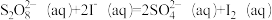 在加入Fe3+后反应进程中的能量变化如图,已知反应机理中有Fe2+出现。下列有关该反应的说法正确的是
在加入Fe3+后反应进程中的能量变化如图,已知反应机理中有Fe2+出现。下列有关该反应的说法正确的是
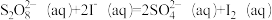 在加入Fe3+后反应进程中的能量变化如图,已知反应机理中有Fe2+出现。下列有关该反应的说法正确的是
在加入Fe3+后反应进程中的能量变化如图,已知反应机理中有Fe2+出现。下列有关该反应的说法正确的是
A.步骤①的热化学方程为: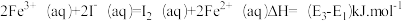 |
| B.决速步是第②步 |
| C.升高温度可以更容易检测到Fe2+ |
| D.无Fe3+时,反应的活化能小于E3-E2,但是△H相同 |
您最近一年使用:0次
2023-10-08更新
|
759次组卷
|
6卷引用:四川省德阳市德阳外国语学校2023-2024学年高二上学期1月月考化学试题
四川省德阳市德阳外国语学校2023-2024学年高二上学期1月月考化学试题浙江省浙南名校联盟2023-2024学年高三上学期第一次联考化学试题浙江省杭州市浙江大学附属中学2023-2024学年高二上学期期末考试化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
名校
解题方法
10 . 实验室利用下列方案探究影响化学反应速率的因素,实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定 溶液褪色时间来判断反应的快慢。请回答相关问题:
溶液褪色时间来判断反应的快慢。请回答相关问题:
(1)该反应的离子方程式为___________ 。
(2)实验①、②、③所加 溶液均要过量,理由是
溶液均要过量,理由是___________ 。
(3)实验①和实验②是探究___________ 对化学反应速率的影响。
(4)实验②测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=___________ 。
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是___________ 。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的___________ (填字母)。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定 溶液褪色时间来判断反应的快慢。请回答相关问题:
溶液褪色时间来判断反应的快慢。请回答相关问题:| 编号 | 温度/℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度/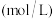 | 体积/ | 浓度/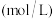 | 体积/ | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
(2)实验①、②、③所加
 溶液均要过量,理由是
溶液均要过量,理由是(3)实验①和实验②是探究
(4)实验②测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=
(5)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
您最近一年使用:0次
2023-10-07更新
|
29次组卷
|
2卷引用:四川省绵阳南山中学实验学校2023-2024学年高二上学期9月月考化学试题



