名校
1 . 已知0.1 mol·L-1 FeCl3溶液与0.01 mol·L-1 KSCN溶液等体积混合,发生如下反应:FeCl3+3KSCN Fe(SCN)3+3KCl,改变下列条件,能使溶液颜色变浅的是
Fe(SCN)3+3KCl,改变下列条件,能使溶液颜色变浅的是
 Fe(SCN)3+3KCl,改变下列条件,能使溶液颜色变浅的是
Fe(SCN)3+3KCl,改变下列条件,能使溶液颜色变浅的是| A.向溶液中加入少量KCl晶体 | B.向溶液中加入一定量KCl溶液 |
| C.向溶液中加入少量AgNO3固体 | D.向溶液中滴加几滴1 mol·L-1 FeCl3溶液 |
您最近一年使用:0次
2018-12-06更新
|
128次组卷
|
4卷引用:【省级联考】内蒙古自治区2018-2019学年高二上学期期中考试理科综合化学试题
【省级联考】内蒙古自治区2018-2019学年高二上学期期中考试理科综合化学试题江西省景德镇一中2017-2018学年高二上学期期末考化学试题江西省抚州市南城县第二中学2019-2020学年高一下学期开学考试(自强班)化学试题(已下线)6.2.2 化学平衡(第2课时 化学平衡移动)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
名校
解题方法
2 . 在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:
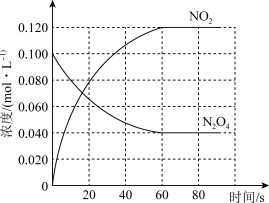
(1)反应的ΔH________ (填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如下图所示。在0~60 s时段,反应速率v(N2O4)为________ mol·L-1·s-1。
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a.T________ (填“大于”或“小于”)100 ℃,判断理由是________________________________ 。
b.温度T时反应的平衡常数K2=____________________ 。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________ (填“正反应”或“逆反应”)方向移动,判断理由是________________________________ 。
 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH
(2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。
a.T
b.温度T时反应的平衡常数K2=
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向

您最近一年使用:0次
名校
3 . 下列事实能用勒夏特列原理解释的是( )
| A.加入催化剂有利于合成氨的反应 |
| B.由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深 |
| C.500 ℃时比室温更有利于合成氨的反应 |
| D.将混合气体中的氨液化有利于合成氨反应 |
您最近一年使用:0次
2018-12-06更新
|
558次组卷
|
9卷引用:【全国百强校】内蒙古巴彦淖尔一中2018-2019学年高二上学期期中考试化学试题
【全国百强校】内蒙古巴彦淖尔一中2018-2019学年高二上学期期中考试化学试题【全国百强校】四川省雅安市雅安中学2018-2019学年高二上学期期中考试化学试题广东省揭阳市惠来县第一中学2018-2019学年高二上学期期中考试化学试题河南省周口中英文学校2019-2020学年高二上学期期中考试化学试题云南省弥勒市第一中学2021-2022学年高二上学期第二次月考化学试题河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题江苏省郑梁梅高级中学2022-2023学年高二上学期第一次月考化学试题(已下线)2.2.1 化学平衡状态——同步学习必备知识河北省滦州市第二中学2023-2024学年高二上学期期中考试 化学试题
4 . Ⅰ.工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g) CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将
CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将________ (填“变大”、“变小”或“不变”,下同),混合气体的平均相对分子质量将_____________________ 。
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g) 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。
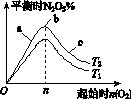
(1)图象中T1和T2的关系是T1________ T2(填“>”、“<”或“=”)。
(2)比较a、b、c三点所处的平衡状态中,反应物NO2的转化率最大的是________ (填字母)。
 CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将
CH3OCH3(g)+3H2O(g)ΔH<0。温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)
 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。
(1)图象中T1和T2的关系是T1
(2)比较a、b、c三点所处的平衡状态中,反应物NO2的转化率最大的是
您最近一年使用:0次
名校
5 . 已知次氯酸是比碳酸还弱的酸,氯水中存在平衡Cl2+H2O⇌HCl+HClO, HClO⇌H++ClO-。达平衡后,要使HClO浓度增大,可加入适量( )
| A.H2S | B.Na2CO3 | C.盐酸 | D.NaOH |
您最近一年使用:0次
名校
6 . 勒夏特列原理是自然界一条重要的基本原理,下列事实能用勒夏特列原理解释的是
| A.NO2气体受压缩后,颜色先变深后变浅 |
B.对2HI(g)  H2(g)+I2(g)平衡体系加压,颜色迅速变深 H2(g)+I2(g)平衡体系加压,颜色迅速变深 |
| C.合成氨工业采用高温、高压工艺提高氨的产率 |
| D.配制硫酸亚铁溶液时,常加入少量铁屑以防止氧化 |
您最近一年使用:0次
2018-10-23更新
|
507次组卷
|
7卷引用:【省级联考】内蒙古自治区2018-2019学年高二上学期期中考试理科综合化学试题
名校
7 . 下列说法正确的是
A.对于A(s)+B(g)  C(g)+D(g)的反应,加入A,反应速率加快 C(g)+D(g)的反应,加入A,反应速率加快 |
B.2NO2 N2O4(正反应放热),升高温度,v(正)增大,v(逆)减小 N2O4(正反应放热),升高温度,v(正)增大,v(逆)减小 |
C.一定温度下,反应 N2(g)+3H2(g)  2NH3(g)在密闭容器中进行,恒压,充入He不改变化学反应速率 2NH3(g)在密闭容器中进行,恒压,充入He不改变化学反应速率 |
| D.100 mL2 mol·L—1稀盐酸与锌反应时,加入少量硫酸铜固体,生成氢气的速率加快 |
您最近一年使用:0次
2018-08-19更新
|
1412次组卷
|
11卷引用:内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题
内蒙古赤峰二中2019-2020学年高一下学期第二次月考(6月)化学试题湖南省醴陵市第一中学2017-2018学年高一下学期期末考试化学试题广西壮族自治区贺州市平桂区平桂高级中学2019届高三摸底考试化学试题【区级联考】天津市武清区2018-2019学年高二上学期期中质量调查化学试题河北省唐山市海港高级中学2019-2020学年高一下学期第五次校考化学试题河北省衡水市第十三中学2019-2020学年高一下学期调研考试化学试题天津市第一中学2020-2021学年高一下学期期中考试化学试题浙江省桐庐分水高级中学2020-2021学年高一下学期第一次月考化学试题天津市武清区梅厂中学2021-2022学年高二上学期阶段性练习化学试题天津市部分重点校2022~2023学年高一下学期期中联考化学试题天津市和平区第五十五中学2022-2023学年高一下学期期中化学试试题
名校
解题方法
8 . Ⅰ.现有反应aA(g)+bB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是________ 热反应,且a+b________ p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________ (填“增大”“减小”或“不变”,下同),正反应速率________ 。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比c(B)/c(C) 将________ 。
(5)若加入催化剂,平衡时气体混合物的总物质的量________ 。
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色________ ,而维持容器内气体的压强不变,充入氖气时,混合物的颜色________ 。(填“变浅”“变深”或“不变”)
Ⅱ.二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。

(1)该条件下反应平衡常数表达式K=___________________________ ;在t1 ℃时,反应的平衡常数为___________ 。
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为:c(CH3OH)=0.4 mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4mol·L-1,此时正、逆反应速率的大小:v正________ v逆(填“>”、“<”或“=”),反应向______ 反应方向进行(填“正”或“逆”)。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比c(B)/c(C) 将
(5)若加入催化剂,平衡时气体混合物的总物质的量
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色
Ⅱ.二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
CH3OCH3(g)+H2O(g) ΔH=-23.5kJ·mol-1。在t1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
(1)该条件下反应平衡常数表达式K=
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为:c(CH3OH)=0.4 mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4mol·L-1,此时正、逆反应速率的大小:v正
您最近一年使用:0次
9 . 下列有关工业生产的叙述中,正确的是
| A.硫酸生产中常采用催化剂提高SO2的转化率 |
| B.合成氨中采用及时分离氨气提高反应速率 |
| C.电镀铜时,溶液中c(Cu2+)基本保持不变 |
| D.用电解熔融氧化镁的方法制取镁 |
您最近一年使用:0次
名校
10 . 红矾钠(Na2Cr2O7·2H2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO·Cr2O3)制备红矾钠的过程中会发生如下反应:4FeO(s)+4Cr2O3(s)+8Na2CO3(s)+7O2(g)  8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
(1)请写出上述反应的化学平衡常数表达式:K=__________________ 。
(2)图1、图2表示上述反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线。由图1判断,反应进行至t2时,曲线发生变化的原因是___________________ (用文字表达);由图2判断,t2到t3的曲线变化的原因可能是________ (填写序号)。
a.升高温度 b.加催化剂 c.通入O2 d.缩小容器体积

(3)工业上可用上述反应中的副产物CO2来生产甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①已知该反应能自发进行,则下列图象正确的是___________ 。
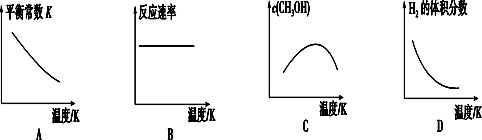
②在T1温度时,将1 mol CO2和3 mol H2充入一密闭容器中,反应达到平衡后,CO2转化率为α,则容器内平衡时的压强与起始压强之比为________ 。
 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g) ΔH<0(1)请写出上述反应的化学平衡常数表达式:K=
(2)图1、图2表示上述反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线。由图1判断,反应进行至t2时,曲线发生变化的原因是
a.升高温度 b.加催化剂 c.通入O2 d.缩小容器体积

(3)工业上可用上述反应中的副产物CO2来生产甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。①已知该反应能自发进行,则下列图象正确的是

②在T1温度时,将1 mol CO2和3 mol H2充入一密闭容器中,反应达到平衡后,CO2转化率为α,则容器内平衡时的压强与起始压强之比为
您最近一年使用:0次



