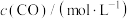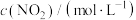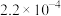2024高三下·全国·专题练习
解题方法
1 . 1200K时,假定体系内只有反应C40H12 (g) C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 2NO(g)+O2(g) 2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO(g) N2O2(g) E1=82kJ/mol v=k1c2(NO)
N2O2(g) E1=82kJ/mol v=k1c2(NO)
N2O2(g)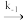 2NO(g) E-1=205kJ/mol v=k-1c(N2O2)
2NO(g) E-1=205kJ/mol v=k-1c(N2O2)
N2O2(g)+O2(g) 2NO2(g) E2=82kJ/mol v=k2c(N2O2)·c(O2)
2NO2(g) E2=82kJ/mol v=k2c(N2O2)·c(O2)
2NO2(g)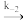 N2O2(g)+O2(g) E-2=72kJ/mol v=k-2c2(NO2)
N2O2(g)+O2(g) E-2=72kJ/mol v=k-2c2(NO2)
则2NO(g) N2O2(g) △H1=
N2O2(g) △H1=______ kJ·mol-1,其平衡常数K与上述速率常数k1、k-1的关系式为K=______ 。2NO(g)+O2(g) 2NO2(g) △H=
2NO2(g) △H=______ kJ·mol-1.
 2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):2NO(g)
 N2O2(g) E1=82kJ/mol v=k1c2(NO)
N2O2(g) E1=82kJ/mol v=k1c2(NO)N2O2(g)
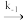 2NO(g) E-1=205kJ/mol v=k-1c(N2O2)
2NO(g) E-1=205kJ/mol v=k-1c(N2O2)N2O2(g)+O2(g)
 2NO2(g) E2=82kJ/mol v=k2c(N2O2)·c(O2)
2NO2(g) E2=82kJ/mol v=k2c(N2O2)·c(O2)2NO2(g)
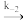 N2O2(g)+O2(g) E-2=72kJ/mol v=k-2c2(NO2)
N2O2(g)+O2(g) E-2=72kJ/mol v=k-2c2(NO2)则2NO(g)
 N2O2(g) △H1=
N2O2(g) △H1= 2NO2(g) △H=
2NO2(g) △H=
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 对于基元反应,如aA+bB cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
反应Ⅰ:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
反应Ⅱ:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g) 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
(1)ΔH4=______ kJ·mol-1
(2)计算653K时的平衡常数K=______ 。
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为______ mol·L-1·s-1
 cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:反应Ⅰ:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1反应Ⅱ:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g)
 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1(1)ΔH4=
(2)计算653K时的平衡常数K=
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
4 . 升高温度绝大多数的化学反应速率增大,但是2NO(g)+O2(g) 2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
i:2NO(g) N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
ii:N2O2(g)+O2(g) 2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=______ 。
 2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g)
2NO2(g)的速率却随温度的升高而减小,某化学小组为研究特殊现象的实质原因,查阅资料知:2NO(g)+O2(g) 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:i:2NO(g)
 N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0
N2O2(g)(快),v1正=k1正·c2(NO) v1逆=k1逆·c(N2O2) ΔH1<0ii:N2O2(g)+O2(g)
 2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0
2NO2(g)(慢),v2正=k2正·c(N2O2)·c(O2) v2逆=k2逆·c2(NO2) ΔH2<0一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出用k1正、k1逆、k2正、k2逆表示的平衡常数表达式K=
您最近一年使用:0次
2024高三下·全国·专题练习
5 . 填空
(1)一步完成的反应称为基元反应,只由基元反应构成的化学反应称为简单反应,两个及以上基元反应构成的化学反应称为复杂反应,复杂反应的速率取决(等)于慢的基元反应速率。基元反应aA+bB=cC+dD的速率方程为v=k·ca(A)·cb(B),其中k为速率常数。已知反应NO2+CO=NO+CO2,在不同温度下反应机理不同。
①温度高于490K时,上述反应为简单反应,请写出其速率方程______ 。
②温度高于520K时,该反应是由两个基元反应构成的复杂反应,其速率方程v=k·c2(NO2),已知慢的基元反应的反应物和产物为NO、NO2、NO3,用方程式表示反应历程。
第一步:______ (慢反应)。
第二步:______ (快反应)。
(2)N2O4(g) 2NO2(g) ΔH=+57kJ·mol-1该反应是高中和大学化学学习的经典素材。
2NO2(g) ΔH=+57kJ·mol-1该反应是高中和大学化学学习的经典素材。
②T1K时,向1L真空容器中加入1molN2O4,达到平衡时NO2的平衡产率为20%,则该温度下的平衡常数K=______ ,达到平衡时吸收的热量为______ kJ。某温度下,该反应达到平衡,NO2与N2O4的混合气体总压强为100KPa,密度为同状态下氢气密度的34.5倍,平衡常数KP=______ KPa(用平衡分压代替平衡浓度计算)。
③若v(N2O4)=k1·c(N2O4)v(NO2)=k2·c(NO2),T2温度下,若k1=k2,则T2______ T1(填“高于”或“低于”)。
(3)复杂反应2NO(g)+O2(g)=2NO2(g)由两个基元反应构成,2NO(g)=N2O2(g)(快速平衡)N2O2(g)+O2(g)=2NO2(g)(慢反应),已知快反应为放热反应,其正、逆反应速率常数分别为k1和k2,慢反应正、逆反应速率常数分别为k3和k4。若v正=k·c2(NO)·c(O2)则k=______ (用k1、k2、k3表示);
(1)一步完成的反应称为基元反应,只由基元反应构成的化学反应称为简单反应,两个及以上基元反应构成的化学反应称为复杂反应,复杂反应的速率取决(等)于慢的基元反应速率。基元反应aA+bB=cC+dD的速率方程为v=k·ca(A)·cb(B),其中k为速率常数。已知反应NO2+CO=NO+CO2,在不同温度下反应机理不同。
①温度高于490K时,上述反应为简单反应,请写出其速率方程
②温度高于520K时,该反应是由两个基元反应构成的复杂反应,其速率方程v=k·c2(NO2),已知慢的基元反应的反应物和产物为NO、NO2、NO3,用方程式表示反应历程。
第一步:
第二步:
(2)N2O4(g)
 2NO2(g) ΔH=+57kJ·mol-1该反应是高中和大学化学学习的经典素材。
2NO2(g) ΔH=+57kJ·mol-1该反应是高中和大学化学学习的经典素材。②T1K时,向1L真空容器中加入1molN2O4,达到平衡时NO2的平衡产率为20%,则该温度下的平衡常数K=
③若v(N2O4)=k1·c(N2O4)v(NO2)=k2·c(NO2),T2温度下,若k1=k2,则T2
(3)复杂反应2NO(g)+O2(g)=2NO2(g)由两个基元反应构成,2NO(g)=N2O2(g)(快速平衡)N2O2(g)+O2(g)=2NO2(g)(慢反应),已知快反应为放热反应,其正、逆反应速率常数分别为k1和k2,慢反应正、逆反应速率常数分别为k3和k4。若v正=k·c2(NO)·c(O2)则k=
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
6 . 工业上,可以采用 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:
① (主反应);
(主反应);
② (主反应);
(主反应);
③ (副反应)。
(副反应)。
一定温度下,向总压强恒定为100kPa的反应器中充入 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成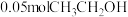 ,则反应①的平衡常数
,则反应①的平衡常数 为
为___________ 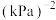 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:①
 (主反应);
(主反应);②
 (主反应);
(主反应);③
 (副反应)。
(副反应)。一定温度下,向总压强恒定为100kPa的反应器中充入
 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成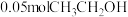 ,则反应①的平衡常数
,则反应①的平衡常数 为
为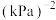 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
7 . 在一定条件下 、
、 主要发生以下反应:
主要发生以下反应:
①
 kJ⋅mol-1
kJ⋅mol-1
②
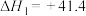 kJ⋅mol-1
kJ⋅mol-1
若在一定温度下,投料比例相同(充入物质的量之比为1∶4的 和
和 ),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为
),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为 ,平衡时
,平衡时 压强为
压强为 ,甲烷压强为
,甲烷压强为 。则甲烷的选择性为
。则甲烷的选择性为________ (用 、
、 、
、 中相关字母表示,下同),反应②的压强平衡常数
中相关字母表示,下同),反应②的压强平衡常数 的值为
的值为_______ 。
 、
、 主要发生以下反应:
主要发生以下反应:①

 kJ⋅mol-1
kJ⋅mol-1②

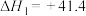 kJ⋅mol-1
kJ⋅mol-1若在一定温度下,投料比例相同(充入物质的量之比为1∶4的
 和
和 ),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为
),通入恒容密闭容器中,发生上述反应达到平衡,测得反应前容器内压强为 ,平衡时
,平衡时 压强为
压强为 ,甲烷压强为
,甲烷压强为 。则甲烷的选择性为
。则甲烷的选择性为 、
、 、
、 中相关字母表示,下同),反应②的压强平衡常数
中相关字母表示,下同),反应②的压强平衡常数 的值为
的值为
您最近一年使用:0次
名校
解题方法
8 . 达成“双碳”目标的重要途径是实现碳的固定。利用CO、 和
和 可以合成生物质能源甲醇:
可以合成生物质能源甲醇:
反应1:
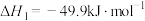
反应2:

反应3:
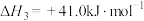
回答下列问题:
(1)反应1在___________ (填“较高温度”“较低温度”或“任何温度”)下能自发进行。
(2)
___________  。
。
(3)T℃时,向一恒容密闭容器中仅充入1molCO(g)和 ,仅发生反应2。下列叙述错误的是___________(填标号)。
,仅发生反应2。下列叙述错误的是___________(填标号)。
(4)在某催化剂作用下,反应2的历程如图所示(图中数据表示微粒的相对能量,*表示吸附在催化剂表面上)。___________ 。
(5)在某催化剂作用下,只发生反应: 。该反应的速率方程式为
。该反应的速率方程式为 ,
,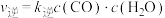 (k为速率常数,只与温度、催化剂有关)。830℃时该反应的平衡常数K=1,达到平衡后,
(k为速率常数,只与温度、催化剂有关)。830℃时该反应的平衡常数K=1,达到平衡后,
________ (填“>”“<”或“=”,下同) ,900℃时
,900℃时
________  。
。
(6) 时,在密闭容器甲、乙中,分别充入
时,在密闭容器甲、乙中,分别充入 和
和 ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1.测得
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1.测得 平衡转化率与压强关系如图所示。
平衡转化率与压强关系如图所示。___________ (填“甲”或“乙”)。
②平衡常数
___________ (填“>”“<”或“=”) ,M点
,M点
___________ kPa。
(7) 时,向一体积为1L的恒容密闭容器中充入1molCO、
时,向一体积为1L的恒容密闭容器中充入1molCO、 和
和 ,在一定条件下发生上述3个反应,达到平衡时得到
,在一定条件下发生上述3个反应,达到平衡时得到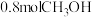 和
和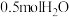 ,此时
,此时 平衡转化率为50%。该温度下,反应1的平衡常数K=
平衡转化率为50%。该温度下,反应1的平衡常数K=___________  。(列出计算式)
。(列出计算式)
 和
和 可以合成生物质能源甲醇:
可以合成生物质能源甲醇:反应1:

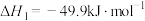
反应2:


反应3:

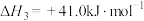
回答下列问题:
(1)反应1在
(2)

 。
。(3)T℃时,向一恒容密闭容器中仅充入1molCO(g)和
 ,仅发生反应2。下列叙述错误的是___________(填标号)。
,仅发生反应2。下列叙述错误的是___________(填标号)。| A.加入催化剂,反应速率增大 |
| B.CO体积分数不变时,反应达到平衡状态 |
| C.平衡后,充入氩气,平衡正向移动 |
D.平衡后,充入 ,CO平衡转化率增大 ,CO平衡转化率增大 |
(4)在某催化剂作用下,反应2的历程如图所示(图中数据表示微粒的相对能量,*表示吸附在催化剂表面上)。
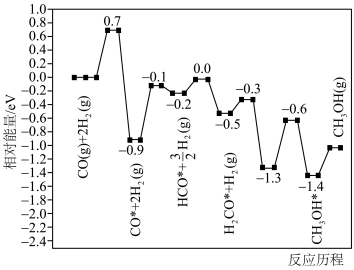
(5)在某催化剂作用下,只发生反应:
 。该反应的速率方程式为
。该反应的速率方程式为 ,
,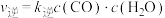 (k为速率常数,只与温度、催化剂有关)。830℃时该反应的平衡常数K=1,达到平衡后,
(k为速率常数,只与温度、催化剂有关)。830℃时该反应的平衡常数K=1,达到平衡后,
 ,900℃时
,900℃时
 。
。(6)
 时,在密闭容器甲、乙中,分别充入
时,在密闭容器甲、乙中,分别充入 和
和 ,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1.测得
,它们分别在有水分子筛(只允许水分子透过)和无水分子筛条件下仅发生反应1.测得 平衡转化率与压强关系如图所示。
平衡转化率与压强关系如图所示。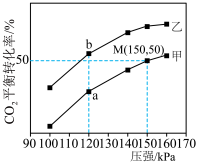
②平衡常数

 ,M点
,M点
(7)
 时,向一体积为1L的恒容密闭容器中充入1molCO、
时,向一体积为1L的恒容密闭容器中充入1molCO、 和
和 ,在一定条件下发生上述3个反应,达到平衡时得到
,在一定条件下发生上述3个反应,达到平衡时得到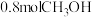 和
和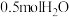 ,此时
,此时 平衡转化率为50%。该温度下,反应1的平衡常数K=
平衡转化率为50%。该温度下,反应1的平衡常数K= 。(列出计算式)
。(列出计算式)
您最近一年使用:0次
2024-02-25更新
|
752次组卷
|
6卷引用:2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学
2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学甘肃省白银市名校2023-2024学年高三下学期联合调研化学试题甘肃省天水市麦积区2024届高三下学期2月第二次模拟检测化学试题湖南省衡阳市第八中学2024届高三下学期高考模拟预测化学试题
解题方法
9 . Ⅰ、 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
(1) 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:
反应的
___________ 
(2)将原料按初始组成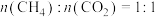 充入密闭容器中,保持体系压强为
充入密闭容器中,保持体系压强为 发生反应。达到平衡时,
发生反应。达到平衡时, 体积分数与温度的关系如图所示:
体积分数与温度的关系如图所示: 的体积分数,则
的体积分数,则___________ 点对应的平衡常数最小,理由是___________
(3)在恒温恒容装置中通入等体积 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为___________ 。该反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,分压 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。
(4)其他条件相同,在不同催化剂(A、B)作用下, 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: 、
、 表示,则
表示,则
___________  (填“>”“<”或“=”下同)。
(填“>”“<”或“=”下同)。
②y点对应的
___________ z点对应的 。
。
Ⅱ.运用电化学原理可以很好利用 资源。
资源。
(5)火星大气由 的二氧化碳气体组成,火星探测器采用
的二氧化碳气体组成,火星探测器采用 电池供电,其反应机理如下图:
电池供电,其反应机理如下图: 电极反应式:
电极反应式:___________ 。
 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:(1)
 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知
 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:| 物质 |  |  |  |
燃烧热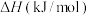 |  |  |  |


(2)将原料按初始组成
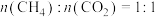 充入密闭容器中,保持体系压强为
充入密闭容器中,保持体系压强为 发生反应。达到平衡时,
发生反应。达到平衡时, 体积分数与温度的关系如图所示:
体积分数与温度的关系如图所示: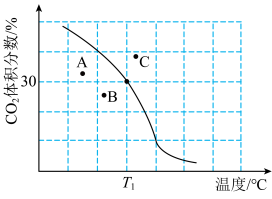
 的体积分数,则
的体积分数,则(3)在恒温恒容装置中通入等体积
 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为
 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。(4)其他条件相同,在不同催化剂(A、B)作用下,
 的产率随反应温度的变化如图所示:
的产率随反应温度的变化如图所示: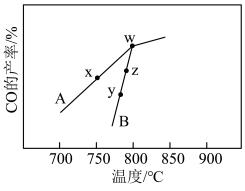
 、
、 表示,则
表示,则
 (填“>”“<”或“=”下同)。
(填“>”“<”或“=”下同)。②y点对应的

 。
。Ⅱ.运用电化学原理可以很好利用
 资源。
资源。(5)火星大气由
 的二氧化碳气体组成,火星探测器采用
的二氧化碳气体组成,火星探测器采用 电池供电,其反应机理如下图:
电池供电,其反应机理如下图:
 电极反应式:
电极反应式:
您最近一年使用:0次
2024-02-25更新
|
847次组卷
|
6卷引用:江西省上饶市2024届高三下学期第一次高考模拟考试化学试题
江西省上饶市2024届高三下学期第一次高考模拟考试化学试题(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)大题预测卷02 (新高考通用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)大题04 化学反应原理综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市上高县2023-2024学年高三下学期5月月考化学试题
10 .  是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
(1)已知下列反应的热化学方程式:
①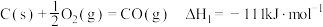
②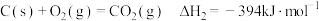
计算 燃烧生成
燃烧生成 反应③
反应③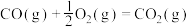 的
的
__________  。
。
(2)已知下列键能数据,结合反应③数据,计算 的键能是
的键能是____________  。
。
(3)650K时,某研究小组测得反应i: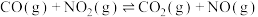 的浓度、速率数据如下:
的浓度、速率数据如下:
已知k为速率常数,一般情况下只与温度有关,实验测得
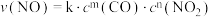 ,通过以上实验数据可知
,通过以上实验数据可知
_________ ,
_______ ;650K时,若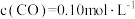 ,
,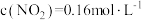 ,
,
________  。
。
(4)在上述实验过程中,同时发生了如下副反应ii: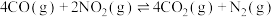 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为____________ 。
(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
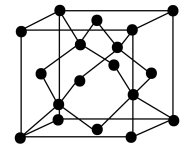
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为__________ nm,晶体密度为____________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 是重要的化工原料,合理使用
是重要的化工原料,合理使用 能发挥其在工业生产、物质合成、速率分析等领域的重要作用。
能发挥其在工业生产、物质合成、速率分析等领域的重要作用。(1)已知下列反应的热化学方程式:
①
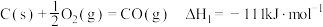
②
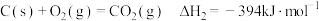
计算
 燃烧生成
燃烧生成 反应③
反应③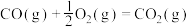 的
的
 。
。(2)已知下列键能数据,结合反应③数据,计算
 的键能是
的键能是 。
。化学键 |
|
|
键能 | 496 | 799 |
(3)650K时,某研究小组测得反应i:
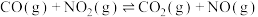 的浓度、速率数据如下:
的浓度、速率数据如下:实验编号 |
|
|
|
① | 0.025 | 0.040 |
|
② | 0.050 | 0.040 |
|
③ | 0.025 | 0.120 |
|
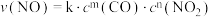 ,通过以上实验数据可知
,通过以上实验数据可知

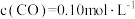 ,
,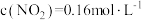 ,
,
 。
。(4)在上述实验过程中,同时发生了如下副反应ii:
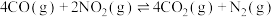 ,650K时,向容积为2L的密闭容器中通入
,650K时,向容积为2L的密闭容器中通入 和
和 ,10min 后体系达到平衡,此时
,10min 后体系达到平衡,此时 、
、 的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为
的物质的量分别为1.8mol、0.3mol,反应i的平衡常数为(5)已知CO是常见配体,配位时简单认为1个CO提供2个电子,EAN规则认为金属的价电子数加上配体提供的电子数等于18时,配位化合物一般较稳定,下列结构能够稳定存在的有__________。
A.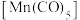 | B.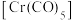 | C.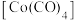 | D.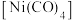 |
(6)CO可以用于生产多晶金刚石箔,将一氧化碳和氢气混合,在高温高压下通过催化剂使之沉积在金属基底上,形成金刚石晶体。金刚石的晶胞如图,晶胞参数为bnm,晶胞中C与C间的最大距离为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次