1 . Ⅰ.铁触媒催化合成氨经历下图所示①至⑥步基元反应(从状态Ⅰ至状态Ⅶ):
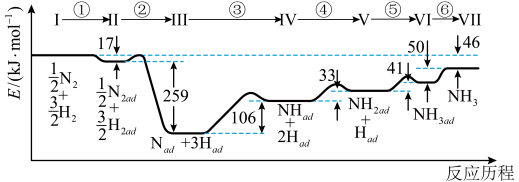
上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g) 2NH3(g) ΔH=
2NH3(g) ΔH=___________ 。
(2)上述反应的ΔS___ 0(填“>”“<”或“=”)。已知:反应N2(g)+3H2(g) 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是____ (填标号)。
A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。
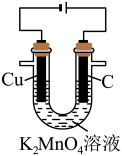
以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH______ (填“升高”“降低”或“不变”)。
(4)铜极、石墨极能否互换并简述理由:___________ 。
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中_______ (填离子符号)向左烧杯迁移。
(6)石墨极的电极反应式为_______ 。实验结论是氧化性:
___  (填>”“<”或“=”)。
(填>”“<”或“=”)。

上图中“ad”表示吸附在催化剂表面的物质。
回答下列问题:
(1)根据上图计算合成氨反应的焓变:N2(g)+3H2(g)
 2NH3(g) ΔH=
2NH3(g) ΔH=(2)上述反应的ΔS
 2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是
2NH3(g)的|ΔS|=199J/(mol·K),则下列温度中,合成氨反应能自发进行的是A.25℃ B.125℃ C.225℃ D.325℃
Ⅱ.高锰酸钾是一种常用的消毒剂和氧化剂。回答下列问题:
实验(一):电解法制备KMnO4。

以石墨、铜为电极,电解K2MnO4溶液制备KMnO4溶液,装置如图所示。
(3)电解过程中,Cu极附近电解质溶液的pH
(4)铜极、石墨极能否互换并简述理由:
实验(二):探究K2FeO4和KMnO4氧化性强弱。装置如图所示。

关闭开关K,观察到左烧杯中紫红色溶液变为浅黄色,右烧杯中无色溶液变为紫红色。
(5)关闭K,盐桥中
(6)石墨极的电极反应式为

 (填>”“<”或“=”)。
(填>”“<”或“=”)。
您最近一年使用:0次
2024-02-02更新
|
182次组卷
|
2卷引用:河北省保定市唐县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 下列说法正确的是
| A.冰在室温下自动融化成水是熵增的过程 |
| B.能够自发进行的反应一定是放热反应 |
| C.能够自发进行的反应一定是熵增的过程 |
| D.△H<0的反应均是自发进行的反应 |
您最近一年使用:0次
3 . 电化学与能源、材料、化工等领域紧密联系,应用广泛。
(1)利用CH4燃料电池电解制备Ca(H2PO4)2,并得到副产物H2、Cl2等,装置如图。
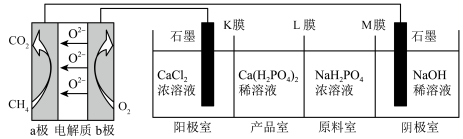
①a极为________ (填“正极”、“负极”、“阴极”或“阳极”),a电极上的电极反应式为________ 。
②K、M、L膜为离子交换膜,其中阳离子交换膜是___________ (填“K膜”、“L膜”、或“M膜”)。
③b极上消耗标准状况下2.24L的O2,理论上阳极室减少___________ molCa2+。
④阴极室的电极反应式为___________ 。
(2)用NaAlO2溶液制备Al2O3的过程如图。
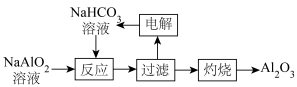
①“灼烧”时得到了Al2O3,该反应能自发的原因是___________ 。
②“电解”时阳极用惰性电极,阳极电极反应式为___________ 。
(1)利用CH4燃料电池电解制备Ca(H2PO4)2,并得到副产物H2、Cl2等,装置如图。

①a极为
②K、M、L膜为离子交换膜,其中阳离子交换膜是
③b极上消耗标准状况下2.24L的O2,理论上阳极室减少
④阴极室的电极反应式为
(2)用NaAlO2溶液制备Al2O3的过程如图。

①“灼烧”时得到了Al2O3,该反应能自发的原因是
②“电解”时阳极用惰性电极,阳极电极反应式为
您最近一年使用:0次
解题方法
4 . 下列有关化学反应的方向说法正确的是
| A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B.化学反应的方向受焓变,熵变、温度共同影响 |
| C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 |
| D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向 |
您最近一年使用:0次
名校
解题方法
5 . 25℃和 时,
时,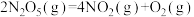
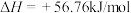 ,该反应能自发进行的原因是
,该反应能自发进行的原因是
 时,
时,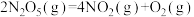
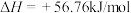 ,该反应能自发进行的原因是
,该反应能自发进行的原因是| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于焓效应 |
您最近一年使用:0次
2023-12-09更新
|
90次组卷
|
6卷引用:河北省青龙满族自治县实验中学2022-2023学年高二上学期1月期末化学试题
名校
6 . 下列说法正确的是
| A.能自发进行的反应一定能迅速发生 |
| B.NH4Cl(s)=NH3(g)+HCl(g)室温下不能自发进行,说明该反应的△H<0 |
| C.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) △H>0,该反应在高温下能自发进行 |
| D.加入合适的催化剂能改变反应的焓变,使非自发反应转化为自发反应 |
您最近一年使用:0次
2023-12-06更新
|
269次组卷
|
2卷引用:河北省石家庄市河北正定中学2023-2024学年高二上学期第二次月考化学试题
名校
7 . 下列说法正确的是
A.向 溶液样品中加入硫酸酸化的 溶液样品中加入硫酸酸化的 溶液,紫色褪去,说明该样品中一定混有 溶液,紫色褪去,说明该样品中一定混有 |
B. 在一定条件下能自发进行,则该反应的 在一定条件下能自发进行,则该反应的 |
C.25℃,向 的氨水溶液中加水, 的氨水溶液中加水, 增大 增大 |
D.反应 达到平衡后,加入KCl固体逆反应速率加快 达到平衡后,加入KCl固体逆反应速率加快 |
您最近一年使用:0次
2023-12-02更新
|
96次组卷
|
2卷引用:河北省泊头市第一中学2023-2024学年高二上学期10月月考化学试题
名校
8 . CO2捕获技术用于去除气流中的CO2或者分离出CO2,有利于减少碳排放。
(1)工业生产中,利用NH3和CO2制取尿素,通常认为该反应分为两步:
i.2NH3(l)+CO2(g)=NH2COONH4(s) △H1=-159kJ•mol-1
ii.NH2COONH4(s)=CO(NH2)2(s)+H2O(l) △H2=+28.5kJ•mol-1
则NH3和CO2制取尿素的总反应的热化学方程式为______ 。
(2)CO2和CH4在一定条件下反应可制得合成气,在体积为1L的恒容密闭容器中分别通入1molCO2和1mol CH4,发生反应:CO2(g)+CH4(g) 2CO(g)+2H2(g) △H=+234kJ•mol-1。
2CO(g)+2H2(g) △H=+234kJ•mol-1。
①该反应的△S______ 0(填“>”“<”或“=”),在______ (填“高温”或“低温”)条件下能自发进行。
②下列情况,能判断该反应达到平衡状态的是______ (填字母)。
A.反应体系的密度保持不变 B.混合气体的平均摩尔质量不变
C.CO2和CH4的物质的量之比不变 D.混合气体中CO的体积分数不变
③若反应体系的起始压强为p1,平衡状态时压强为p2,则CO2的平衡转化率α(CO2)=______ (用含有p1、p2的式子表示)。
(3)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m= 。
。

①图1中投料比m相同,温度从高到低的顺序为______ 。
②图2中m1、m2、m3从大到小的顺序为______ 。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各组分的物质的量分数与温度的关系。则曲线a代表的物质为______ (填化学式)。
(1)工业生产中,利用NH3和CO2制取尿素,通常认为该反应分为两步:
i.2NH3(l)+CO2(g)=NH2COONH4(s) △H1=-159kJ•mol-1
ii.NH2COONH4(s)=CO(NH2)2(s)+H2O(l) △H2=+28.5kJ•mol-1
则NH3和CO2制取尿素的总反应的热化学方程式为
(2)CO2和CH4在一定条件下反应可制得合成气,在体积为1L的恒容密闭容器中分别通入1molCO2和1mol CH4,发生反应:CO2(g)+CH4(g)
 2CO(g)+2H2(g) △H=+234kJ•mol-1。
2CO(g)+2H2(g) △H=+234kJ•mol-1。①该反应的△S
②下列情况,能判断该反应达到平衡状态的是
A.反应体系的密度保持不变 B.混合气体的平均摩尔质量不变
C.CO2和CH4的物质的量之比不变 D.混合气体中CO的体积分数不变
③若反应体系的起始压强为p1,平衡状态时压强为p2,则CO2的平衡转化率α(CO2)=
(3)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H<0。设m为起始时的投料比,即m= 。
。
①图1中投料比m相同,温度从高到低的顺序为
②图2中m1、m2、m3从大到小的顺序为
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各组分的物质的量分数与温度的关系。则曲线a代表的物质为
您最近一年使用:0次
2023-11-24更新
|
154次组卷
|
2卷引用:河北省定州市2023-2024学年高二上学期11月期中考试化学试题
名校
9 . 硫及其化合物的转化是资源利用和环境保护的重要研究课题,回答下列问题:
Ⅰ.若在绝热、恒容的密闭容器中通入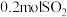 和
和 ,发生反应
,发生反应
 ,一段时间内,正反应速率随时间的变化曲线如图所示。
,一段时间内,正反应速率随时间的变化曲线如图所示。

(1)混合气体的密度:a___________ (填“>”、“<”或“=”)c;___________ (填“高温”、“低温”或“任意温度”)条件下,有利于该反应自发进行。
(2)b点时,
___________ (用分式表示)。
(3)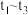 内,
内, 先增大后减小的主要原因为
先增大后减小的主要原因为___________ 。
Ⅱ.常温下,氢硫酸( 的水溶液)的电离方程式可表示为和
的水溶液)的电离方程式可表示为和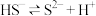 。现将氢硫酸与氢氧化钠溶液混合。已知:
。现将氢硫酸与氢氧化钠溶液混合。已知: ,
, 。
。
(4)对于反应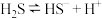 ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为___________ 。
(5)若将等体积等浓度的氢硫酸与氢氧化钠溶液混合,发生反应的化学方程式为___________ 。
(6)常温下,当混合后溶液中的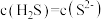 时,该溶液的pH约为
时,该溶液的pH约为___________ (已知:lg2≈0.3)。
Ⅰ.若在绝热、恒容的密闭容器中通入
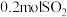 和
和 ,发生反应
,发生反应
 ,一段时间内,正反应速率随时间的变化曲线如图所示。
,一段时间内,正反应速率随时间的变化曲线如图所示。
(1)混合气体的密度:a
(2)b点时,

(3)
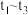 内,
内, 先增大后减小的主要原因为
先增大后减小的主要原因为Ⅱ.常温下,氢硫酸(
 的水溶液)的电离方程式可表示为和
的水溶液)的电离方程式可表示为和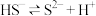 。现将氢硫酸与氢氧化钠溶液混合。已知:
。现将氢硫酸与氢氧化钠溶液混合。已知: ,
, 。
。(4)对于反应
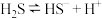 ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为(5)若将等体积等浓度的氢硫酸与氢氧化钠溶液混合,发生反应的化学方程式为
(6)常温下,当混合后溶液中的
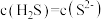 时,该溶液的pH约为
时,该溶液的pH约为
您最近一年使用:0次
名校
10 . 下列说法正确的是
A.稀氨水中存在平衡NH3•H2O NH NH +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 +OH-,若要使平衡逆向移动且c(OH-)增大,可加入NH4Cl固体 |
| B.某固体化合物M不导电,但熔融时能完全电离,则M一定是强电解质 |
| C.熵值增大的反应都能自发进行 |
D.溶液中存在平衡FeCl3+3KSCN Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 Fe(SCN)3+3KCl,平衡时加入KCl固体时,平衡逆向移动 |
您最近一年使用:0次



