名校
解题方法
1 . 下列说法正确的是
A.反应N2(g)+3H2(g) 2NH3(g)的△H<0,△S>0 2NH3(g)的△H<0,△S>0 |
| B.反应2CO+2NO=N2+2CO2在常温下能自发进行,则反应的△H>0,△S<0 |
| C.反应4Fe(s)+3O2(g)=2Fe2O3(s)常温下可自发进行,该反应为吸热反应 |
| D.反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) △H>0能自发进行,其原因是△S>0 |
您最近一年使用:0次
2022-11-16更新
|
141次组卷
|
2卷引用:湖北省十堰市县区普通高中联合体2022-2023学年高二上学期11月期中联考化学试题
名校
2 . 已知反应: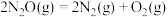
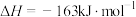 ,下列说法正确的是
,下列说法正确的是
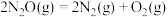
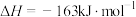 ,下列说法正确的是
,下列说法正确的是| A.高温下自发 | B.低温下自发 | C.任何温度均自发 | D.任何温度不自发 |
您最近一年使用:0次
2022-11-13更新
|
71次组卷
|
2卷引用:湖北省鄂州市部分高中教科研协作体2022-2023学年高二上学期期中考试化学试题
解题方法
3 . 下列关于反应方向、速率和平衡的说法正确的是
| A.凡是放热反应均是自发进行的反应,吸热反应都是非自发的 |
| B.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在常温下能自发进行,说明该反应的ΔH<0 |
您最近一年使用:0次
4 .  在常温下为固体,结构和白磷类似,呈正四面体形,与
在常温下为固体,结构和白磷类似,呈正四面体形,与 互为同素异形体。已知:断裂
互为同素异形体。已知:断裂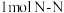 和
和 所需要的能量分别为
所需要的能量分别为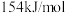 和
和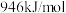 ,下列说法错误的是
,下列说法错误的是
 在常温下为固体,结构和白磷类似,呈正四面体形,与
在常温下为固体,结构和白磷类似,呈正四面体形,与 互为同素异形体。已知:断裂
互为同素异形体。已知:断裂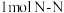 和
和 所需要的能量分别为
所需要的能量分别为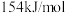 和
和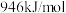 ,下列说法错误的是
,下列说法错误的是A. 含有 含有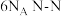 ,而且 ,而且 分子的熔沸点比 分子的熔沸点比 高 高 |
B.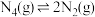 反应放热,故 反应放热,故 比 比 稳定 稳定 |
C.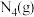 分解生成 分解生成 在任何温度下均能自发进行 在任何温度下均能自发进行 |
D. 和 和 的相互转化为氧化还原反应 的相互转化为氧化还原反应 |
您最近一年使用:0次
5 . 在一定温度下,氯气溶于水的过程为:
①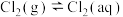 ;
;
②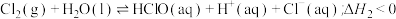 ,下列说法错误的是
,下列说法错误的是
①
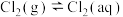 ;
;
②
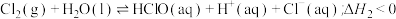 ,下列说法错误的是
,下列说法错误的是A. |
B.②的平衡常数表达式为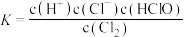 |
C.升高温度,氯水中的 减小 减小 |
D.取氯水稀释,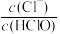 增大 增大 |
您最近一年使用:0次
名校
6 . 某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数如下表所示。请回答下列问题:
(1)根据上述反应可推导出 、
、 与
与 之间的关系:
之间的关系:
_______ ;
(2)根据反应③判断熵变
_______ 0(填“>”“=”或“<”),依据反应自发进行的判据:ΔG=ΔH-TΔS<0时反应可自发进行,判断:在_______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃下,测得反应③在某时刻时,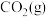 、
、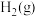 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时v正
,则此时v正____ v逆(填“>”“=”或“<”)。
(4)提高反应③的反应速率且增大 的产率,可采取的措施_______。
的产率,可采取的措施_______。
(5) 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应④完成之后,以
排放并实现资源利用,原理如图1所示。反应④完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
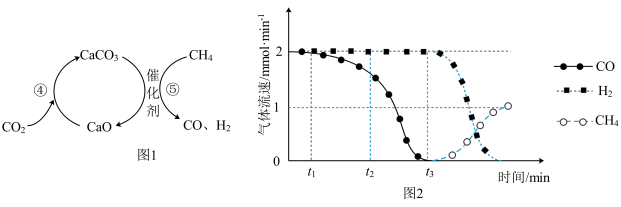
则反应⑤的化学方程式为_______ ,下列叙述正确的是_______ 。
A.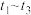 ,
, 比
比 多,且生成
多,且生成 速率不变,有可能是发生副反应
速率不变,有可能是发生副反应
B. 时刻,副反应生成
时刻,副反应生成 的速率大于反应⑤生成
的速率大于反应⑤生成 速率
速率
C. 之后,生成
之后,生成 的速率为0,是因为反应⑤不再发生
的速率为0,是因为反应⑤不再发生
| 化学反应 | 平衡常数 | |||
| 500℃ | 700℃ | 800℃ | ||
①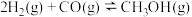  |  | 2.5 | 0.34 | 0.15 |
②  |  | 1.0 | 1.70 | 2.52 |
③  |  | |||
 、
、 与
与 之间的关系:
之间的关系:
(2)根据反应③判断熵变

(3)500℃下,测得反应③在某时刻时,
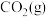 、
、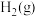 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 、
、 ,则此时v正
,则此时v正(4)提高反应③的反应速率且增大
 的产率,可采取的措施_______。
的产率,可采取的措施_______。| A.扩大反应容器的容积 | B.使用合适的催化剂 |
| C.缩小反应容器的容积 | D.从平衡体系中及时分离出 |
 捕获和转化可减少
捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应④完成之后,以
排放并实现资源利用,原理如图1所示。反应④完成之后,以 为载气,将恒定组成的
为载气,将恒定组成的 、
、 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
,在催化剂上有积碳。
则反应⑤的化学方程式为
A.
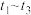 ,
, 比
比 多,且生成
多,且生成 速率不变,有可能是发生副反应
速率不变,有可能是发生副反应
B.
 时刻,副反应生成
时刻,副反应生成 的速率大于反应⑤生成
的速率大于反应⑤生成 速率
速率C.
 之后,生成
之后,生成 的速率为0,是因为反应⑤不再发生
的速率为0,是因为反应⑤不再发生
您最近一年使用:0次
7 . 下列说法正确的是
| A.熵增的反应都是自发的,自发反应的现象一定非常明显 |
B.应该投入大量资金研究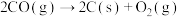  该过程发生的条件,以解决含碳燃料不充分燃烧引起的环境问题 该过程发生的条件,以解决含碳燃料不充分燃烧引起的环境问题 |
C.已知  ,该反应吸热,一定不能自发进行 ,该反应吸热,一定不能自发进行 |
D.常温下,若反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
您最近一年使用:0次
2022-11-09更新
|
204次组卷
|
2卷引用:湖北省问津联合体2022-2023学年高二上学期10月质量检测化学试题
名校
解题方法
8 . Ⅰ.已知在氨水中存在下平衡:NH3+H2O NH3·H2O
NH3·H2O NH
NH +OH-。
+OH-。
(1)向氨水中加入 固体时,平衡向
固体时,平衡向_______ (填“左”或“右”)移动,OH-的浓度_______ (填“增大”或“减小”,下同), 的浓度
的浓度_______ 。
(2)向氨水中加入浓盐酸,平衡向_______ (填“左”或“右”)移动,此时溶液中浓度减小的微粒有_______ 。
(3)向氨水中加入少量的NaOH固体,平衡向_______ (填“左”或“右”)移动。
Ⅱ.地下水中的氮污染主要是由 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:2NO
将硝酸盐还原成氮气:2NO +5H2
+5H2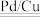 N2↑+2OH-+4H2O。
N2↑+2OH-+4H2O。
(4)下列说法错误的是_______ (填序号)。
A.氮肥 溶于水的过程中熵值增大
溶于水的过程中熵值增大
B.在酸性条件下,活泼金属与 反应属于自发反应
反应属于自发反应
C.Pd/Cu双金属催化剂是该反应是否能自发发生的决定因素
(5)已知:2NO +5H2
+5H2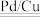 N2↑+2OH-+4H2O的
N2↑+2OH-+4H2O的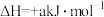 ,
,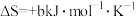 (a、b均为正值),该反应
(a、b均为正值),该反应_______ (填“能”“不能”或“无法判断是否能”)自发进行。
 NH3·H2O
NH3·H2O NH
NH +OH-。
+OH-。(1)向氨水中加入
 固体时,平衡向
固体时,平衡向 的浓度
的浓度(2)向氨水中加入浓盐酸,平衡向
(3)向氨水中加入少量的NaOH固体,平衡向
Ⅱ.地下水中的氮污染主要是由
 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下, 将硝酸盐还原成氮气:2NO
将硝酸盐还原成氮气:2NO +5H2
+5H2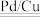 N2↑+2OH-+4H2O。
N2↑+2OH-+4H2O。(4)下列说法错误的是
A.氮肥
 溶于水的过程中熵值增大
溶于水的过程中熵值增大B.在酸性条件下,活泼金属与
 反应属于自发反应
反应属于自发反应C.Pd/Cu双金属催化剂是该反应是否能自发发生的决定因素
(5)已知:2NO
 +5H2
+5H2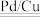 N2↑+2OH-+4H2O的
N2↑+2OH-+4H2O的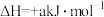 ,
,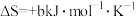 (a、b均为正值),该反应
(a、b均为正值),该反应
您最近一年使用:0次
9 . 已知: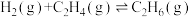
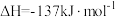 。请回答下列问题:
。请回答下列问题:
(1)该反应在_______ (填“低温”、“高温”或“任何温度”下能自发进行。
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
(3)若在10 L的密闭容器内2 mol H2(g)与a molC2H4(g)进行上述反应,测得 的平衡转化率与投料比X,
的平衡转化率与投料比X,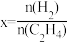 以及温度的关系如图所示。
以及温度的关系如图所示。
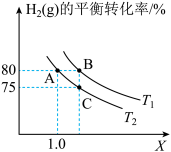
①反应从开始分别进行到A、B、C点时,_______ (填“吸收”或“放出”)的热量QA、QB、QC由大到小的顺序为_______ 。
②T1_______ (填“>”、“<”或“=”)T2。
③B点对应的体系中a=_______ 。A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。
(4)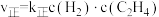 ,
,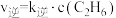 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
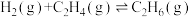
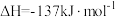 。请回答下列问题:
。请回答下列问题:(1)该反应在
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 | B.c正(H2)=c逆(C2H6) |
| C.容器内混合气体的压强不变 | D.容器内混合气体的密度不变 |
 的平衡转化率与投料比X,
的平衡转化率与投料比X,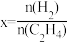 以及温度的关系如图所示。
以及温度的关系如图所示。
①反应从开始分别进行到A、B、C点时,
②T1
③B点对应的体系中a=
(4)
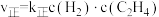 ,
,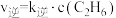 ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。| A.k正增大的倍数大于k逆 | B.k正增大的倍数小于k逆 |
C.k正减小的倍数大于 | D.k正减小的倍数小于k逆 |
您最近一年使用:0次
2022-11-07更新
|
112次组卷
|
3卷引用:湖北省恩施州高中教育联盟2022-2023学年高二上学期期中考试化学试题
名校
解题方法
10 . 下列表述正确的是
| A.△H>0和△S>0的反应,在任何温度下都不能自发进行 |
B.根据 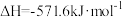 可知氢气的燃烧热为571.6 kJ/mol 可知氢气的燃烧热为571.6 kJ/mol |
| C.HCl溶液和NaOH溶液反应的中和热△H =-57.3 kJ/mol,则含2 mol硫酸的稀溶液与足量氢氧化钡溶液反应放热为114.6 kJ |
D.已知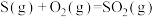 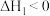 , ,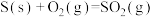 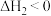 ,则△H1<△H2 ,则△H1<△H2 |
您最近一年使用:0次
2022-11-04更新
|
138次组卷
|
7卷引用:湖北省六校新高考联盟学校2022-2023学年高二上学期9月联考化学试题



