解题方法
1 . 氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。甲烷水蒸气催化重整是制高纯氢的方法之一,在1L固定容积密闭容器中投入1.8molCH4和3.6molH2O(g),若只发生反应:CH4(g)+2H2O(g) CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。

(1)金属氢化物是一类储氢材料,如MgH2,该物质能与水反应:MgH2+2H2O=Mg(OH)2+2H2↑。上述反应涉及的物质中含有离子键的是_______ 。
(2)①CH4(g)+2H2O(g) CO2(g)+4H2(g),说明该反应自发进行的原因
CO2(g)+4H2(g),说明该反应自发进行的原因_______ 。
②反应在10min时的平衡常数K=_______ (列出数学计算式,不必算出结果)。
(3)第6min时改变的条件是_______ 。
(4)画出X物质4min~9min之间的变化图像_______ 。
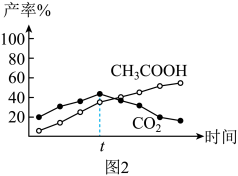
(5)反应的过程中发生副反应CO2(g)+CH4(g)=CH3COOH(g) △H2=-32.2kJ•mol-1,反应所用的时间和CO2、CH3COOH的产率如图2所示,t时刻后,CO2的产率下降,其原因是_______ 。
(6)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s) 2NH3(g)+CO2(g)。下列各项:
2NH3(g)+CO2(g)。下列各项:
①2v(NH3)正=c(CO2)逆;
②密闭容器中总压强不变;
③密闭容器中混合气体的密度不变;
④密闭容器中氨气的体积分数不变;
⑤密闭容器中c(NH3)不变。
能判断该反应已经达到化学平衡状态的是_______ 。
 CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
CO2(g)+4H2(g) △H1=+165.0kJ•mol-1,测得CH4、H2O及某一生成物X的物质的量浓度随反应时间的变化如图1所示(反应中条件有变化时,只考虑改变一个条件)。
(1)金属氢化物是一类储氢材料,如MgH2,该物质能与水反应:MgH2+2H2O=Mg(OH)2+2H2↑。上述反应涉及的物质中含有离子键的是
(2)①CH4(g)+2H2O(g)
 CO2(g)+4H2(g),说明该反应自发进行的原因
CO2(g)+4H2(g),说明该反应自发进行的原因②反应在10min时的平衡常数K=
(3)第6min时改变的条件是
(4)画出X物质4min~9min之间的变化图像
(5)反应的过程中发生副反应CO2(g)+CH4(g)=CH3COOH(g) △H2=-32.2kJ•mol-1,反应所用的时间和CO2、CH3COOH的产率如图2所示,t时刻后,CO2的产率下降,其原因是

(6)将一定量纯净的氨基甲酸铵置于密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:H2NCOONH4(s)
 2NH3(g)+CO2(g)。下列各项:
2NH3(g)+CO2(g)。下列各项:①2v(NH3)正=c(CO2)逆;
②密闭容器中总压强不变;
③密闭容器中混合气体的密度不变;
④密闭容器中氨气的体积分数不变;
⑤密闭容器中c(NH3)不变。
能判断该反应已经达到化学平衡状态的是
您最近一年使用:0次
2 . 下列说法不正确的是
A.测定盐酸和 溶液的中和热时,每次实验均应测量三个温度,即盐酸起始温度、 溶液的中和热时,每次实验均应测量三个温度,即盐酸起始温度、 溶液起始温度和反应后的终止温度 溶液起始温度和反应后的终止温度 |
B.反应 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
| C.能够设计成原电池的反应是自发进行的氧化还原反应 |
| D.工业合成氨中需用高温,目的是提高平衡转化率 |
您最近一年使用:0次
名校
3 . 氢气和氧气发生反应生成水的过程用如下模型表示,“—”表示化学键。下列说法正确的是


| A.过程I是放热过程 |
| B.该反应的能量转化形式只能以热能的形式进行 |
| C.a的总能量大于d的总能量 |
| D.1 mol H2O在不同状态时的熵值:S[H2O(l)]<S[H2O(s)] |
您最近一年使用:0次
2022-12-08更新
|
163次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2023-2024学年高二下学期开学化学试题
名校
解题方法
4 . 下列说法不正确的是
A. 、 、 的反应在任何温度下都能自发进行 的反应在任何温度下都能自发进行 |
| B.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小 |
| C.焓变和熵变都与反应的自发性有关,因此焓变或熵变不可单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂可改变化学反应自发进行的方向 |
您最近一年使用:0次
2022-12-05更新
|
257次组卷
|
3卷引用:广东省深圳市蛇口育才教育集团育才中学2023-2024学年高二上学期阶段检测(一)化学试题
解题方法
5 . 无机阻燃剂 Al(OH)3作用原理为:2Al(OH)3(s)=Al2O3(s)+3H2O(g)。关于 Al(OH)3阻燃反应的焓变和熵变说法正确的是
| A.ΔH >0, ΔS >0 | B.ΔH >0, ΔS <0 |
| C.ΔH <0, ΔS >0 | D.ΔH <0, ΔS<0 |
您最近一年使用:0次
名校
解题方法
6 . 已知反应
 的反应机理如下:
的反应机理如下:
① (快)
(快)
② (慢)
(慢)
③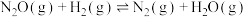 (快);
(快);
下列有关说法正确的是

 的反应机理如下:
的反应机理如下:①
 (快)
(快)②
 (慢)
(慢)③
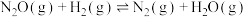 (快);
(快);下列有关说法正确的是
| A.该反应在任何温度下都能自发进行 |
| B.总反应速率取决于② |
C. 和 和 是该反应的催化剂 是该反应的催化剂 |
| D.加压活化分子数和活化分子百分数都增大 |
您最近一年使用:0次
2022-11-23更新
|
227次组卷
|
2卷引用:广东省东莞实验中学2022-2023学年高二下学期期中考试化学试题
名校
7 . 下列有关说法正确的是
A.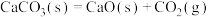 室温下不能自发进行,说明该反应的 室温下不能自发进行,说明该反应的 |
B. 室温下能自发进行,说明该反应的 室温下能自发进行,说明该反应的 |
C.  ,其他条件不变时升高温度,反应速率 ,其他条件不变时升高温度,反应速率 和氢气的平衡转化率均增大 和氢气的平衡转化率均增大 |
D. 的电离常数 的电离常数 随着温度的升高而增大,说明 随着温度的升高而增大,说明 的电离放热 的电离放热 |
您最近一年使用:0次
名校
解题方法
8 . 化学用语是学习化学的重要工具,下列化学用语中,正确的是
| A.已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,氢气的燃烧热为241.8 kJ·mol-1 |
| B.氢硫酸溶液显酸性的主要原因:H2S ⇌2H++S2- |
| C.某反应ΔH<0,ΔS>0,则该反应在任意条件下均可自发进行 |
| D.100℃时,纯水的PH=6,呈酸性 |
您最近一年使用:0次
名校
解题方法
9 . 下列说法不正确的是。
| A.盐酸与碳酸氢钠的反应是吸热的 |
| B.乙烯聚合为聚乙烯是一个熵减的过程 |
| C.自发反应就是能较快进行的反应,非自发反应就是不可能发生的反应 |
D.反应 在低温下能自发进行,则该反应的 在低温下能自发进行,则该反应的 |
您最近一年使用:0次
2022-11-16更新
|
99次组卷
|
3卷引用:广东省深圳市校联盟2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
10 . 多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
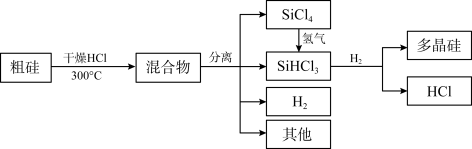
回答下列问题:
Ⅰ.硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,
(1)该反应的热化学方程式为_______ 。
Ⅱ.将SiCl4氢化为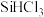 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:
①SiCl4(g)+H2(g) SiHCl3(g)+HCl(g) △H1>0
SiHCl3(g)+HCl(g) △H1>0
②3SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0
③2SiCl4(g)+H2(g)+Si(s)+HCl(g)=3SiHCl3(g) △H3
(2)已知体系自由能变△G=△H-T△S,△G<0时反应自发进行。三个氢化反应的△G与温度的关系如图1所示,可知:反应①能自发进行的最低温度是_______ ;相同温度下,反应②比反应①的△G小,主要原因是_______ 。

(3)以上反应在不同温度下反应相同时间的某一时刻,反应②中SiCl4转化率如图2所示。下列叙述正确的是_______ (填序号)。
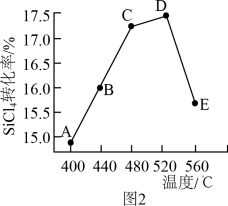
a.B点:v正>v逆 b.v正:A点>E点 c.反应适宜温度:480-520℃
(4)反应③的△H3=_______ (用△H1,△H2表示)。温度升高,反应③的平衡常数K_______ (填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除SiCl4、SiHCl3和Si外,还有_______ (填分子式)。

回答下列问题:
Ⅰ.硅粉与HCl在300℃时反应生成1 mol SiHCl3气体和H2,放出225 kJ热量,
(1)该反应的热化学方程式为
Ⅱ.将SiCl4氢化为
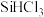 有三种方法,对应的反应依次为:
有三种方法,对应的反应依次为:①SiCl4(g)+H2(g)
 SiHCl3(g)+HCl(g) △H1>0
SiHCl3(g)+HCl(g) △H1>0②3SiCl4(g)+2H2(g)+Si(s)
 4SiHCl3(g) △H2<0
4SiHCl3(g) △H2<0③2SiCl4(g)+H2(g)+Si(s)+HCl(g)=3SiHCl3(g) △H3
(2)已知体系自由能变△G=△H-T△S,△G<0时反应自发进行。三个氢化反应的△G与温度的关系如图1所示,可知:反应①能自发进行的最低温度是

(3)以上反应在不同温度下反应相同时间的某一时刻,反应②中SiCl4转化率如图2所示。下列叙述正确的是

a.B点:v正>v逆 b.v正:A点>E点 c.反应适宜温度:480-520℃
(4)反应③的△H3=
(5)由粗硅制备多晶硅过程中循环使用的物质除SiCl4、SiHCl3和Si外,还有
您最近一年使用:0次



