1 . 氢气与氧气生成水的反应是氢能源应用的重要途径。下列有关说法正确的是
| A.H2的燃烧热为ΔH=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g)ΔH=+571.6 kJ/mol |
| B.氢氧燃料电池的负极反应为O2+2H2O+4e—=4OH— |
| C.常温常压下氢氧燃料电池放电过程中消耗11.2L H2,转移电子数目为6.02×1023 |
| D.一定温度下,反应2H2(g)+O2(g)=2H2O(g)能自发进行,该反应的ΔH<0 |
您最近一年使用:0次
名校
解题方法
2 . 第24届冬奥会在北京、张家口两地举办。国家速滑馆“冰丝带”里屡破奥运会纪录,该冰场是冬奥史上“最快冰面”,冰层表面结构如图所示。下列有关说法错误的是


| A.冰熔化是吸热的熵增过程 |
| B.第一层固态冰中,水分子间通过氢键形成空间网状结构,密度比液态水小 |
| C.固态水分子之间的化学键较强,“准液体”水分子之间的化学键较弱 |
| D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产生“流动性水分子”,使冰面变滑 |
您最近一年使用:0次
2023-02-12更新
|
322次组卷
|
2卷引用:广东省阳山县南阳中学2022-2023学年高二下学期第一次月考化学试题
3 . 空燃比是指机动车内燃机气缸内混合气中空气与燃料之间的质量比例,通过调节空燃比可控制机动车尾气中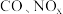 、碳氢化合物等污染物的排放。内燃机工作时,气缸中会发生反应
、碳氢化合物等污染物的排放。内燃机工作时,气缸中会发生反应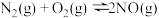
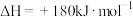 ,下列说法正确的是
,下列说法正确的是
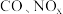 、碳氢化合物等污染物的排放。内燃机工作时,气缸中会发生反应
、碳氢化合物等污染物的排放。内燃机工作时,气缸中会发生反应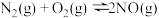
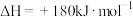 ,下列说法正确的是
,下列说法正确的是A.上述反应在高温下可以自发进行,则该反应 |
B.上述反应平衡常数表达式 |
| C.气缸内温度升高,正反应速率加快,逆反应速率减慢 |
| D.实际应用中,控制气缸内空燃比越小,机动车尾气对环境的污染越小 |
您最近一年使用:0次
名校
4 . 对于某可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是| A.该反应为放热反应,则该反应只有在低温下才能自发进行 |
| B.保持容器内气体压强不变,向其中加入He,化学反应速率不变 |
| C.保持容器容积不变,向其中加入He,化学反应速率增大 |
| D.达到化学平衡时,4v正(O2)=5v逆(NO) |
您最近一年使用:0次
5 . 下列说法正确的是
| A.ΔS>0的反应一定是自发的 |
| B.平衡产率是化学反应的最大限度,是无法改变的 |
| C.电离与电解是相同的化学过程 |
| D.若MA为强碱弱酸盐,Ka(HA)越小,则Kh(A—)越大 |
您最近一年使用:0次
名校
6 . 下列说法中,正确的是
A. 转化变为 转化变为 时,熵减小 时,熵减小 |
| B.使用催化剂能使非自发反应转化成自发反应 |
C.室温下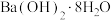 晶体与 晶体与 晶体的反应是非自发反应 晶体的反应是非自发反应 |
D.某反应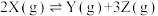 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 、 、 |
您最近一年使用:0次
名校
解题方法
7 . 下列依据热化学方程式得出的结论正确的是
A.反应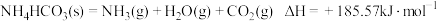 能自发进行是因为体系有自发地向混乱度增大的方向转变的倾向 能自发进行是因为体系有自发地向混乱度增大的方向转变的倾向 |
B.在一定温度和压强下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 ,放出热量19.3kJ,则其热化学方程式为 ,放出热量19.3kJ,则其热化学方程式为 |
| C.已知酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
D.已知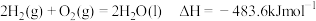 ,则氢气的燃烧热为 ,则氢气的燃烧热为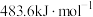 |
您最近一年使用:0次
名校
解题方法
8 . TiN有着诱人的金黄色,熔点高、硬度大、化学稳定性好,可应用于高温结构材料和超导材料。利用气相沉积法制备氮化钛的反应为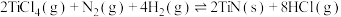
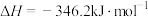 。回答下列问题:
。回答下列问题:
(1)若该反应高温时为非自发反应,则该反应的
___________ 0(填“>”或“<”)。
(2)将0.2mol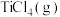 、2mol
、2mol 和2mol
和2mol 投入2L反应容器中,只改变温度,测得TiN的质量变化如下表所示:
投入2L反应容器中,只改变温度,测得TiN的质量变化如下表所示:
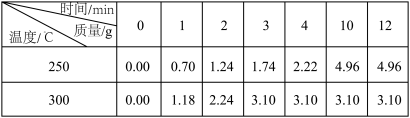
①250℃时,前2min内,用 的浓度变化表示的平均反应速率
的浓度变化表示的平均反应速率
___________ 。
②平衡后,逆反应的速率:v(逆,250℃)___________ v(逆,300℃)(填“>”或“<”,下同)。
③达到平衡时,反应放出的热量:Q(250℃)___________ Q(300℃)。
(3)将0.40mol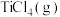 ,0.30mol
,0.30mol 和1.20mol
和1.20mol 投入到某刚性反应器中,测得在反应过程中TiN的质量和反应体系的总压强p随着温度升高的变化曲线如图:
投入到某刚性反应器中,测得在反应过程中TiN的质量和反应体系的总压强p随着温度升高的变化曲线如图:

①下列说法正确的是___________ (填选项字母)。
A.a、b、c三点时,该反应均处于平衡状态
B.m→n过程中,该化学平衡逆向移动
C.混合气体的平均相对分子质量: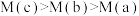
②a、b、c三点对应温度下的平衡常数由大到小的顺序为___________ 。
③温度为 K时,该反应达到平衡时,氢气的转化率
K时,该反应达到平衡时,氢气的转化率
___________ (保留三位有效数字);以气体分压表示的该反应的平衡常数
___________ MPa。
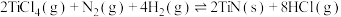
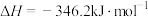 。回答下列问题:
。回答下列问题:(1)若该反应高温时为非自发反应,则该反应的

(2)将0.2mol
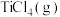 、2mol
、2mol 和2mol
和2mol 投入2L反应容器中,只改变温度,测得TiN的质量变化如下表所示:
投入2L反应容器中,只改变温度,测得TiN的质量变化如下表所示:
①250℃时,前2min内,用
 的浓度变化表示的平均反应速率
的浓度变化表示的平均反应速率
②平衡后,逆反应的速率:v(逆,250℃)
③达到平衡时,反应放出的热量:Q(250℃)
(3)将0.40mol
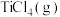 ,0.30mol
,0.30mol 和1.20mol
和1.20mol 投入到某刚性反应器中,测得在反应过程中TiN的质量和反应体系的总压强p随着温度升高的变化曲线如图:
投入到某刚性反应器中,测得在反应过程中TiN的质量和反应体系的总压强p随着温度升高的变化曲线如图:
①下列说法正确的是
A.a、b、c三点时,该反应均处于平衡状态
B.m→n过程中,该化学平衡逆向移动
C.混合气体的平均相对分子质量:
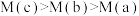
②a、b、c三点对应温度下的平衡常数由大到小的顺序为
③温度为
 K时,该反应达到平衡时,氢气的转化率
K时,该反应达到平衡时,氢气的转化率

您最近一年使用:0次
9 . 研究化学反应进行的方向对于反应设计具有重要意义,下列说法正确的是
A.乙烯聚合为聚乙烯,反应的 ,因此该反应不能自发进行 ,因此该反应不能自发进行 |
| B.其他条件不变的情况下,使用催化剂,可以改变汽车尾气的反应方向 |
C.在室温下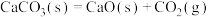 不能自发进行,说明该反应的 不能自发进行,说明该反应的 |
D.一定温度下,反应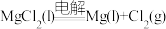 的 的 、 、 |
您最近一年使用:0次
10 . 已知胆矾溶于水时,溶液温度降低,结合图分析(Q1、Q2、Q3均大于0,单位是kJ/mol),下列相关说法错误的是
CuSO4•5H2O(s) CuSO4(s)+5H2O(l)
CuSO4(s)+5H2O(l) CuSO4(aq)+5H2O(l)
CuSO4(aq)+5H2O(l)
H2O(l) H2O(g)
H2O(g)
CuSO4•5H2O(s)
 CuSO4(s)+5H2O(l)
CuSO4(s)+5H2O(l) CuSO4(aq)+5H2O(l)
CuSO4(aq)+5H2O(l) H2O(l)
 H2O(g)
H2O(g)| A.Q1>Q2 |
| B.20g10%的CuSO4溶液蒸干至质量不再变化时,吸收Q3kJ的热量 |
| C.1molH2O(l)转变为1molH2O(g)时吸收热量Q3kJ |
| D.H2O(l)=H2O(g)能自发进行,说明熵增的方向是自发进行的方向 |
您最近一年使用:0次



