1 . 常温下,将体积均为 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是
 的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随
的HA溶液和BOH溶液分别加水稀释至V,溶液的pH随 的变化如图所示。已知
的变化如图所示。已知 ,下列说法正确的是
,下列说法正确的是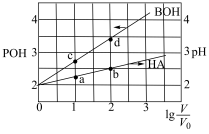
A.电离常数: |
| B.水的电离程度:b>d |
C.升温,a点溶液中 增大 增大 |
| D.等浓度HA和BOH溶液等体积混合,溶液的pH<7 |
您最近一年使用:0次
名校
解题方法
2 . 常温时,采用甲基橙和酚酞双指示剂,用盐酸滴定Na2CO3溶液,溶液中 lgc(H2CO3)、 lgc(HCO )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
 )、lgc(CO
)、lgc(CO )、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是
)、lgc(H+ )、lgc(OH-)随溶液 pH 的变化及滴定曲线如图所示,下列说法不正确的是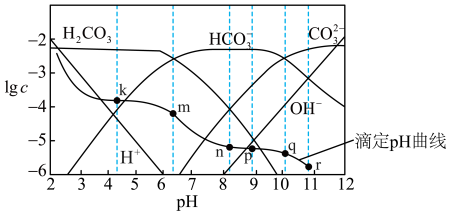
| A.整个滴定过程中可先用酚酞再用甲基橙作指示剂 |
| B.n点的pH为m点和q点pH的平均值 |
C.r点溶液中:c(OH-) = c(H+ )+c(HCO )+c(H2CO3) )+c(H2CO3) |
| D.r点到 k 点对应的变化过程中,溶液中水的电离程度一直减小 |
您最近一年使用:0次
2024-01-08更新
|
169次组卷
|
10卷引用:河北省部分重点高中2023-2024学年高三上学期第一次综合素养测评化学试题
河北省部分重点高中2023-2024学年高三上学期第一次综合素养测评化学试题河北省衡水中学2023-2024学年高三上学期一调考试化学试题河北省石家庄市部分名校2024届高三上学期一调考试化学试题河北省唐山市第二十三中2023-2024学年高三上学期期中考试化学试题辽宁省朝阳市2021届高三第四次模拟考试化学试题广东省河源中学2023-2024学年上学期高三年级一调考试化学试题内蒙古赤峰二中2023-2024学年高三上学期第三次月考化学试题2024届陕西省西安市西北工业大学附属中学高三上学期第二次模拟考试理科综合试题-高中化学2024届陕西省西安市第一中学高三上学期模拟测试理科综合试题-高中化学湖南省长沙麓山国际实验学校2023-2024学年高二下学期4月份学情检测化学试卷
3 . 25℃时,分别向浓度均为 ,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的
,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的 与加入氨水的体积变化关系如图所示。下列说法正确的是
与加入氨水的体积变化关系如图所示。下列说法正确的是
 ,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的
,体积均为20mL的HX和HY的溶液中滴入等物质的量浓度的氨水,溶液中水电离出的 与加入氨水的体积变化关系如图所示。下列说法正确的是
与加入氨水的体积变化关系如图所示。下列说法正确的是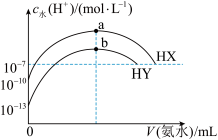
A.HY的电离方程式为 |
B.b点时溶液中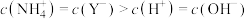 |
C.HX的电离平衡常数约为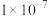 |
| D.a、b两点对应溶液中存在的微粒种类、数目相同 |
您最近一年使用:0次
2024-01-07更新
|
98次组卷
|
3卷引用:河北省沧州市部分学校2023-2024学年高二上学期11月期中考试化学试题
4 . 以下事实不能 说明醋酸是弱电解质的是
| A.氢离子浓度相同的醋酸溶液和盐酸溶液,前者浓度大 |
B.醋酸溶液中CH3COOH分子和 离子共存 离子共存 |
| C.相同浓度的醋酸溶液和硫酸溶液,后者导电性强 |
D.将 醋酸溶液体积稀释十倍,稀释后 醋酸溶液体积稀释十倍,稀释后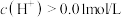 |
您最近一年使用:0次
2023-12-28更新
|
87次组卷
|
2卷引用:河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
5 . 常温下,将 溶液滴加到
溶液滴加到 等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
 溶液滴加到
溶液滴加到 等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
等浓度的某一元酸HA溶液中,测得混合溶液的pH与粒子浓度比值的负对数的变化关系如图所示下列叙述不正确的是
A.m点对应的 溶液体积小于 溶液体积小于 |
B. 的数量级为 的数量级为 |
C.l点所示溶液中: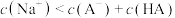 |
D.各点的水溶液中水的电离程度大小关系: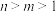 |
您最近一年使用:0次
2023-12-27更新
|
441次组卷
|
8卷引用:河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题
河北省保定市高碑店市崇德实验中学2023-2024学年高二上学期1月考试化学试题湖北省孝感市孝感高级中学2021届高三2月调研考试化学试题(已下线)学科网2021年高三3月大联考考后强化卷(新课标Ⅲ卷)(已下线)学科网2021年高三3月大联考考后强化卷(新课标Ⅰ卷)江西省南昌市第十中学2021届高三下学期第一次月考化学试题湖南省武冈市第一中学2021-2022学年高三下学期5月月考化学试题内蒙古赤峰二中2023-2024学年高三上学期第四次月考化学试题(已下线)题型14 电解质溶液-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
2023高三·全国·专题练习
名校
6 . 已知K2Cr2O7溶液中存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
 +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
| A.图中T1℃>T2℃ |
B.t1后溶液中有2c(Cr2O )+c(CrO )+c(CrO )=c(K+) )=c(K+) |
| C.T2℃时,上述反应的平衡常数的数量级是10-12 |
D.T1℃下,加入一定量K2Cr2O7固体后达到新平衡时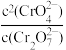 的值增大 的值增大 |
您最近一年使用:0次
2023-12-16更新
|
197次组卷
|
3卷引用:河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)
7 . 常温下,用0.100mol·L-1盐酸滴定20.00mL0.100mol·L-1NH3·H2O溶液,溶液的pH与所加盐酸体积的关系如图所示(不考虑溶液的体积和温度变化)。下列说法错误的是
已知: 。
。
已知:
 。
。
| A.a点对应的pH约为11.1 |
B.b点溶液中, |
| C.a→c的过程中,水的电离程度先减小后增大 |
| D.NH3·H2O溶液属于混合物,不属于电解质 |
您最近一年使用:0次
2023-12-04更新
|
249次组卷
|
3卷引用:河北省邢台市四校联盟2023-2024学年高二上学期11月月考化学试题
名校
解题方法
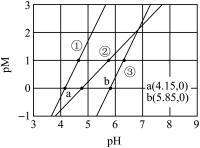
8 . 常温下,向含有CH3COOH、CuSO4、FeSO4的工业废水中逐滴加入NaOH溶液,pM随pH变化关系如图所示[pM表示 或
或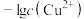 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: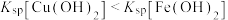 ;当离子浓度
;当离子浓度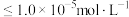 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
 或
或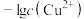 或
或 ],曲线①③斜率相同。已知:
],曲线①③斜率相同。已知: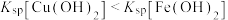 ;当离子浓度
;当离子浓度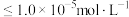 时,可认为该离子沉淀完全。下列说法不正确的是
时,可认为该离子沉淀完全。下列说法不正确的是
A.曲线①表示 与pH的关系 与pH的关系 |
B.pH=6时,溶液中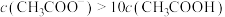 |
C.pH=7时,可认为 沉淀完全 沉淀完全 |
D.pH=8时 |
您最近一年使用:0次
2023-12-01更新
|
422次组卷
|
5卷引用:河北省沧州市部分高中2023-2024学年高三上学期11月期中考试化学试题
河北省沧州市部分高中2023-2024学年高三上学期11月期中考试化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)(已下线)选择题11-15安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题江西省宜春市丰城市第九中学2023-2024学年高二下学期4月月考化学试题
名校
9 .  为二元弱酸,常温下将
为二元弱酸,常温下将 的
的 溶液滴入
溶液滴入 的
的 溶液中,溶液中
溶液中,溶液中 (或
(或 )的分布分数
)的分布分数 溶液体积
溶液体积 的
的 与
与 的关系如图所示。[已知:
的关系如图所示。[已知: ]下列叙述正确的是
]下列叙述正确的是
 为二元弱酸,常温下将
为二元弱酸,常温下将 的
的 溶液滴入
溶液滴入 的
的 溶液中,溶液中
溶液中,溶液中 (或
(或 )的分布分数
)的分布分数 溶液体积
溶液体积 的
的 与
与 的关系如图所示。[已知:
的关系如图所示。[已知: ]下列叙述正确的是
]下列叙述正确的是
A.曲线I表示的是 的分布分数变化曲线 的分布分数变化曲线 |
B. 的 的 数量级为 数量级为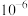 |
C.b点对应的溶液中, |
D.在b、c、d三点中,水的电离程度大小关系为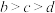 |
您最近一年使用:0次
2023-11-26更新
|
495次组卷
|
8卷引用:河北省承德市双滦区实验中学2023-2024学年高三上学期一轮复习联考(三) 化学试题
河北省承德市双滦区实验中学2023-2024学年高三上学期一轮复习联考(三) 化学试题 河北省保定市唐县第一中学2023-2024学年高二上学期1月期末化学试题(已下线)选择题11-14湖南省长沙市长郡中学2023-2024学年高二上学期12月阶段性检测化学试题(已下线)选择题11-14(已下线)选择题11-14(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)江西省宜春市上高县2023-2024学年高三下学期5月月考化学试题
名校
解题方法
10 . 常温下,向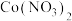 、
、 和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表
和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表 、
、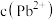 或
或 ,
, 。
。

下列叙述错误的是
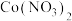 、
、 和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表
和 HR 的混合液中滴加 NaOH 溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表 、
、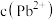 或
或 ,
, 。
。
下列叙述错误的是
A.X、Z分别代表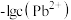 、 、 与 pH 的关系 与 pH 的关系 |
B.常温下,弱酸 HR 的电离常数 |
| C.图中 a 点对应的 pH 为6.5 |
D.常温下, 和 和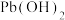 共存时: 共存时: |
您最近一年使用:0次
2023-11-16更新
|
869次组卷
|
6卷引用:河北省沧州市2023-2024学年高三上学期期末联考化学试题



