解题方法
1 . 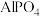 的沉淀溶解平衡曲线如图所示。下列说法不正确的是
的沉淀溶解平衡曲线如图所示。下列说法不正确的是

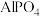 的沉淀溶解平衡曲线如图所示。下列说法不正确的是
的沉淀溶解平衡曲线如图所示。下列说法不正确的是
A.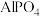 沉淀溶解是吸热的过程 沉淀溶解是吸热的过程 |
B.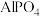 在b点对应的溶解度大于c点 在b点对应的溶解度大于c点 |
C. |
D.图中四个点的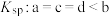 |
您最近一年使用:0次
2023-08-04更新
|
511次组卷
|
2卷引用:陕西省渭南市白水县2020~2021学年高二上学期期末考试化学试题
2 . 某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:
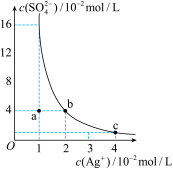
(1)a点表示Ag2SO4________ (填“饱和”或“不饱和”)溶液。
(2)b点对应的Ksp________ (填“<”“>”或“=”)c点对应的Ksp。
(3)现将足量的Ag2SO4分别放入:
a.40 mL 0.01 mol·L-1 K2SO4溶液
b.10 mL蒸馏水
c.10 mL 0.02 mol·L-1 H2SO4溶液
则Ag2SO4的溶解度由大到小的排列顺序为________ (填字母)。
(4)下列有关Ag2SO4的说法中正确的是________ 。
A.含有大量SO 的溶液中肯定不存在Ag+
的溶液中肯定不存在Ag+
B.Ag2SO4的溶度积常数Ksp=1.6×10-5 (mol·L-1)3
C.0.02 mol·L-1的AgNO3溶液与0.2 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
(5)往Ag2SO4固体中加入足量的Na2CrO4溶液,可观察到砖红色沉淀(Ag2CrO4为砖红色),写出沉淀转化的离子方程式:________ 。

(1)a点表示Ag2SO4
(2)b点对应的Ksp
(3)现将足量的Ag2SO4分别放入:
a.40 mL 0.01 mol·L-1 K2SO4溶液
b.10 mL蒸馏水
c.10 mL 0.02 mol·L-1 H2SO4溶液
则Ag2SO4的溶解度由大到小的排列顺序为
(4)下列有关Ag2SO4的说法中正确的是
A.含有大量SO
 的溶液中肯定不存在Ag+
的溶液中肯定不存在Ag+B.Ag2SO4的溶度积常数Ksp=1.6×10-5 (mol·L-1)3
C.0.02 mol·L-1的AgNO3溶液与0.2 mol·L-1的Na2SO4溶液等体积混合不会生成沉淀
(5)往Ag2SO4固体中加入足量的Na2CrO4溶液,可观察到砖红色沉淀(Ag2CrO4为砖红色),写出沉淀转化的离子方程式:
您最近一年使用:0次
名校
解题方法
3 . 马日夫盐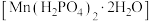 易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为
易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为 ,还含少量的FeO、
,还含少量的FeO、 和
和 )为原料制备马日夫盐的一种工艺流程如图所示:
)为原料制备马日夫盐的一种工艺流程如图所示:
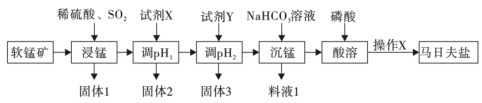
已知常温下,几种离子形成氢氧化物沉淀时,开始沉淀与恰好完全沉淀时的pH如表所示:
回答下列问题:
(1)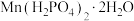 中锰元素的化合价是
中锰元素的化合价是______ 。
(2)浸锰过程中除了 是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式
是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式____________ 。
(3)固体2的主要成分经处理可得到一种用于生产油漆、涂料的物质,该处理方法是__________ ;调 时,
时, 的范围是
的范围是__________ 。
(4)试剂Y不宜为____________ (填字母)。
A.氨水 B. C.
C.
(5)沉锰过程中有一种无色无味气体生成,写出相应反应的离子方程式____________ 。由表中数据可求出常温下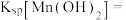
____________ (离子浓度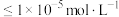 时可认为其沉淀完全)。
时可认为其沉淀完全)。
(6)操作X包括______ 、过滤、洗涤、干燥。马日夫盐可作防锈剂的原因是在防锈处理过程中生成了具有保护作用的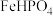 ,处理过程中马日夫盐可转化为
,处理过程中马日夫盐可转化为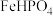 的原理是
的原理是____________ 。
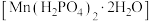 易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为
易溶于水,且水溶液呈酸性,主要用作大型机械设备的防锈剂,也用作各种武器等的润滑层和防护层。以软锰矿(主要成分为 ,还含少量的FeO、
,还含少量的FeO、 和
和 )为原料制备马日夫盐的一种工艺流程如图所示:
)为原料制备马日夫盐的一种工艺流程如图所示:
已知常温下,几种离子形成氢氧化物沉淀时,开始沉淀与恰好完全沉淀时的pH如表所示:
|
|
|
| |
开始沉淀 | 2.7 | 7.6 | 7.7 | 4.0 |
完全沉淀 | 3.2 | 9.6 | 10.0 | 5.2 |
(1)
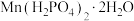 中锰元素的化合价是
中锰元素的化合价是(2)浸锰过程中除了
 是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式
是还原剂外还有一种还原剂,写出该还原剂被氧化的离子方程式(3)固体2的主要成分经处理可得到一种用于生产油漆、涂料的物质,该处理方法是
 时,
时, 的范围是
的范围是(4)试剂Y不宜为
A.氨水 B.
 C.
C.
(5)沉锰过程中有一种无色无味气体生成,写出相应反应的离子方程式
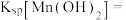
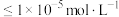 时可认为其沉淀完全)。
时可认为其沉淀完全)。(6)操作X包括
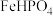 ,处理过程中马日夫盐可转化为
,处理过程中马日夫盐可转化为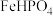 的原理是
的原理是
您最近一年使用:0次
名校
解题方法
4 . 室温时, 在水中的沉淀溶解平衡曲线如图所示。已知
在水中的沉淀溶解平衡曲线如图所示。已知 的溶度积(室温)
的溶度积(室温)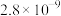 ,下列说法中不正确的是
,下列说法中不正确的是

 在水中的沉淀溶解平衡曲线如图所示。已知
在水中的沉淀溶解平衡曲线如图所示。已知 的溶度积(室温)
的溶度积(室温)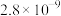 ,下列说法中不正确的是
,下列说法中不正确的是
A. 的数值为 的数值为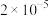 | B. 点时有 点时有 生成 生成 |
C.加入蒸馏水可使溶液由 点变成 点变成 点 点 | D. 点与 点与 点对应的溶度积相等 点对应的溶度积相等 |
您最近一年使用:0次
2022-11-18更新
|
684次组卷
|
38卷引用:陕西省黄陵中学2020-2021学年高二上学期期末考试化学试题
陕西省黄陵中学2020-2021学年高二上学期期末考试化学试题(已下线)2013届陕西省宝鸡市高三第三次模拟理综化学试卷2014-2015陕西省西安市庆安高级中学高二上学期期末化学试卷2014-2015陕西省西安市七十中高二上学期期末考试化学试卷新疆维吾尔自治区喀什区第二中学2020-2021学年高二上学期期末考试化学试题安徽省合肥六校联盟2020-2021学年高二上学期期末联考化学试题河北省石家庄市辛集市第一中学2020-2021学年高二月考第四次考试(一)化学试题江西省抚州市崇仁县第二中学2021-2022学年高二上学期第二次月考化学试题(已下线)2010年浙江江山实验中学高二年级5月月考化学试卷(已下线)2012届浙江省余姚中学高三上学期期中考试化学试卷2015-2016学年广西南宁市二十六中高二下学期期中化学试卷2016-2017学年广西陆川中学高二上9月月考化学卷2016-2017学年辽宁省沈阳铁路中学高二上期中化学试卷2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷2018版化学(苏教版)高考总复习专题八课时跟踪训练--难溶电解质的沉淀溶解平衡黑龙江省牡丹江市第一高级中学2018届高三上学期期中考试化学试题江西省临川实验学校2017-2018学年高二上学期期末质量检测化学试题安徽省滁州市民办高中2017-2018学年高二下学期第一次联考化学试题河北省承德市隆化县存瑞中学2018-2019学年高二上学期第二次质检化学试题广州省广州市石化中学2018-2019学年高二上学期期末考试化学试题山东省德州市陵城区第一中学2019-2020学年高二12月月考化学试题黑龙江省双鸭山市第一中学2020届高三12月月考化学试题江西省新余市分宜中学2019-2020学年高二上学期第二次段考化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编湖南省株洲市第二中学2019-2020学年高二上学期入学考试化学试题山西省朔州市怀仁市第一中学校云东校区2019-2020学年高二下学期期末考试化学试题(已下线)3.4.1 沉淀溶解平衡原理(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)山西省长治市第二中学校2020-2021学年高二上学期第二次月考化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省牡丹江市第二中学2022-2023学年高二上学期期中考试化学试题河北省隆化存瑞中学2022-2023学年高二上学期期中考试化学试题江西省抚州市金溪一中等三校2022-2023年高二上学期第二次联考化学试题辽宁省鞍山市普通高中2022-2023学年高二上学期第三次月考化学试题(已下线)第15讲 沉淀溶解平衡-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)天津市第四十七中学2023-2024学年高二上学期12月月考化学试题
名校
5 . 已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS:Ksp=1.6×10-24。下列说法错误的是
| A.相同温度下,CuS的溶解度小于ZnS的溶解度 |
| B.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
| C.足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最小浓度为1.3×10-35mol/L |
| D.在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
您最近一年使用:0次
2022-09-16更新
|
151次组卷
|
2卷引用:陕西省黄陵中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
6 . 硫化镉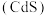 是一种难溶于水的黄色颜料,在水溶液中存在如下溶解平衡:
是一种难溶于水的黄色颜料,在水溶液中存在如下溶解平衡: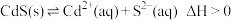 ,其沉淀溶解平衡曲线如图所示。下列说法错误的是
,其沉淀溶解平衡曲线如图所示。下列说法错误的是
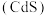 是一种难溶于水的黄色颜料,在水溶液中存在如下溶解平衡:
是一种难溶于水的黄色颜料,在水溶液中存在如下溶解平衡: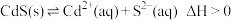 ,其沉淀溶解平衡曲线如图所示。下列说法错误的是
,其沉淀溶解平衡曲线如图所示。下列说法错误的是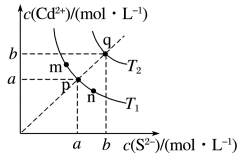
A.图中温度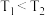 |
B.图中各点对应的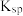 的关系为: 的关系为: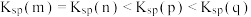 |
C.向m点的溶液中加入少量 固体,溶液组成由m沿 固体,溶液组成由m沿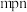 线向p方向移动 线向p方向移动 |
D.温度降低时,q点的饱和溶液的组成由q沿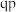 线向p方向移动 线向p方向移动 |
您最近一年使用:0次
2021-09-19更新
|
1603次组卷
|
13卷引用:陕西省洛南县洛南中学2022届高三上学期第一次模拟考试化学试题
陕西省洛南县洛南中学2022届高三上学期第一次模拟考试化学试题(已下线)专题3.4.1 难溶电解质的溶解平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.1 难溶电解质的沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第三章 水溶液中的离子平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)备战2022年高考化学精准检测卷【全国卷】06江西省赣州市教育发展联盟2021-2022学年高二上学期第7次联考化学试题 云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(A卷)(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)云南省曲靖市会泽实验高级中学校2022-2023学年高二下学期3月月考(二)化学试题(已下线)第6讲 沉淀溶解平衡图像分析江西省宜春市宜丰中学2023-2024学年高二上学期10月月考化学试题湖南省邵东市第一中学2023-2024学年高二下学期第一次月考化学试题
名校
解题方法
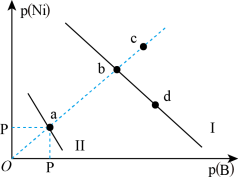
7 . 已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;p(Ni)=-lgc(Ni2+),p(B)=-lgc(S2-)或-lgc(CO )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
 )。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是
| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动 |
| C.对于曲线Ⅰ,在b点加热,b点向c点移动 |
D.P为3.5且对应的阴离子是CO |
您最近一年使用:0次
2021-09-05更新
|
3069次组卷
|
42卷引用:陕西省宝鸡市陈仓区2022届高三上学期第一次教学质量检测化学试题
陕西省宝鸡市陈仓区2022届高三上学期第一次教学质量检测化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)选择性必修1(SJ)专题3专题培优专练选择性必修1 化学反应原理综合训练(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)3.4.2 沉淀溶解平衡原理的应用-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2021年高考全国乙卷化学试题变式题江西省九江市第一中学2021-2022学年高二上学期第二次月考化学试题陕西省汉中中学2021-2022学年高二上学期第四次月考化学试题湖北省宜昌英杰学校2021-2022学年高三上学期10月月考化学试题四川省资阳市高中2018届高三第二次诊断性考试理科综合化学试题西北师大附中2018届下学期高三年级第二次模拟理综化学试卷西藏自治区拉萨中学2018届高三第七次月考理综化学试题【全国市级联考】河北省保定市2018届高三第二次模拟考试理科综合化学试题【全国市级联考】江西省南昌市2018届高三第三次模拟考试理综化学试题【全国百强校】广东省阳春市第一中学2018届高三第九次月考理综化学试题【市级联考】湖北省十堰市2019届高三下学期模拟化学试题四川省泸县第四中学2019届高三下学期三诊模拟理科综合化学试题辽宁省六校协作体2020届高三上学期期中考试化学试题步步为赢 高二化学寒假作业:综合检测(一)福建省厦门外国语学校2020届高三12月月考化学试题2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】吉林省梅河口市第五中学2020届高三下学期模拟考试化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编鲁科版(2019)选择性必修1化学反应原理 综合训练高中必刷题高二选择性必修1化学反应原理综合训练(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第三章 水溶液中的离子平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过素养 学科素养拓展训练人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过素养 学科素养拓展训练山东省临朐县实验中学2020-2021学年高二上学期12月月结学情检测化学试题(已下线)【直击双一流】06-备战2022年高考化学名校进阶模拟卷(通用版)湖南省株洲市第一中学2021-2022学年高三下学期期中考试化学试题吉林省长春市第五中学2022-2023学年高二上学期期中考试化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)T13-溶液中的离子平衡浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题浙江省绍兴区上虞区2022-2023学年高三下学期第二次适应性考试(二模)化学试题
解题方法
8 . 下列离子方程式书写正确的是
A. 沉淀在水中的溶解: 沉淀在水中的溶解: |
B. 的电离: 的电离: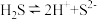 |
C. 的水解: 的水解: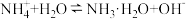 |
D.明矾净水原理: |
您最近一年使用:0次
9 . 化学在生产生活中有着广泛的应用,请回答下列问题:
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化______ (填“能”或“不能”)用勒夏特列原理解释。
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:______ 。
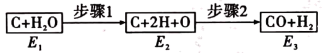
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为______ (填离子符号),再加碱调节至pH为______ 时,铁刚好沉淀完全(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱至pH为6时,锌开始沉淀。若上述过程不加H2O2后果是______ 。(已知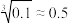 ,lg2
,lg2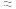 0.3)
0.3)
(1)开启啤酒瓶后瓶中立刻泛起大量泡沫,该变化
(2)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:
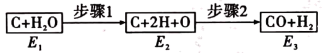
(3)某中学开展劳动实习,学生用废电池的锌皮制备ZnSO4∙7H2O,该过程中需除去锌皮中的少量杂质铁,方法是先加稀H2SO4和H2O2溶解,铁变为
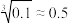 ,lg2
,lg2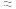 0.3)
0.3)| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp的近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
解题方法
10 . 难溶电解质在水溶液中存在着电离平衡。在常温下,溶液里各种离子的浓度与它们化学计量数的方次的乘积是一个常数,叫溶度积常数(Ksp)。
例如已知:Ksp=c(Cu2+)·c2(OH-)=2×10-20,当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。
(1)请写出Cu(OH)2沉淀溶解平衡表达式_______ 。
(2)某CuSO4溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于_______ (写出计算步骤)。
(3)要使0.2 mol/L CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为_______ (写出计算步骤)。
例如已知:Ksp=c(Cu2+)·c2(OH-)=2×10-20,当溶液中各种离子的浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。
(1)请写出Cu(OH)2沉淀溶解平衡表达式
(2)某CuSO4溶液里c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
(3)要使0.2 mol/L CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为
您最近一年使用:0次







