名校
解题方法
1 .  时,在含有大量
时,在含有大量 的饱和溶液中存在沉淀溶解平衡:
的饱和溶液中存在沉淀溶解平衡: ,加入
,加入 固体,下列说法正确的是
固体,下列说法正确的是
 时,在含有大量
时,在含有大量 的饱和溶液中存在沉淀溶解平衡:
的饱和溶液中存在沉淀溶解平衡: ,加入
,加入 固体,下列说法正确的是
固体,下列说法正确的是A.溶液中 和 和 的浓度都增大 的浓度都增大 |
B.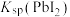 增大 增大 |
C. 的沉淀溶解平衡向右移动 的沉淀溶解平衡向右移动 |
D.溶液中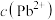 减小 减小 |
您最近一年使用:0次
2023-02-19更新
|
363次组卷
|
17卷引用:北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题
北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题2016-2017学年吉林省吉林二中高二上学期9月月考化学试卷2016-2017学年陕西西安一中高二上月考二化学卷黑龙江省哈尔滨师范大学附属中学2017-2018学年高二上学期期中考试化学试题河北省张家口市2017-2018学年高二12月月考化学试题山西省临汾第一中学等五校2017-2018学年高二上学期期末联考化学试题(已下线)2018年11月18日 《每日一题》人教选修4-每周一测四川省宜宾市第三中学2018-2019学年高二上学期11月月考化学试题福建省长乐高级中学2018-2019学年高二下学期期末考试化学试题(已下线)2019年11月17日《每日一题》人教版(选修4)—— 每周一测新疆维吾尔自治区石河子第二中学2019-2020学年高二上学期第二次月考化学试题黑龙江省哈尔滨市第三十二中学校2021-2022学年高二下学期期中考试化学试题第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡(已下线)3.4 沉淀溶解平衡-同步学习必备知识(已下线)题型139 沉淀溶解平衡及其影响因素(已下线)第15讲 沉淀溶解平衡-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)上海市进才中学2023-2024学年高二上学期1月期末化学试题
名校
2 . 当Mg(OH)2固体在水中溶解达到平衡时:Mg(OH)2 (s)⇌Mg2++2OH- ,为使Mg(OH)2固体的量减少,可加入的物质是
| A.MgSO4 | B.NaOH | C.HCl | D.NaCl |
您最近一年使用:0次
2022-12-04更新
|
646次组卷
|
8卷引用:北京市西城职业学校2021-2021学年高二上学期期中测试化学试题
名校
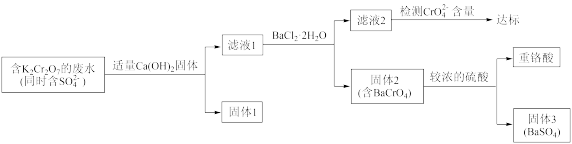
3 . 含有 的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有
的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 的废水并回收重铬酸。处理废水的具体流程如下:
的废水并回收重铬酸。处理废水的具体流程如下:
已知: 、
、 易溶于水,其它几种盐在常温下的溶度积如下表所示
易溶于水,其它几种盐在常温下的溶度积如下表所示
(1)  溶液中同时存在
溶液中同时存在 :
: ,向含
,向含 的废水中加入
的废水中加入 ,该平衡向
,该平衡向___________ 方向移动(填“正反应”或“逆反应”)。
(2)向滤液1中加入 的目的是使
的目的是使 从溶液中沉淀出来。结合表中数据,说明选用
从溶液中沉淀出来。结合表中数据,说明选用 而不选用
而不选用 处理废水的理由:
处理废水的理由:___________ 。
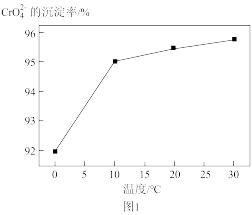
(3)研究温度对 沉淀效率的影响实验结果如下:在相同的时间间隔内,不同温度下
沉淀效率的影响实验结果如下:在相同的时间间隔内,不同温度下 的沉淀率如图1所示。
的沉淀率如图1所示。
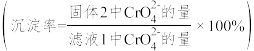
已知: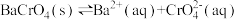
 ,
, 的沉淀效率随温度变化的原因是
的沉淀效率随温度变化的原因是___________ 。
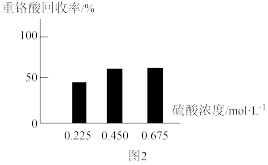
(4)向固体2中加入硫酸,回收重铬酸。硫酸浓度对重铬酸的回收率如图2所示。结合化学平衡移动原理,解释使用 的硫酸时,重铬酸的回收率明显高于使用
的硫酸时,重铬酸的回收率明显高于使用 的硫酸的原因:
的硫酸的原因:___________ 。
(5)综上所述,沉淀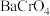 并进一步回收重铬酸的效果与
并进一步回收重铬酸的效果与___________ 有关。
 的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有
的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 的废水并回收重铬酸。处理废水的具体流程如下:
的废水并回收重铬酸。处理废水的具体流程如下:
已知:
 、
、 易溶于水,其它几种盐在常温下的溶度积如下表所示
易溶于水,其它几种盐在常温下的溶度积如下表所示| 物质 |  | 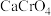 | 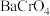 |  |
| 溶度积 | 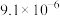 | 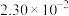 | 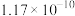 |  |
 溶液中同时存在
溶液中同时存在 :
: ,向含
,向含 的废水中加入
的废水中加入 ,该平衡向
,该平衡向(2)向滤液1中加入
 的目的是使
的目的是使 从溶液中沉淀出来。结合表中数据,说明选用
从溶液中沉淀出来。结合表中数据,说明选用 而不选用
而不选用 处理废水的理由:
处理废水的理由:(3)研究温度对
 沉淀效率的影响实验结果如下:在相同的时间间隔内,不同温度下
沉淀效率的影响实验结果如下:在相同的时间间隔内,不同温度下 的沉淀率如图1所示。
的沉淀率如图1所示。
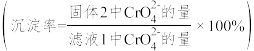
已知:
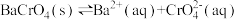
 ,
, 的沉淀效率随温度变化的原因是
的沉淀效率随温度变化的原因是(4)向固体2中加入硫酸,回收重铬酸。硫酸浓度对重铬酸的回收率如图2所示。结合化学平衡移动原理,解释使用
 的硫酸时,重铬酸的回收率明显高于使用
的硫酸时,重铬酸的回收率明显高于使用 的硫酸的原因:
的硫酸的原因:
(5)综上所述,沉淀
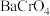 并进一步回收重铬酸的效果与
并进一步回收重铬酸的效果与
您最近一年使用:0次
名校
解题方法
4 . 可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。
(1)室温下,测得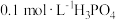 溶液的
溶液的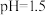 ,用电离方程式解释原因:
,用电离方程式解释原因:___________ 。
(2)羟基磷灰石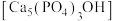 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: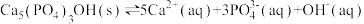 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:___________ 。
(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。
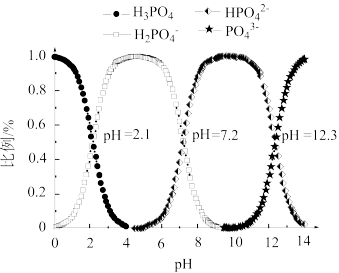
① 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是___________ 。
a.溶液中
b. 的电离程度大于其水解程度
的电离程度大于其水解程度
c.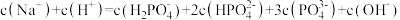
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:___________ 。
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用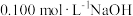 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。
①加热的目的是___________ 。
②该可乐样品中磷酸的含量为___________ g/L。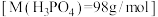
 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。(1)室温下,测得
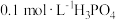 溶液的
溶液的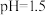 ,用电离方程式解释原因:
,用电离方程式解释原因:(2)羟基磷灰石
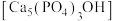 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: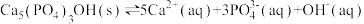 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。

①
 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是a.溶液中

b.
 的电离程度大于其水解程度
的电离程度大于其水解程度c.
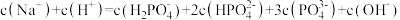
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用
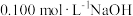 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。①加热的目的是
②该可乐样品中磷酸的含量为
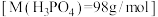
您最近一年使用:0次
名校
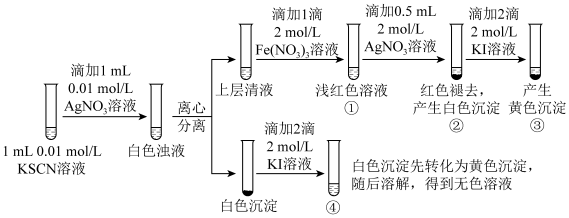
5 . 已知: (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,不正确 的是
 (白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。
下列说法中,
A.①中现象能说明 与 与 生成的白色浊液中存在沉淀溶解平衡 生成的白色浊液中存在沉淀溶解平衡 |
B.②中现象产生的原因是发生了反应: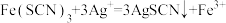 |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的 进一步发生了反应 进一步发生了反应 |
您最近一年使用:0次
2021-11-15更新
|
697次组卷
|
3卷引用:北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题
北京市北师大附属实验中学2021-2022学年高二上学期期中考试化学试题辽宁省大连市第八中学2021-2022学年高三上学期12月月考化学试题(已下线)第21讲 难溶电解质的沉淀溶解平衡(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
6 . 实验:①向盛有1mL0.1mol/LMgCl2溶液试管中加1mL0.3mol/LNaOH溶液,得到浊液a,过滤得到滤液b和白色沉淀c。②向沉淀c中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色,下列分析不正确 的是
A.浊液a中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
| B.滤液b中加入上述FeCl3溶液有红褐色沉淀生成,证明Fe(OH)3比Mg(OH)2更难溶 |
| C.②中颜色变化说明Mg(OH)2转化为Fe(OH)3 |
| D.实验②可以证明Fe(OH)3比Mg(OH)2更难溶 |
您最近一年使用:0次
名校
7 . 甲、乙两物质的溶解度曲线如图所示,下列说法不正确的是
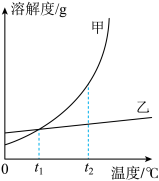

| A.甲溶于水,一定明显放热 |
B. ℃时,甲、乙的溶解度相同 ℃时,甲、乙的溶解度相同 |
C.分别将等质量的甲、乙饱和溶液从 ℃降至 ℃降至 ℃,析出固体(不含结晶水)的质量甲一定多于乙 ℃,析出固体(不含结晶水)的质量甲一定多于乙 |
| D.从甲的溶液中(含少量杂质)将甲固体结晶的操作为:加热浓缩、冷却结晶 |
您最近一年使用:0次
解题方法
8 . 室温下向100mL蒸馏水中加入1gCaCO3,一段时间后再向其中加入10mL蒸馏水,一段时间后继续加入10mL蒸馏水。该过程中电导率的变化如下图:
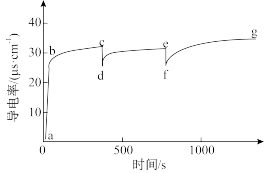
已知:室温下,CaCO3的溶解度为0.0013g。
下列说法不正确 的是

已知:室温下,CaCO3的溶解度为0.0013g。
下列说法
| A.a→b电导率上升是由于CaCO3固体部分溶解于水中 |
| B.c和e对应的时刻分别加入了10mL蒸馏水 |
| C.c→d、e→f,电导率下降,说明CaCO3的溶解平衡逆向移动 |
| D.g后的电导率几乎不再改变,说明CaCO3的溶解达到平衡状态 |
您最近一年使用:0次
2021-05-10更新
|
1098次组卷
|
8卷引用:北京市西城区2021届高三化学第二次模拟考试
北京市西城区2021届高三化学第二次模拟考试(已下线)2021年高考化学押题预测卷(北京卷)(02)北京市师范大学亚太实验学校2021-2022学年高二上学期期中考试化学试题广东省华附、省实、广雅、深中四校2020-2021学年高二下学期期末联考化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)3.4.1 沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)第八章 水溶液中的离子反应与平衡 第52讲 难溶电解质的溶解平衡
名校
9 . 具有十八面体结构的Ag3PO4晶体是一种高效光催化剂,可用于实现“碳中和”,也可用于降解有机污染物。
Ⅰ.配位-沉淀法制备 高效光催化剂
高效光催化剂

已知:i.Ag3PO4难溶于水,可溶于硝酸;
ii.Ag3PO4沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
iii.银氨溶液中存在: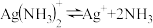
(1)配制银氨溶液时的反应现象是___________ 。
(2)加入 溶液时,发生以下反应,请将离子方程式补充完整:
溶液时,发生以下反应,请将离子方程式补充完整:
□ +□ +□ =□NH3+□ +□
+□ +□ =□NH3+□ +□ ___________
(3) 和
和 在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:
在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:___________ 。
Ⅱ.Ag3PO4光催化剂的使用和再生
已知:Ag3PO4晶体在光照条件下发挥催化作用时,首先引发反应。a.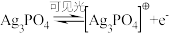
(4)Ag3PO4光催化CO2制备甲醇可实现“碳中和”,a的后续反应: ,
,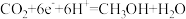 ,则由CO2制备甲醇的总反应的化学方程式为
,则由CO2制备甲醇的总反应的化学方程式为___________ 。
(5)Ag3PO4光催化降解RhB(代表有机污染物),RhB被氧化成CO2和H2O。a的后续反应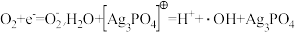
注:Ag3PO4在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
用Ag3PO4依次降解三份相同的废水,测得3次降解过程中RhB的残留率(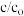 :即时浓度与起始浓度之比)随时间变化的曲线如图。
:即时浓度与起始浓度之比)随时间变化的曲线如图。

①下列说法正确的是___________ (填字母序号)。
a. 和
和 是降解RhB的重要氧化剂
是降解RhB的重要氧化剂
b.第1次使用后Ag3PO4的光催化性能降低
c.该实验条件下,Ag3PO4使用两次即基本失效
②第1次光降解时,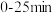 内的反应速率为
内的反应速率为___________ 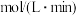 (废水中RhB初始浓度
(废水中RhB初始浓度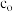 为
为 ,RhB的摩尔质量为
,RhB的摩尔质量为 )
)
Ⅰ.配位-沉淀法制备
 高效光催化剂
高效光催化剂
已知:i.Ag3PO4难溶于水,可溶于硝酸;
ii.Ag3PO4沉淀的生成速率会影响其结构和形貌,从而影响其光催化性能;
iii.银氨溶液中存在:
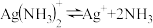
(1)配制银氨溶液时的反应现象是
(2)加入
 溶液时,发生以下反应,请将离子方程式补充完整:
溶液时,发生以下反应,请将离子方程式补充完整:□
 +□ +□ =□NH3+□ +□
+□ +□ =□NH3+□ +□ (3)
 和
和 在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:
在溶液中反应也可制得Ag3PO4固体,但制得的Ag3PO4固体光催化性能极差。从速率角度解释其原因:Ⅱ.Ag3PO4光催化剂的使用和再生
已知:Ag3PO4晶体在光照条件下发挥催化作用时,首先引发反应。a.
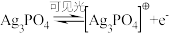
(4)Ag3PO4光催化CO2制备甲醇可实现“碳中和”,a的后续反应:
 ,
,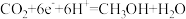 ,则由CO2制备甲醇的总反应的化学方程式为
,则由CO2制备甲醇的总反应的化学方程式为(5)Ag3PO4光催化降解RhB(代表有机污染物),RhB被氧化成CO2和H2O。a的后续反应
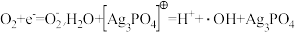
注:Ag3PO4在该催化过程中可能发生光腐蚀,生成单质银,影响其光催化性能。
用Ag3PO4依次降解三份相同的废水,测得3次降解过程中RhB的残留率(
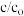 :即时浓度与起始浓度之比)随时间变化的曲线如图。
:即时浓度与起始浓度之比)随时间变化的曲线如图。
①下列说法正确的是
a.
 和
和 是降解RhB的重要氧化剂
是降解RhB的重要氧化剂b.第1次使用后Ag3PO4的光催化性能降低
c.该实验条件下,Ag3PO4使用两次即基本失效
②第1次光降解时,
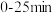 内的反应速率为
内的反应速率为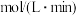 (废水中RhB初始浓度
(废水中RhB初始浓度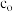 为
为 ,RhB的摩尔质量为
,RhB的摩尔质量为 )
)
您最近一年使用:0次
2021-05-10更新
|
561次组卷
|
3卷引用:北京市海淀区2021届高三二模化学试题
10 . 某品牌牙膏的成分含水、丙三醇、二氧化硅、苯甲酸钠、十二烷基硫酸钠和氟化钠等。已知:牙釉质中含有羟基磷酸钙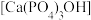 ,是牙齿的保护层。在牙齿表面存在平衡:
,是牙齿的保护层。在牙齿表面存在平衡:

下列说法不正确 的是
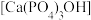 ,是牙齿的保护层。在牙齿表面存在平衡:
,是牙齿的保护层。在牙齿表面存在平衡:

下列说法
| A.若使牙膏呈弱酸性,更有利于保护牙釉质 |
| B.丙三醇的俗称是甘油 |
C. 是摩擦剂,有助于去除牙齿表面的污垢 是摩擦剂,有助于去除牙齿表面的污垢 |
D.NaF能将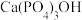 转化为更难溶的 转化为更难溶的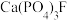 ,减少龋齿的发生 ,减少龋齿的发生 |
您最近一年使用:0次



