1 . 自然界中原生铜的硫化物经氧化、淋滤后变成CuSO4溶液,遇到闪锌矿(ZnS)可慢慢转变为铜蓝(CuS)。已知: Ksp(ZnS)=2 ×10-22, Ksp(CuS)=6 ×10-36。下列说法正确的是

| A.Cu2+基态核外电子排布式为[Ar]3d84s1 |
B.反应ZnS(s)+Cu2+(ag)  CuS(s)+Zn2+(aq)正向进行,需满足 CuS(s)+Zn2+(aq)正向进行,需满足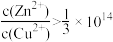 |
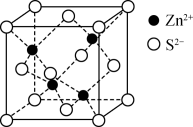
| C.ZnS 晶胞(见如图)中S2-的配位数为4 |
D.生成铜蓝后的溶液中一定存在: c(S2-)=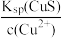 且c(S2- )> 且c(S2- )> 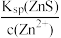 |
您最近一年使用:0次
名校
2 . 已知:①AgCl为难溶于水和酸的白色固体,Ag2S为难溶于水和酸的黑色固体。
②室温下,Ksp(AgCl)=2.0×10-10,Ksp(Ag2S)=2.0×10-48。
向AgCl的悬浊液中加入一定量的Na2S溶液并振荡,白色固体向黑色固体转化。下列说法正确的是
②室温下,Ksp(AgCl)=2.0×10-10,Ksp(Ag2S)=2.0×10-48。
向AgCl的悬浊液中加入一定量的Na2S溶液并振荡,白色固体向黑色固体转化。下列说法正确的是
| A.Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+2c(S2-) |
| B.向AgCl悬浊液加入足量氨水,溶液变澄清。反应的离子方程式为:AgCl+4NH3•H2O=[Ag(NH3)4]++Cl-+4H2O |
C.反应2AgCl+S2- Ag2S+2Cl-正向进行,需满足 Ag2S+2Cl-正向进行,需满足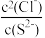 <2×1028 <2×1028 |
D.将转化后的体系静置,上层清液中离子存在关系:c(Ag+)=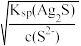 且c(Ag+)> 且c(Ag+)>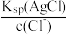 |
您最近一年使用:0次
2021-12-27更新
|
434次组卷
|
5卷引用:江苏省高邮市2021-2022学年高三上学期12月学情调研化学试题
江苏省高邮市2021-2022学年高三上学期12月学情调研化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)天津市耀华中学2022-2023学年高三上学期统练三 化学试题
名校
3 . 下列有关说法正确的是
A. 溶液中: 溶液中: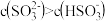 |
B.常温下,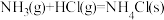 能自发的原因是 能自发的原因是 |
C.已知: ,保持温度不变,增大压强, ,保持温度不变,增大压强, 的浓度减小 的浓度减小 |
D.向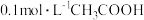 溶液中加适量水,导致溶液中 溶液中加适量水,导致溶液中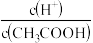 减小 减小 |
您最近一年使用:0次
2021-12-25更新
|
299次组卷
|
2卷引用:江苏省昆山市七校2021-2022学年高二上学期12月联考化学试题
4 . 室温下,通过下列实验探究NaHSO3溶液的性质:
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定某NaHSO3溶液的pH,测得pH约为6 |
| 2 | 向某NaHSO3溶液中加入过量的Ba(OH)2溶液,产生白色沉淀 |
| 3 | 向某NaHSO3溶液中加入等体积等浓度的烧碱溶液,测得溶液pH约为9 |
| 4 | 向某苏打溶液中滴加几滴NaHSO3溶液,未观察到明显实验现象 |
A.NaHSO3溶液中存在c(OH-)=c(H+)-c(SO )+c(HSO )+c(HSO ) ) |
B.实验2反应静置后的上层清液中有c(Ba2+)×c(SO )>Ksp(BaSO3) )>Ksp(BaSO3) |
C.实验3得到的溶液中有c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
D.实验4中反应的离子方程式为CO +HSO +HSO =HCO =HCO +SO +SO |
您最近一年使用:0次
名校
5 . CuCl为白色粉末,微溶于水,溶于浓盐酸或NaCl浓溶液,不溶于乙醇。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如图:
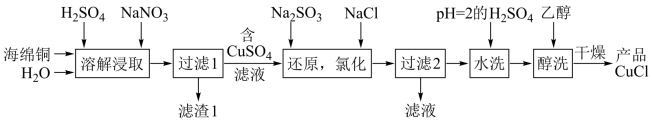
(1)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图1、图2所示。
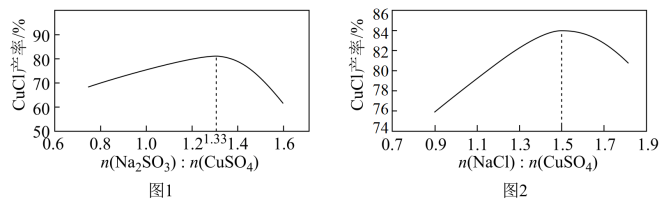
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为___ 。
②当n(Na2SO3):n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是___ 。
③当1.0<n(NaCl):n(CuSO4)<1.5时,比值越大CuCl产率越大,结合沉淀平衡移动原理分析其原因是___ 。
(2)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为___ 。
(3)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液bmL,反应中Cr2O 被还原为Cr3+,求样品中CuCl的质量分数
被还原为Cr3+,求样品中CuCl的质量分数___ (写计算过程)。

(1)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图1、图2所示。

①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为
②当n(Na2SO3):n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是
③当1.0<n(NaCl):n(CuSO4)<1.5时,比值越大CuCl产率越大,结合沉淀平衡移动原理分析其原因是
(2)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为
(3)为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液bmL,反应中Cr2O
 被还原为Cr3+,求样品中CuCl的质量分数
被还原为Cr3+,求样品中CuCl的质量分数
您最近一年使用:0次
2021-12-22更新
|
738次组卷
|
7卷引用:江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题
江苏省前黄高级中学、如东中学、姜堰中学2021-2022学年高三上学期12月份阶段性测试化学试题江苏省姜堰中学、如东中学、前黄中学三校2021- 2022学年高三联考化学试题(已下线)黄金卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省徐州市第七中学2021-2022学年高三下学期2月检测化学试题(已下线)2022年江苏卷高考真题变式题14-17(已下线)江苏省2022年普通高中学业水平选择性考试变式题(实验探究题)湖南省益阳市第一中学2021-2022学年高二下学期期末考试化学试题
6 . 砷(As)是一些工厂和矿山废水中的污染元素,其剧毒、难降解且易生物聚集的特点极大的威胁了水环境安全和人体健康。天然水体中砷元素主要以As(III)和As(V)存在,且As(III)的毒性更大。常见除砷的方法有沉淀法、氧化絮凝法和离子交换法等。
(1)沉淀法除砷:砷酸盐的溶解度小,工业上需要将废水中和至pH>12,再用氧化剂将As(III)转化成As(V),然后用石灰乳沉淀除砷,得到Ca5(AsO4)3OH沉淀。“沉砷”的最佳温度控制在80~85℃的原因是_______ 。
(2)高铁酸盐氧化絮凝法除砷。
已知:a.As(III)和As(V)水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图所示。
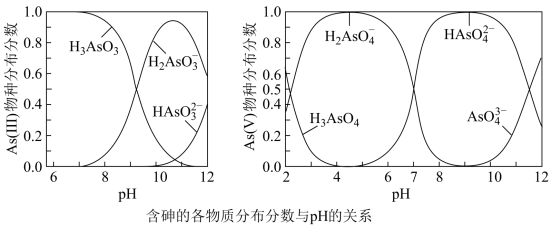
b.高铁酸钾易溶于水,具有强氧化性;溶液酸性越强,其氧化性越强;在pH<1的酸性条件下质子化,主要以HFeO 形式存在。
形式存在。
c.高铁酸钾在一定pH范围的水溶液中易生成Fe(OH)3胶体,溶液的pH对胶体粒子表面所带电荷有影响。pH=7.1时,胶体粒子表面不带电荷;pH>7.1时,胶体粒子表面带负电荷,pH越高,表面所带负电荷越多;pH<7.1时,胶体粒子表面带正电荷,pH越低,表面所带正电荷越多。
①pH<1时,HFeO 将As(III)氧化为As(V)的离子方程式为
将As(III)氧化为As(V)的离子方程式为_______ 。
②在一定pH范围内,K2FeO4的还原产物可形成Fe(OH)3胶体,吸附As(V)的离子达到除砷目的;不同pH对K2FeO4氧化絮凝除砷影响如图所示。除砷过程中控制废水pH为4~7,pH过低或过高,砷的去除率都下降,其原因是_______ 。
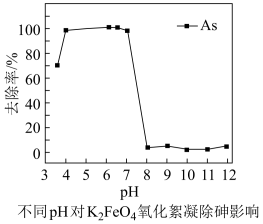
(3)离子交换法除砷:强碱性离子交换树脂上的OH与废水中的H2AsO 、HAsO
、HAsO 、AsO
、AsO 进行离子交换,OH-进入水中,H2AsO
进行离子交换,OH-进入水中,H2AsO 、HAsO
、HAsO 、AsO
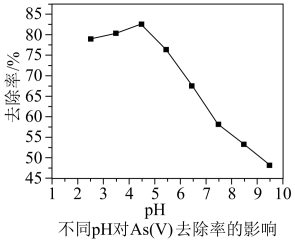
、AsO 被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是
被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是_______ 。
(1)沉淀法除砷:砷酸盐的溶解度小,工业上需要将废水中和至pH>12,再用氧化剂将As(III)转化成As(V),然后用石灰乳沉淀除砷,得到Ca5(AsO4)3OH沉淀。“沉砷”的最佳温度控制在80~85℃的原因是
(2)高铁酸盐氧化絮凝法除砷。
已知:a.As(III)和As(V)水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系分别如题图所示。

b.高铁酸钾易溶于水,具有强氧化性;溶液酸性越强,其氧化性越强;在pH<1的酸性条件下质子化,主要以HFeO
 形式存在。
形式存在。c.高铁酸钾在一定pH范围的水溶液中易生成Fe(OH)3胶体,溶液的pH对胶体粒子表面所带电荷有影响。pH=7.1时,胶体粒子表面不带电荷;pH>7.1时,胶体粒子表面带负电荷,pH越高,表面所带负电荷越多;pH<7.1时,胶体粒子表面带正电荷,pH越低,表面所带正电荷越多。
①pH<1时,HFeO
 将As(III)氧化为As(V)的离子方程式为
将As(III)氧化为As(V)的离子方程式为②在一定pH范围内,K2FeO4的还原产物可形成Fe(OH)3胶体,吸附As(V)的离子达到除砷目的;不同pH对K2FeO4氧化絮凝除砷影响如图所示。除砷过程中控制废水pH为4~7,pH过低或过高,砷的去除率都下降,其原因是

(3)离子交换法除砷:强碱性离子交换树脂上的OH与废水中的H2AsO
 、HAsO
、HAsO 、AsO
、AsO 进行离子交换,OH-进入水中,H2AsO
进行离子交换,OH-进入水中,H2AsO 、HAsO
、HAsO 、AsO
、AsO 被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是
被树脂固定以达到除As(V)目的;不同pH对As(V)去除率的影响如图所示。结合As(V)在水溶液中的存在形态与pH的关系和OH-的交换效率分析,pH=4.5时去除率最高的原因是
您最近一年使用:0次
7 . 某科研课题小组研究利用含H+、Na+、Zn2+、Mn2+、Fe2+、Fe3+、SO 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
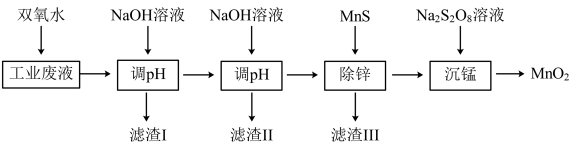
回答下列问题:
(1)加入双氧水的目的是___ 。
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程___ 。
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
为防止Mn2+同时沉淀造成产品不纯,最终选择将溶液的pH控制为7,则此时溶液中Zn2+的沉淀率为___ ,利用滤渣Ⅱ制备高纯的ZnO时,必然含有极其微量的___ (以化学式表示)。
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq) ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=___ 。(填数值)
(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式___ 。
 的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
的工业废电解质溶液,制备高纯的ZnO、MnO2、Fe2O3,设计实验流程如图:
回答下列问题:
(1)加入双氧水的目的是
(2)第一次调pH使Fe3+完全沉淀,写出反应的离子方程
(3)第二次调pH前,科研小组成员分析此时的溶液,得到常温下相关数据如表(表中金属离子沉淀完全时,其浓度为1×10-5mol·L-1)。
| 浓度/(mol·L-1) | 氢氧化物的Ksp | 开始沉淀的pH | 沉淀完全的pH | |
| Zn2+ | 0.12 | 1.2×10-17 | 6.0 | 8.1 |
| Mn2+ | 0.10 | 4.0×10-14 | 7.8 | 9.8 |
(4)已知常温下,Ksp(MnS)=3.0×10-14,Ksp(ZnS)=1.5×10-24,在除锌时发生沉淀转化反应为:MnS(s)+Zn2+(aq)
 ZnS(s)+Mn2+(aq),其平衡常数K=
ZnS(s)+Mn2+(aq),其平衡常数K=(5)沉锰反应在酸性条件下完成,写出该反应的离子方程式
您最近一年使用:0次
名校
8 . 某兴趣小组进行下列实验:
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
①将0.1 mol·L-1 MgCl2溶液和0.5 mol·L-1 NaOH溶液等体积混合得到浊液
②取少量①中浊液,滴加0.1 mol·L-1 FeCl3溶液,出现红褐色沉淀
③将①中浊液过滤,取少量白色沉淀,滴加0.1 mol·L-1 FeCl3溶液,白色沉淀变为红褐色沉淀
④另取少量白色沉淀,滴加饱和NH4Cl溶液,沉淀溶解
下列说法中不正确的是
| A.将①中所得浊液过滤,所得滤液中含少量Mg2+ |
| B.①中浊液中存在沉淀溶解平衡: Mg(OH)2(s)⇌ Mg2+(aq)+2OH-(aq) |
| C.实验②和③均能说明Fe(OH)3比Mg(OH)2难溶 |
D.NH4Cl溶液中的NH 可能是④中沉淀溶解的原因 可能是④中沉淀溶解的原因 |
您最近一年使用:0次
2021-08-10更新
|
974次组卷
|
11卷引用:江苏省扬州中学2021-2022学年上学期高二12月月考化学试题
江苏省扬州中学2021-2022学年上学期高二12月月考化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.1 沉淀溶解平衡原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)河北省石家庄市正中实验中学东校区2022-2023学年高二上学期10月月考化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡作业(二十一) 沉淀溶解平衡的应用
名校
解题方法
9 . 室温下BaSO4沉淀溶解平衡曲线如图,下列结论正确的是
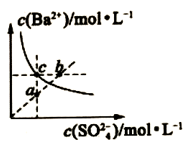
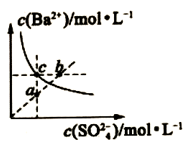
| A.b点无BaSO4沉淀生成 | B.蒸发可使溶液由a点到c点 |
| C.曲线上任意点的Ksp相同 | D.向a点加入BaCl2固体,溶液可达b点 |
您最近一年使用:0次
2021-06-29更新
|
394次组卷
|
5卷引用:江苏省宿迁市2020-2021学年高二下学期期末考试化学试题
江苏省宿迁市2020-2021学年高二下学期期末考试化学试题江苏省宿迁市沭阳县2020-2021学年高二下学期期末调研测试化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)(已下线)3.4.1 沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版选修4)安徽省亳州市第一中学2021-2022学年高二上学期第二次月考化学试题
名校
10 . 下列有关海水中提取镁的说法不正确的是
| A.得到Mg(OH)2沉淀的化学反应方程式为Ca(OH)2 +MgCl2=Mg(OH)2↓+CaCl2 |
B.加入盐酸,Mg(OH)2(s)  Mg2+(aq)+2OH-(aq)平衡正向移动 Mg2+(aq)+2OH-(aq)平衡正向移动 |
| C.在空气中加热灼烧MgCl2·6H2O可得到无水氯化镁 |
| D.电解熔融氯化镁时金属镁在阴极析出 |
您最近一年使用:0次



