解题方法
1 . 下列实验不能达到实验目的的是()
| A | B | C | D |
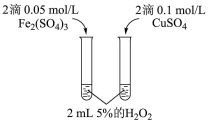 |  |  |  |
| 研究阳离子对H2O2分解速率的影响 | 研究沉淀的转化 | 研究酸碱性对平衡移动的影响 | 研究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 25 ℃时,在氢氧化镁悬浊液中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+2OH-(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。下列说法错误的是
Mg2+(aq)+2OH-(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。下列说法错误的是
 Mg2+(aq)+2OH-(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。下列说法错误的是
Mg2+(aq)+2OH-(aq),已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。下列说法错误的是| A.若向Mg(OH)2浊液中加入少量NH4Cl(s),c(Mg2+)会增大 |
| B.若向Mg(OH)2浊液中加入适量蒸馏水,Ksp保持不变,故上述平衡不发生移动 |
| C.若向Mg(OH)2浊液中滴加CuSO4溶液,沉淀将由白色逐渐变为蓝色 |
| D.若向Mg(OH)2浊液中加入少量Na2CO3(s),固体质量将增大 |
您最近一年使用:0次
2020-05-18更新
|
286次组卷
|
12卷引用:江西省宜春市丰城中学2022-2023学年高二上学期期末考试化学试题
江西省宜春市丰城中学2022-2023学年高二上学期期末考试化学试题苏教版高三单元精练检测八化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高二(普通班)上学期期末考试化学试题吉林省四平市双辽市第二中学2019-2020学年高二上学期期末考试化学试题山西省太原市山西省实验中学2019-2020学年高二上学期12月月考化学试题广西南宁市第三中学2019-2020学年高二下学期期中段考化学试题四川省成都市郫都区川科外国语学校2020-2021学年高二11月月考化学试题广西桂林市第十八中学2020-2021学年高二下学期期中考试化学试题吉林省抚松县第一中学2021-2022学年高二上学期第三次月考化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡新疆实验中学2023-2024学年高二上学期期中考试化学试题
3 . 25℃时,在Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[-1g(M2+)]与溶液pH的变化关系如图所示,已知该温度下Ksp[Cu(OH)2]<Ksp[Fe(OH)2]。
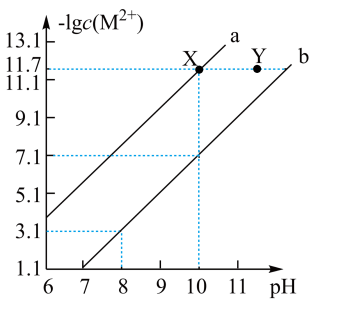
下列说法正确的是 ( )

下列说法正确的是 ( )
| A.向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液 |
| B.b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1(mol/L)3 |
| C.当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:c(Fe2+):c(Cu2+)=1:104.6 |
| D.除去CuSO4溶液中含有的少量Fe2+,可加入适量CuO |
您最近一年使用:0次
2020-04-27更新
|
505次组卷
|
12卷引用:江西省上高县第二中学2018届高三第七次月考理科综合-化学试题
江西省上高县第二中学2018届高三第七次月考理科综合-化学试题黑龙江省哈尔滨市第六中学2017届高三下学期第三次模拟考试理科综合化学试题河南省南阳市第一中学2017-2018学年高二上学期第三次月考化学试题辽宁省大连市旅顺口区2020届高三上学期期中考试化学试题山东省实验中学2020届高三上学期第二次诊断考试化学试题山东省枣庄市2020届高三上学期期末考试化学试题河北省衡水市枣强中学2019-2020学年高二下学期第一次月考化学试题(已下线)考点13 沉淀溶解平衡-2020年高考化学命题预测与模拟试题分类精编河北省张家口宣化一中2021届高三上学期期末考试化学试题黑龙江省大庆铁人中学2021届高三下学期5月第三次模拟考试理综化学试题(已下线)模块十 水溶液中的离子平衡(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)
真题
名校
4 . 下列有关电解质溶液的说法正确的是
A.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中 减小 减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向盐酸中加入氨水至中性,溶液中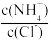 >1 >1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中 不变 不变 |
您最近一年使用:0次
2020-04-02更新
|
5596次组卷
|
44卷引用:江西省宜春市丰城市第九中学2023-2024学年高一下学期第一次月考化学试题(日新班)
江西省宜春市丰城市第九中学2023-2024学年高一下学期第一次月考化学试题(日新班)2016年全国普通高等学校招生统一考试化学(新课标3卷精编版)2017届四川省龙泉中学、温江中学等五校高三上第一次联考化学卷2017届四川省成都七中高三上学期10月阶段测化学卷2017届湖北省荆州中学高三上第四次质检化学试卷河北省邯郸市(大名县、永年区、磁县、邯山区)四县2016-2017学年高二下学期期中联考化学试题湖北省荆州中学2018届高三第二次月考化学试题福建省福州市2016-2017学年高二上学期期中考试化学试题安徽省淮北市第一中学2017-2018学年高二上学期第四次月考(12月)化学试题河南省中原名校(即豫南九校)2017-2018学年高二上学期第二次联考化学试题天津市和平区2017-2018学年高二上学期期末考试化学试题天津市静海县第一中学2017-2018学年高二上学期期末终结性检测化学试题江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题(已下线)《考前20天终极攻略》6月1日 专项一 四大平衡常数及其应用内蒙古北京八中乌兰察布分校2017-2018学年高二下学期第二次调研考试化学试题【全国校级联考】内蒙古赤峰市重点高中(赤峰二中,平煤高级中学等)2017-2018学年高二下学期期末联考(A)化学试题(已下线)解密13 沉淀溶解平衡——备战2018年高考化学之高频考点解密广东省蓝精灵中学2018-2019学年高二上学期联考化学试题四川省成都市七中实验学校2019届高三上学期10月月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)上学期期中考试化学试题吉林省松原市扶余市第一中学2018-2019学年高二上学期期末考试化学试题【全国百强校】内蒙古自治区鄂尔多斯市第一中学2018-2019学年高二下学期开学考试化学试题2016年全国普通高等学校招生统一考试化学(全国3卷参考版)云南省马关县二中2020届高三上学期开学考试化学试题河北省秦皇岛市六校2020届高三上学期期初检测联考化学试题天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题陕西省榆林市第二中学2019-2020学年高二上学期期中考试化学试题(已下线)专题8.3 盐类水解(练)-《2020年高考一轮复习讲练测》北京市2019—2020学年高二上学期期末考试模拟试题(选修4人教版 )2019—2020学年高二上学期化学期末复习—选择题专题训练一西藏自治区日喀则市南木林高级中学2020届高三上学期第四次月考理综化学试题重庆市云阳江口中学校2019-2020学年高二上学期第二次月考化学试题江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 水解平衡常数的应用(强化练习)重庆市江北中学2019-2020学年高二上学期期末模拟考试化学试题河南省南阳市2019-2020学年高二上学期期终质量评估化学试题安徽省黄山市2019-2020学年高二上学期期末质量检测 化学(理)试题(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题江西省抚州市金溪县第一中学2020-2021学年高二上学期第二次月考化学试题河北省安平中学2019-2020学年高二上学期第四次月考化学试题(已下线)3.3.2 影响盐类水解的因素-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)陕西省西安市长安区第一中学2017-2018学年高二上学期第四次教学质量检测化学试题江西省抚州市金溪县第一中学2021-2022学年高二下学期第二次月考化学试题
名校
解题方法
5 . 某常见金属的结晶水化合物MCl3·6H2O有如下转化关系:下列推断正确的是( )


| A.固体1一定是既能与盐酸反应,又能与强碱反应 |
| B.气体1通过五水硫酸铜晶体,固体变蓝色 |
| C.常温下,溶液2能溶解铜 |
| D.固体2浊液中滴加Na2S溶液,白色固体变黄色 |
您最近一年使用:0次
2020-03-06更新
|
188次组卷
|
2卷引用:江西省奉新县第一中学2021届高三上学期第一次月考化学试题
名校
6 . 已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
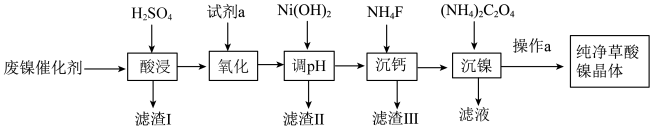
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:______________ 。
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:_____________ 。
(3)“调pH”时pH的调控范围为__________________ 。
(4)写出“沉镍”时发生反应的离子方程式:__________ ,当Ca2+沉淀完全时,溶液中 c(F-)>________ mol·L-1(写出计算式即可)。
(5)操作a的内容是____________________ 。

已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)请写出一种能提高“酸浸”速率的措施:
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式:
(3)“调pH”时pH的调控范围为
(4)写出“沉镍”时发生反应的离子方程式:
(5)操作a的内容是
您最近一年使用:0次
名校
7 . 以下实验操作方法以及结论错误的是( )
①用燃烧的方法鉴别乙醇、四氯化碳、苯
②欲证明CH2=CHCHO中含有碳碳双键,滴入酸性KMnO4溶液,看紫红色是否褪去
③欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸、氢氧化钠、酸碱指示剂。
④向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则 Ksp(BaCO3)﹤Ksp(BaSO4)
⑤油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油分离
⑥检验溴乙烷中的溴元素,将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,再滴加AgNO3溶液
⑦用足量的NaOH溶液与矿物油和地沟油加热,可鉴别出地沟油。
①用燃烧的方法鉴别乙醇、四氯化碳、苯
②欲证明CH2=CHCHO中含有碳碳双键,滴入酸性KMnO4溶液,看紫红色是否褪去
③欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸、氢氧化钠、酸碱指示剂。
④向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,则 Ksp(BaCO3)﹤Ksp(BaSO4)
⑤油脂皂化后可用渗析的方法使高级脂肪酸钠和甘油分离
⑥检验溴乙烷中的溴元素,将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,再滴加AgNO3溶液
⑦用足量的NaOH溶液与矿物油和地沟油加热,可鉴别出地沟油。
| A.②③④⑤⑥ | B.①②⑥⑦ | C.③④⑤⑥ | D.②④⑤⑥ |
您最近一年使用:0次
名校
解题方法
8 . 下列图示与对应的叙述相符的是( )


| A.图1中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性 |
| B.用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图2曲线,可确定首先沉淀的是Cl- |
C.图3表示在N2(g)+3H2(g)  2NH3(g)达到平衡后,减小NH3浓度时速率的变化 2NH3(g)达到平衡后,减小NH3浓度时速率的变化 |
| D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+) |
您最近一年使用:0次
12-13高二下·江西抚州·期末
名校
9 . 如表为有关化合物的pKsp,pKsp=-lgKsp。某同学设计实验如下:①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX;②向①中加NaY,则沉淀转化为AgY;③向②中加入NaZ,沉淀又转化为AgZ。则表中a、b、c的大小关系为
| 相关化合物 | AgX | AgY | AgZ |
| pKsp | a | b | c |
| A.a>b>c | B.a<b<c | C.c<a<b | D.a+b=c |
您最近一年使用:0次
2020-01-16更新
|
486次组卷
|
7卷引用:江西省上高县第二中学2017-2018学年高二上学期期末考试化学试题
江西省上高县第二中学2017-2018学年高二上学期期末考试化学试题(已下线)2012-2013学年江西省抚州市高二下学期期末考试化学试卷广东省中山市第一中学2017-2018学年高二上学期第三次统测化学试题江西省南昌市进贤一中2019-2020学年高二上学期期末考试化学试题宁夏银川市宁夏大学附属中学2019-2020学年高二下学期期末考试化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二上学期期末考试化学试题(已下线)第5讲 难溶电解质的溶解平衡
10 . 已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3主要:Cu2++ +H2O=Cu(OH)2↓+CO2↑ 次要:Cu2++
+H2O=Cu(OH)2↓+CO2↑ 次要:Cu2++ =CuCO3↓
=CuCO3↓
(2)CuSO4+Na2S主要:Cu2++S2-=CuS↓ 次要:Cu2++S2-+2H2O=Cu(OH)2↓+H2S↑
下列几种物质的溶解度大小的比较中,正确的是( )
(1)CuSO4+Na2CO3主要:Cu2++
 +H2O=Cu(OH)2↓+CO2↑ 次要:Cu2++
+H2O=Cu(OH)2↓+CO2↑ 次要:Cu2++ =CuCO3↓
=CuCO3↓(2)CuSO4+Na2S主要:Cu2++S2-=CuS↓ 次要:Cu2++S2-+2H2O=Cu(OH)2↓+H2S↑
下列几种物质的溶解度大小的比较中,正确的是( )
| A.Cu(OH)2>CuCO3>CuS | B.CuS>Cu(OH)2>CuCO3 |
| C.CuS<Cu(OH)2<CuCO3 | D.Cu(OH)2<CuCO3<CuS |
您最近一年使用:0次
2020-01-12更新
|
222次组卷
|
32卷引用:2011届江西省上高二中高三上学期第三次月考化学试卷
(已下线)2011届江西省上高二中高三上学期第三次月考化学试卷江西省上高县第二中学2017-2018学年高二上学期期末考试化学试题(已下线)2010年浙江省温州二中高二第二学期期中考试化学试题(已下线)2010年海南省嘉积中学高二上学期第二次月考化学试卷(已下线)2010—2011学年山西省大同一中高二上学期期末考试化学试卷(已下线)2010—2011学年湖北省蒲圻高中高二上学期期末统考化学试卷(已下线)2011-2012学年河北省魏县一中高二上学期期中考试化学试卷(已下线)2011-2012学年河北唐山市第一中学高二年级调研考试化学试卷(已下线)2011-2012学年河北广平县第一中学高二第二次调研考试理科化学试题(已下线)2012-2013学年浙江省桐乡一中高二下学期期中考试化学试卷(已下线)2014年化学高考总复习课时演练 8-4难溶电解质的溶解平衡练习卷(已下线)2014年高考化学苏教版总复习 8-4 难溶电解质的溶解平衡练习卷(已下线)2014年高考化学一轮复习课后规范训练8-4练习卷2014-2015学年湖北省长阳县第一高级中学高二上学期期中化学试卷2015届上海理工大学附中高三上学期月考化学试卷2014-2015山西省山大附中高二12月月考化学试卷2014-2015福建省三明一中高二上学期第二次月考化学试卷2016届安徽省巢湖市无为一中高三上学期第一次月考化学试卷2016-2017学年江西省南昌二中高二上第二次考试化学卷内蒙古赤峰二中2017-2018学年高二上学期第二次月考化学试题内蒙古赤峰二中2017-2018学年高二上学期第一次月考化学试题广东省中山市第一中学2017-2018学年高二上学期第三次统测化学试题(已下线)2018年9月30日《每日一题》人教选修4每周一测【全国百强校】河北省石家庄市第二中学2018-2019学年高二第一学期12月月考化学试题2019年广东省汕头市高三第一次模拟考试化学试题云南省福贡县一中2019-2020学年高二上学期期末考试化学试题(已下线)上海市奉贤区2014届高三1月调研(期末)测试化学试题新疆伊犁奎屯市第一高级中学2020-2021学年高二上学期期末考试化学试题广东省揭阳普宁二中2021届上学期高三第二次月考化学试题上海市实验学校2021-2022学年高三下学期4月月考化学试题上海市川沙中学2021-2022学年高三下学期5月月考化学试题河北省行唐启明中学2022-2023学年高二上学期期末考试化学试题



