名校
解题方法
1 . 根据信息回答以下与金属元素相关的问题。
I .镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(1)钙在周期表中的位置为__________ 。锶比钙的金属性更强,它们的单质都能和水反应放出氢气,则锶与水反应的化学方程式为_____________ 。颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应那么剧烈,原因是__________ 。
(2)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的化合物,Y、Z与水反应均可放出气体。0.0lmolY溶于l00mL盐酸恰好完全反应,生成氯化物混合溶液,则盐酸的物质的量浓度为___________ , Z的电子式为_____________________ 。
II. KMnO4常用作氧化剂、防腐剂、消毒剂、漂白剂和水处理剂等。
(3)工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4,化学方程式为_________________ 。此过程不用瓷坩埚的原因是_________________________ 。
(4)高锰酸钾在酸性介质中还原产物为Mn2+,废液中c(Mn2+)浓度较大时会污染水体。实验室可以用过二硫酸铵[(NH4)2S2O8]溶液检验废水中Mn2+,实验现象是溶液变紫红色(还原产物为 ),写出检验Mn2+的离子方程式
),写出检验Mn2+的离子方程式_________________ 。
I .镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(1)钙在周期表中的位置为
(2)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的化合物,Y、Z与水反应均可放出气体。0.0lmolY溶于l00mL盐酸恰好完全反应,生成氯化物混合溶液,则盐酸的物质的量浓度为
II. KMnO4常用作氧化剂、防腐剂、消毒剂、漂白剂和水处理剂等。
(3)工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4,化学方程式为
(4)高锰酸钾在酸性介质中还原产物为Mn2+,废液中c(Mn2+)浓度较大时会污染水体。实验室可以用过二硫酸铵[(NH4)2S2O8]溶液检验废水中Mn2+,实验现象是溶液变紫红色(还原产物为
 ),写出检验Mn2+的离子方程式
),写出检验Mn2+的离子方程式
您最近一年使用:0次
2 . 下图是元素周期表的一部分。
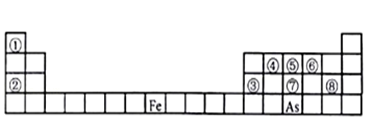
Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为_______ ,由①、⑤两元素构成的10电子化合物的形成过程为_______ 。
(2)⑦、⑧的最高价含氧酸的酸性较弱的是_______ 。(化学式表示)
(3)As在元素周期表中位置为__ ;氢化物的沸点:NH3 _______ AsH3(填“>”或“<”)
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_______ ,当消耗75g还原剂时,电子转移了__ mol。
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。
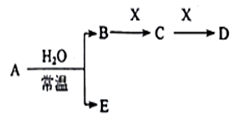
(1)A与水反应的化学方程式为_______ 。
(2)工业上常用CO热还原法冶炼X,写出其化学方程式_______ 。
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式_______ 。
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为_______ ;
(2)B的化学式为_______ 。

Ⅰ、用化学用语回答下列问题:
(1)由②、⑥两元素形成的强氧化性物质的电子式为
(2)⑦、⑧的最高价含氧酸的酸性较弱的是
(3)As在元素周期表中位置为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
Ⅱ、A、B、C、D、E、X是上述周期表给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如下图所示转化关系(部分生成物和反应条件略去),若常温下A为红棕色气体,B为强酸,X为常见金属单质。

(1)A与水反应的化学方程式为
(2)工业上常用CO热还原法冶炼X,写出其化学方程式
(3)某温度下(>100℃)若m克X与H2O反应放出QkJ(Q>0)的热量。写出该反应的热化学方程式
Ⅲ、由①、⑤、⑥、S和Fe五种元素组成的相对分子质量为392的化合物B,B中含有结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色有刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
(1)由实验a、b推知B溶液中含有的离子为
(2)B的化学式为
您最近一年使用:0次
名校
3 . 下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)在标号元素中,最活泼的金属元素是____ 。最活泼的非金属元素是____ 。(写元素符号)⑨元素的离子结构示意图是____________________ 。
(2)①与②形成共价化合物的电子式________________ 。用电子式表示⑤与⑨形成化合物的形成过程__________________________________________ 。
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是________ 。(写元素符号)
(4)⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是____ (写分子式);其三种元素的最高价含氧酸的酸性由强到弱的顺序 _________ 。(写酸的分子式)
(5)写出⑥元素的单质与氢氧化钠反应的离子方程式:____________________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在标号元素中,最活泼的金属元素是
(2)①与②形成共价化合物的电子式
(3)⑤、⑥、⑦三种元素的原子半径由大到小的顺序是
(4)⑦、⑧、⑨三种元素所形成的气态氢化物中,最稳定的氢化物是
(5)写出⑥元素的单质与氢氧化钠反应的离子方程式:
您最近一年使用:0次
2017-05-10更新
|
176次组卷
|
2卷引用:重庆市江津田家炳中学2016-2017学年高一下学期期中考试化学试题
真题
解题方法
4 . 金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数) 。
。
(1) 元素在周期表中位置是
元素在周期表中位置是_______ ,其原子结构示意图_______ ;
(2) 与最活跃的非金属元素A形成化合物D,D的电子式为
与最活跃的非金属元素A形成化合物D,D的电子式为_______ ;
(3)配平用钙线氧脱磷的化学方程式:
___ P +___ FeO +____ CaO
____ Ca3(PO4)2+____ Fe;
(4)将钙线试样溶于稀盐酸,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测Mn+的方法是_______ (用离子方程式表达);
(5)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3_______ g。
 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数) 。
。(1)
 元素在周期表中位置是
元素在周期表中位置是(2)
 与最活跃的非金属元素A形成化合物D,D的电子式为
与最活跃的非金属元素A形成化合物D,D的电子式为(3)配平用钙线氧脱磷的化学方程式:

(4)将钙线试样溶于稀盐酸,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测Mn+的方法是
(5)取1.6g钙线试样,与水充分反应,生成224mLH2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3
您最近一年使用:0次
2016-12-09更新
|
89次组卷
|
3卷引用:2010年普通高等学校招生全国统一考试理综化学部分(重庆卷)
9-10高一下·重庆·期末
5 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,
按要求填写下列空白:
(1)在这些元素中,化学性质最不活泼的元素是:_______ (填元素符号),其原子结构示意图为_______________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是______ ,碱性最强的化合物的电子式是________________ 。
(3)最高价氧化物属两性氧化物的元素是______ (填元素符号);写出它的最高价氧化物与氢氧化钠溶液反应的化学方程式:__________________________ 。
(4)用电子式表示元素④与⑦形成的化合物的形成过程:_______________ 。
该化合物属于_________ (填 “共价”或“离子”)化合物。
(5)比较:氢化物稳定性②_____ ③,最高价氧化物对应水化物的酸性②____ ⑥
(填“>”、“<”或“=”)。
(6)⑥的最高价氧化物与烧碱溶液反应的离子方程式为__________________ ;
(7)工业上制取元素⑥的单质的化学方程式为_______________________ 。
按要求填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)最高价氧化物属两性氧化物的元素是
(4)用电子式表示元素④与⑦形成的化合物的形成过程:
该化合物属于
(5)比较:氢化物稳定性②
(填“>”、“<”或“=”)。
(6)⑥的最高价氧化物与烧碱溶液反应的离子方程式为
(7)工业上制取元素⑥的单质的化学方程式为
您最近一年使用:0次



