1 . 按要求回答问题。
(1)1 mol HCHO分子中含有σ键的数目为___________ NA。
(2)CS2分子中,共价键的类型有___________ 。
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是___________ (填序号,下同),只存在非极性键的是___________ ,只存在离子键的是___________ ,既存在离子键又存在极性共价键的是___________ ,既存在离子键又存在非极性共价键的是___________ 。
(4)第一电离能比较Mg___________ Al,解释原因___________ 。
(1)1 mol HCHO分子中含有σ键的数目为
(2)CS2分子中,共价键的类型有
(3)下列物质中:
①MgCl2;②Na2O2; ③CS2 ;④NaOH;⑤H2。
只存在极性键的是
(4)第一电离能比较Mg
您最近一年使用:0次
名校
2 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物(ETFE)制成。回答下列问题:
的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______ 。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填标号),判断的根据是_______ ;第三电离能的变化图是_______ (填标号)。

(3)氟化氢的沸点高于氯化氢的原因是_______ 。
(4)聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
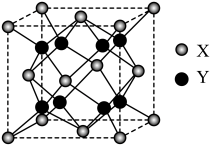
(5)萤石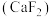 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______ ;若该立方晶胞参数为a pm,正负离子的核间距最小为_______ pm。
 与四氟乙烯
与四氟乙烯 的共聚物(ETFE)制成。回答下列问题:
的共聚物(ETFE)制成。回答下列问题:(1)基态F原子的价电子排布图(轨道表示式)为
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(3)氟化氢的沸点高于氯化氢的原因是
(4)聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因
(5)萤石
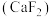 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
您最近一年使用:0次
3 . 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
(1) 元素基态原子次外层电子数是最外层电子数的
元素基态原子次外层电子数是最外层电子数的 ,其价电子轨道表示式是
,其价电子轨道表示式是___________ 。
(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是___________ ,在元素周期表中的位置是___________ 。
(3)Z元素基态原子的轨道表示式是图中的___________ (填写序号),

另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合___________ 。
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能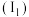 。如图所示:
。如图所示:

①同周期内,随着原子序数的增大, 值变化的总趋势是
值变化的总趋势是___________ 。
②根据第一电离能的含义和元素周期律,可推断出
___________  。
。
(1)
 元素基态原子次外层电子数是最外层电子数的
元素基态原子次外层电子数是最外层电子数的 ,其价电子轨道表示式是
,其价电子轨道表示式是(2)Y是1~36号元素原子核外电子排布中未成对电子数最多的元素,B元素的名称是
(3)Z元素基态原子的轨道表示式是图中的

另一轨道表示式不能作为基态原子的轨道表示式是因为它不符合
a.能量最低原理 b.泡利不相容原理 c.洪特规则
(4)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫作第一电离能
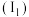 。如图所示:
。如图所示:
①同周期内,随着原子序数的增大,
 值变化的总趋势是
值变化的总趋势是②根据第一电离能的含义和元素周期律,可推断出

 。
。
您最近一年使用:0次
4 . 根据有关知识,回答下列问题。
(1)符号 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。
(2)铝原子核外电子云有__________ 种不同的伸展方向,有__________ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是__________ (填元素符号,下同),电负性最大的元素是__________ 。
(4)Be的第一电离能大于B的第一电离能,这是因为__________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:__________ 。
(6)锰元素位于第四周期第ⅦB族,请写出基础 的价层电子排布式
的价层电子排布式__________ 。
(1)符号
 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C. 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)锰元素位于第四周期第ⅦB族,请写出基础
 的价层电子排布式
的价层电子排布式
您最近一年使用:0次
名校
解题方法
5 . 我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)下列N原子的电子排布图表示的状态中,能量最高的是___________(填字母)。
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在B和N之间的元素有___________ 种。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ ,Na在空气中燃烧发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为___________ (填“发射”或“吸收”)光谱。
(4) 与同主族磷的氢化物
与同主族磷的氢化物 键角大小比较
键角大小比较___________ ,请解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:___________ 。
(1)下列N原子的电子排布图表示的状态中,能量最高的是___________(填字母)。
A. | B. |
C. | D. |
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在B和N之间的元素有
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)
 与同主族磷的氢化物
与同主族磷的氢化物 键角大小比较
键角大小比较 的键角比
的键角比 的键角大的原因:
的键角大的原因:
您最近一年使用:0次
2023-12-23更新
|
350次组卷
|
2卷引用:湖南省张家界市民族中学2023-2024学年高二上学期期中考试化学试题
6 . 翡翠的主要成分为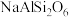 ,还含有其他多种金属阳离子,其中
,还含有其他多种金属阳离子,其中 的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
(1)基态 最外电子层的电子排布图(轨道表示式)为
最外电子层的电子排布图(轨道表示式)为___________ 。
(2)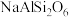 所含元素中,第一电离能最小的是
所含元素中,第一电离能最小的是___________ (填元素符号,下同);电负性最大的是___________ 。
(3)配合物 中的配体是
中的配体是___________ , 的沸点比
的沸点比 的高了许多,主要原因是
的高了许多,主要原因是___________
(4)已知某 的结构如图所示。
的结构如图所示。


___________ ,粒子内部的键角
___________  (填“>”“ <”或“=”)。
(填“>”“ <”或“=”)。
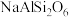 ,还含有其他多种金属阳离子,其中
,还含有其他多种金属阳离子,其中 的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一
的含量决定其绿色的深浅,是决定翡翠品质的重要因素之一(1)基态
 最外电子层的电子排布图(轨道表示式)为
最外电子层的电子排布图(轨道表示式)为(2)
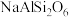 所含元素中,第一电离能最小的是
所含元素中,第一电离能最小的是(3)配合物
 中的配体是
中的配体是 的沸点比
的沸点比 的高了许多,主要原因是
的高了许多,主要原因是(4)已知某
 的结构如图所示。
的结构如图所示。


 (填“>”“ <”或“=”)。
(填“>”“ <”或“=”)。
您最近一年使用:0次
解题方法
7 . 乙炔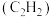 和丙烯腈
和丙烯腈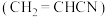 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。
(1) 的基态核外电子排布式为
的基态核外电子排布式为_______ 。 元素在周期表中的位置为
元素在周期表中的位置为_______ 。
(2)基态N原子第一电离能比基态O原子_______ (填“高”,“低”或“相等”)
(3) 的分子构型为
的分子构型为_______ 。
(4)每个丙烯腈分子中碳原子的杂化轨道类型有_______ 。
(5) 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为_______  。
。
(6)丙烯腈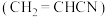 分子中共面的原子数目最多为
分子中共面的原子数目最多为_______ 。
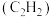 和丙烯腈
和丙烯腈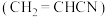 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。(1)
 的基态核外电子排布式为
的基态核外电子排布式为 元素在周期表中的位置为
元素在周期表中的位置为(2)基态N原子第一电离能比基态O原子
(3)
 的分子构型为
的分子构型为(4)每个丙烯腈分子中碳原子的杂化轨道类型有
(5)
 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为 。
。(6)丙烯腈
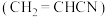 分子中共面的原子数目最多为
分子中共面的原子数目最多为
您最近一年使用:0次
名校
8 . 我国科学家构建了新型催化剂“纳米片”(Co−N−C),该“纳米片”可用于氧化 和吸附
和吸附 。回答下列问题:
。回答下列问题:
(1)基态Co原子的价层电子排布式为______ ,N、C、Co中第一电离能最大的是______ (填元素符号)。
(2)在空气中 会被氧化成
会被氧化成 。
。 的空间结构是
的空间结构是______ , 中S原子采用
中S原子采用______ 杂化。已知氧族元素氢化物的熔沸点高低顺序为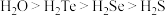 ,其原因是
,其原因是______ 。
(3)氰气 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为______ 。
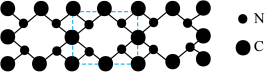
(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为______ 。
 和吸附
和吸附 。回答下列问题:
。回答下列问题:(1)基态Co原子的价层电子排布式为
(2)在空气中
 会被氧化成
会被氧化成 。
。 的空间结构是
的空间结构是 中S原子采用
中S原子采用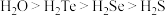 ,其原因是
,其原因是(3)氰气
 称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则
称为拟卤素,它的分子中每个原子最外层都达到8电子结构,则 分子中σ键、π键个数之比为
分子中σ键、π键个数之比为(4)氮和碳组成的一种新型材料,硬度超过金刚石,其部分结构如下图所示。它的化学式为

您最近一年使用:0次
2023-02-10更新
|
619次组卷
|
3卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题
9 . 下图是元素周期表的一部分,所列的字母分别代表一种化学元素。试回答下列问题:
(1)基态n原子中,核外电子占据最高能层的符号是_______ ,占据该能层的电子云轮廓图形状为_______ 。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ 。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
①o元素价电子的轨道表示式为_______ 。
②比较两元素的 、
、 可知,气态
可知,气态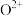 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为_______ (填元素符号)。
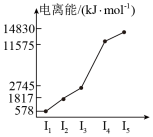
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式_______ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p(序号)两元素的部分电离能数据列于下表:
| 元素 | o | p | |
电离能 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
②比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)元素的基态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能,c、d、e三元素中,电子亲和能从大到小的顺序为
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式

您最近一年使用:0次
名校
解题方法
10 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
(1)元素p的原子结构示意图为___________________ 。
(2)o、p两元素的部分电离能数据如下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是_________________________________________________________ 。
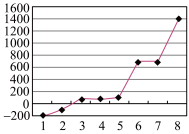
(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是___________________ (填图1中的序号)。
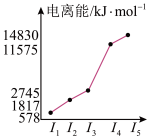
(4)表中所列的某主族元素的电离能情况如图所示,则该元素是___________________ (填元素符号)。
(5)基态钒原子的价电子排布图为___________________ 。
(6)写出单电子数最多的原子的电子排布式:__________________________________________ 。
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
a | |||||||||||||||||
b | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o | p | |||||||||||||||
(1)元素p的原子结构示意图为
(2)o、p两元素的部分电离能数据如下表:
元素 元素电离能/  | o | p |
| 717 | 759 |
| 1509 | 1561 |
| 3248 | 2957 |
比较两元素的
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是(3)第三周期8种元素单质熔点高低的顺序如图所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图所示,则该元素是

(5)基态钒原子的价电子排布图为
(6)写出单电子数最多的原子的电子排布式:
(7)下列状态的镁中,电离最外层一个电子所需能量最大的是 (填标号)。
A.[Ne]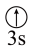 | B.[Ne]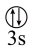 | C.[Ne]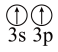 | D.[Ne]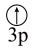 |
您最近一年使用:0次



