1 . 金属氢化物是具有良好发展前景的储氢材料。
(1)LiH中,离子半径:Li+_________ H-(填“>”、“=”或“<”)。
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_________ (填元素符号)。
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是_____ 。
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是_____________________ ;只含有σ键的是__________ ;含有由两个原子的s轨道重叠形成的σ键的是________ ;不存在化学键的是________ ;含有离子键和非极性键的是_________ 。
(1)LiH中,离子半径:Li+
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是
您最近一年使用:0次
解题方法
2 . 按下列要求作答。
(1)第二周期中,第一电离能介于B和N之间的元素共有_________ 种。
(2)第四周期中,原子核外电子排布有两个未成对电子的元素有_________ 种。
(3)硅烷(Si,H2H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________________________ 。

(1)第二周期中,第一电离能介于B和N之间的元素共有
(2)第四周期中,原子核外电子排布有两个未成对电子的元素有
(3)硅烷(Si,H2H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是

您最近一年使用:0次
3 . (1)某元素原子共有3个价电子,其中一个价电子位于第三能层 能级,该能层有
能级,该能层有______ 个原子轨道,该元素基态原子的价电子排布图为______ 。
(2) 、
、 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出 原子的核外电子排布式:
原子的核外电子排布式:______ 。
 能级,该能层有
能级,该能层有(2)
 、
、 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出 原子的核外电子排布式:
原子的核外电子排布式:电离能/ |  |  |  |  |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
您最近一年使用:0次
2020-03-05更新
|
468次组卷
|
3卷引用:四川省武胜烈面中学校2019-2020学年高二下学期期中考试化学试题
名校
4 . 完成下列各题:
(1)写出电子式NH4Cl_______ ,它的阳离子价层电子对对数为______ ,该离子空间构型为_______ 。
(2)周期表一共18列,第四周期第11列元素A,表示A所在族的符号为_________ ,它的基态原子结构示意图为_____ ,A+离子的价层电子排布图为____________ ,A2+离子的价层电子排布式为_____________ ,A+离子和A2+离子较稳定的是(填离子符号)_______ ,原因________________________ 。
(3)乙炔和乙烯分子,它们的σ键个数之比为______ ,乙烯分子中C原子杂化方式为________ ,C、N、O三种原子第一电离能从大到小排列____________ 。
(1)写出电子式NH4Cl
(2)周期表一共18列,第四周期第11列元素A,表示A所在族的符号为
(3)乙炔和乙烯分子,它们的σ键个数之比为
您最近一年使用:0次
名校
解题方法
5 . 硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
 元素的基态原子的价电子排布图为
元素的基态原子的价电子排布图为______ ,B、N、O元素的第一电离能由大到小的顺序为______ 。
 三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为
三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为______ ,B原子的杂化类型为______ 。
 自然界中,含B的钠盐是一种天然矿藏,其化学式写作
自然界中,含B的钠盐是一种天然矿藏,其化学式写作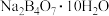 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个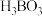 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“
,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“ ”标出其中的配位键,该阴离子通过
”标出其中的配位键,该阴离子通过______ 相互结合形成链状结构。

 科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为
科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为______ 。
 磷化硼
磷化硼 是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为______ ,当晶胞晶格参数为478pm时,磷化硼中硼原子和磷原子之间的最近距离为______ cm。
 元素的基态原子的价电子排布图为
元素的基态原子的价电子排布图为 三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为
三氟化硼在常温常压下为具有刺鼻恶臭和强刺激性气味的无色有毒腐蚀性气体,其分子的立体构型为 自然界中,含B的钠盐是一种天然矿藏,其化学式写作
自然界中,含B的钠盐是一种天然矿藏,其化学式写作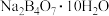 ,实际上它的阴离子结构单元是由两个
,实际上它的阴离子结构单元是由两个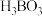 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“
,其结构式如图1,它的阴离子可形成链状结构。该阴离子由极性键和配位键构成,请在答题卷中抄上图1结构式后用“ ”标出其中的配位键,该阴离子通过
”标出其中的配位键,该阴离子通过
 科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为
科学家发现硼化镁在39K时有超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图2是该晶体微观结构中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影。则硼化镁的化学式为 磷化硼
磷化硼 是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
是一种有价值的超硬耐磨涂层材料,这种陶瓷材料可作为金属表面的保护薄膜。磷化硼晶胞如图3所示,在BP晶胞中B的堆积方式为
您最近一年使用:0次
2020-01-06更新
|
415次组卷
|
2卷引用:四川省成都市第七中学2021届高三上学期1月月考理综化学试题
名校
6 . 向硫酸铜水溶液中逐滴滴加氨水,先生成蓝色沉淀,继续滴加氨水得到深蓝色溶液,再向溶液中加入乙醇,有深蓝色晶体[Cu(NH3)4]SO4·H2O析出。
(1)铜元素位于元素周期表中____ 区,高温超导体钇钡铜氧材料中铜元素有+2和+3两种价态,基态Cu3+的电子排布式为____ 。
(2)非金属元素N、O、S的第一电离能由大到小的顺序是____ (用元素符号表示)。
(3)上述深蓝色晶体中含有的元素的电负性最小的是____ (用元素符号表示)。
(4)H2O的中心原子轨道杂化类型为____ 杂化;SO42-离子的立体构型是____ ,写出与SO42-互为等电子体的一种离子____ 。
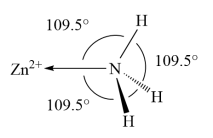
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因____ 。
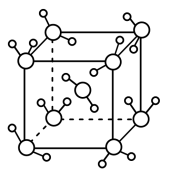
(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为____ g.cm-3(只列式,不计算)。
(1)铜元素位于元素周期表中
(2)非金属元素N、O、S的第一电离能由大到小的顺序是
(3)上述深蓝色晶体中含有的元素的电负性最小的是
(4)H2O的中心原子轨道杂化类型为
(5)NH3分子在独立存在时H-N-H键角为106.7°。如图为[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因

(6)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图所示。已知晶胞参数a=333.7 pm,阿伏加 德罗常数的值取6.02×1023,则重冰的密度为

您最近一年使用:0次
2019-11-13更新
|
289次组卷
|
3卷引用:2019年四川省遂宁市高三零诊考试理综化学试题
名校
7 . 氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示:
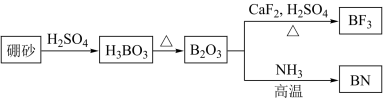
请回答下列问题:
(1)写出B2O3与NH3反应生成BN的化学反应方程式______________
(2)基态N原子的价层电子排布式为________ 。
(3)B、N、O相比,第一电离能最大的是______ ,BN中B元素的化合价为_____
(4)写出一个与SO42﹣互为等电子体的微粒__________ 。
(5)BF3能与NH3反应生成BF3•NH3,BF3•NH3中BF3与NH3之间通过________ (填“离子键”、“配位键”或“氢键”) 结合。

请回答下列问题:
(1)写出B2O3与NH3反应生成BN的化学反应方程式
(2)基态N原子的价层电子排布式为
(3)B、N、O相比,第一电离能最大的是
(4)写出一个与SO42﹣互为等电子体的微粒
(5)BF3能与NH3反应生成BF3•NH3,BF3•NH3中BF3与NH3之间通过
您最近一年使用:0次
名校
8 . 光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)Se在周期表的位置为_____ ,硅的基态原子电子排布式为_____ ,基态Ga原子核外电子占据的最高能级为_____ ,铜的基态原子价电子排布图为______ 。
(2)P、S、Ga电负性从大到小的顺序为____________________ 。
(3)与Al元素在元素周期表中处于对角线的铍,在性质上具有相似性,请写出铍的氧化物与氢氧化钠溶液反应的离子方程式_______________________
(4)As元素的第一电离能_____ Se元素的第一电离能(填“大于”、“小于”或“等于”),原因是_______________ 。
(5)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是_________________________
(1)Se在周期表的位置为
(2)P、S、Ga电负性从大到小的顺序为
(3)与Al元素在元素周期表中处于对角线的铍,在性质上具有相似性,请写出铍的氧化物与氢氧化钠溶液反应的离子方程式
(4)As元素的第一电离能
(5)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
您最近一年使用:0次
9 . (1)基态Si原子中,电子占据的最高能层符号为______ ,该能层具有的原子轨道数为______ .
(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:

晶体Q中各种微粒间的作用力有______ (填序号).
a.离子键b.共价键c.配位键d.氢键
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2﹣,不考虑空间构型,[Cu(OH)4]2﹣的结构可用示意图表示为______ ,科学家推测胆矾结构示意图可简单表示如图:胆矾的化学式用配合物的形式表示为_____________________ .

(4)第一电离能介于B、N之间的第二周期元素有______ 种.S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_____

(2)BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:

晶体Q中各种微粒间的作用力有
a.离子键b.共价键c.配位键d.氢键
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2﹣,不考虑空间构型,[Cu(OH)4]2﹣的结构可用示意图表示为

(4)第一电离能介于B、N之间的第二周期元素有

您最近一年使用:0次
2019-05-02更新
|
665次组卷
|
4卷引用:四川省宜宾市第四中学2018-2019学年高二下学期期中考试化学试题
10 . 光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)已知Se在周期表的位置为_____ ,硅的基态原子电子排布式为_____ ,基态Ga原子核外电子占据的最高能级为_____ ,铜的基态原子价电子排布图为_____ 。
(2)P、S、Ga电负性从大到小的顺序为_____ 。
(3)与Al元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为____ (标出配位键)
(4)已知[Cu(H2O)4]2+具有对称的空间构型,[Cu(H2O)4]2+中的2个H2O被Cl-取代,能得到2种不同结构的产物,则[Cu(H2O)4]2+的空间构型为_____ 。
(5)As元素的第一电离能____ Se元素的第一电离能(填“大于”、“小于”或“等于”),原因是__________ 。
(6)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是____ 。
(1)已知Se在周期表的位置为
(2)P、S、Ga电负性从大到小的顺序为
(3)与Al元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-的结构式为
(4)已知[Cu(H2O)4]2+具有对称的空间构型,[Cu(H2O)4]2+中的2个H2O被Cl-取代,能得到2种不同结构的产物,则[Cu(H2O)4]2+的空间构型为
(5)As元素的第一电离能
(6)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是
您最近一年使用:0次
2019-04-26更新
|
181次组卷
|
2卷引用:【校级联考】四川省蓉城名校联盟2018-2019学年高二下学期期中考试化学试题



