1 . 已知有3种基态元素原子的核外电子排布式:① ②
② ③
③ ,下列说法错误的是
,下列说法错误的是
 ②
② ③
③ ,下列说法错误的是
,下列说法错误的是| A.①与②可组成空间结构为正四面体形的化合物 |
| B.电负性:②>①>③ |
| C.第一电离能:①>③>② |
| D.三种元素均位于p区 |
您最近一年使用:0次
名校
2 . 下列说法中,错误的是
| A.基态原子是指处于最低能量状态的原子 |
B.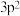 表示3p能级的两个轨道上各有一个电子 表示3p能级的两个轨道上各有一个电子 |
| C.电负性的大小可以作为判断元素非金属性强弱的依据 |
| D.第一电离能的大小可以作为判断元素金属性强弱的依据 |
您最近一年使用:0次
名校
3 . 下列关于元素周期表、原子结构或元素性质的说法中错误的是
| A.共价化合物中,电负性大的成键元素表现为负价 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.目前的元素周期表共有7个周期,7个主族,8个副族,1个0族 |
| D.主族元素的价电子即最外层电子,过渡元素的价电子还包括次外层甚至倒数第三层电子 |
您最近一年使用:0次
解题方法
4 . 电负性最大的元素是
| A.Na | B.F | C.H | D.Cl |
您最近一年使用:0次
名校
5 . 下列有关物质结构与性质的理解正确的是
| A.电负性大的元素,其第一电离能一定大 |
| B.σ键存在于所有分子中 |
C. 、 、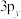 、 、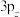 三个轨道相互垂直,能量相等 三个轨道相互垂直,能量相等 |
| D.干冰和冰的结构表明范德华力和氢键通常都具有方向性 |
您最近一年使用:0次
名校
解题方法
6 . 工业上电解熔融 和冰晶石(
和冰晶石( )的混合物可制得铝。下列说法不正确的是
)的混合物可制得铝。下列说法不正确的是
 和冰晶石(
和冰晶石( )的混合物可制得铝。下列说法不正确的是
)的混合物可制得铝。下列说法不正确的是A.半径大小: | B.电负性大小: |
C.电离能大小: | D.碱性强弱: |
您最近一年使用:0次
2024-03-04更新
|
214次组卷
|
2卷引用:江苏省镇江市丹阳高级中学2023-2024学年高三下学期3月月考化学试题
解题方法
7 . A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大。C是周期表中电负性最大的元素。基态E原子的核外电子有7种空间运动状态。基态F原子有3个未成对电子。按要求回答下列问题:
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式___________ 。
(2)基态原子第一电离能大小介于E和F之间的元素有___________ 。(用元素符号表示)
(3)氨硼烷(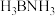 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为___________ (用元素符号表示)。
(4)磷酸盐在微生物作用下可转化为 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为___________ 。 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为___________ 。
(1)A和E可形成一种正四面体形的配合物离子,请写出该离子的化学式
(2)基态原子第一电离能大小介于E和F之间的元素有
(3)氨硼烷(
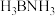 )是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为
)是一种安全、高效的储氢材料。与N原子相连的H呈正电性,与B原子相连的H呈负电性,则氨硼烷分子中原子的电负性从大到小的顺序为(4)磷酸盐在微生物作用下可转化为
 ,
, 的中心原子的杂化方式为
的中心原子的杂化方式为 键角为93.6°,小于
键角为93.6°,小于 模型的预测值,原因为
模型的预测值,原因为
您最近一年使用:0次
2024-03-04更新
|
225次组卷
|
2卷引用:浙江省杭州第二中学东河校区2023-2024学年高二上学期期末考试化学试题
名校
8 . 下表为元素周期表前三周期的一部分:
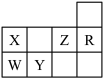
(1)Y的基态原子的电子排布式为___________ 。
(2)X的氢化物的沸点与W的氢化物的沸点比较:________ >_______ (填化学式),原因是________ 。
(3)选出X的基态原子的电子排布图___________ ,另一电子排布图不能作为基态原子的电子排布图是因为它不符合___________ (填序号)。

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,___________ (填元素符号)元素第一电离能最大,___________ 元素的电负性最大。
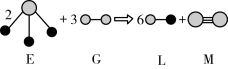
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是___________ 。
A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键

(1)Y的基态原子的电子排布式为
(2)X的氢化物的沸点与W的氢化物的沸点比较:
(3)选出X的基态原子的电子排布图

A.能量最低原理 B.泡利原理 C.洪特规则
(4)以上五种元素中,
(5)由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图所示,则下列判断错误的是

A.G是最活泼的非金属单质
B.L是极性分子
C.E的中心原子杂化轨道类型为sp2杂化
D.M的化学性质比同主族相邻元素单质的化学性质活泼
E.M分子中有1个σ键,2个π键
您最近一年使用:0次
9 . 高纯硅可以采用下列方法制备.下列说法正确的是

| A.晶体Si导电性介于导体和绝缘体之间,常用于制造光导纤维 |
B.可以通过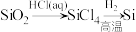 实现粗硅的制备 实现粗硅的制备 |
C.步骤①的反应为 ,不能说明碳的非金属性比硅强 ,不能说明碳的非金属性比硅强 |
D.已知电负性: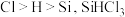 遇水会剧烈反应,化学方程式为 遇水会剧烈反应,化学方程式为 |
您最近一年使用:0次
2024-03-01更新
|
373次组卷
|
2卷引用:山东省部分学校2023-2024学年高三下学期2月份大联考(开学)质量检测化学试题
10 . 根据已学知识,请回答下列问题:
(1)基态 N 原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的原子轨道形状为___________ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:___________ 。
(3)某元素被科学家称之为人体微量元素中的"防癌之王",其原子的价层电子排布式为4s24p4,该元素的名称是___________ 。
(4)已知铁是26号元素,写出基态 Fe 的价层电子排布式:___________ ;在元素周期表中,该元素在___________ (填“s”“p”“d”“f”或“ds”)区。
(5)从原子结的角度分析 B 、N和O的第一电能由大到小的顺序为___________ ,电负性由大到小的顺序是___________ 。
(1)基态 N 原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的"防癌之王",其原子的价层电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出基态 Fe 的价层电子排布式:
(5)从原子结的角度分析 B 、N和O的第一电能由大到小的顺序为
您最近一年使用:0次



