2010·上海嘉定·二模
名校
1 . 已知C3N4晶体很可能具有比金刚石更大的硬度,且原子间均已单键结合,下列关于晶体说法正确的是
| A.C3N4晶体是分子晶体 |
| B.C3N4晶体中,C-N键的键长比金刚石中C-C键的键长要长 |
| C.C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子 |
| D.C3N4晶体中微粒间通过离子键结合 |
您最近一年使用:0次
2020-03-23更新
|
191次组卷
|
20卷引用:云南省楚雄州南华县民族中学2018-2019学年高二上学期期中考试化学试题
云南省楚雄州南华县民族中学2018-2019学年高二上学期期中考试化学试题(已下线)上海市嘉定、黄浦区2010届高三第二次模拟考试化学试题(已下线)2012届浙江省杭州高中高三第二次月考化学试卷(已下线)2012届浙江省杭西高中高三上学期11月月考试卷(已下线)2011-2012学年河南许昌鄢陵一高高二下学期期中考试化学试卷(已下线)2012-2013年湖北省仙桃市毛嘴高中高二上学期学业水平监测试化学卷2015-2016学年贵州省思南中学高二下第二次月考化学试卷2015-2016学年四川省南充高中高二下期末化学试卷2017届上海师范大学第二附属中学高三上学期期中考试化学试卷陕西省黄陵中学高新部2017-2018学年高二6月月考化学试题贵州省剑河县二中2018-2019学年高二上学期期末考试化学试题云南省景东一中2018-2019学年高二下学期开学考试化学试题鲁科版高二化学物质结构与性质单元练习卷:第3章 物态的聚集状态与物质性质云南省新平县三中2019-2020学年高二上学期期中考试化学试题云南省开远市第二中学校2019-2020学年高二上学期期末考试化学试题四川省南充市阆中中学2020届高三化学《晶体类型与性质》专题练习上海市曹杨二中2016-2017学年高二下学期第一次考试化学(等级考)试题四川省棠湖中学2019-2020学年高二下学期期中考试化学试题四川省阿坝州九寨沟2019-2020学年高二上学期期末考试化学试题陕西省宝鸡市金台区2020-2021学年高二下学期期末考试化学试题
2 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___ 。
(2)锗(Ge)、砷(As)、硒的第一电离能大小排序为___ (填元素符号)。H2SeO4的酸性比H2SeO3的强,其原因是___ 。
(3)H2SeO3的中心原子杂化类型是___ ,SeO32-的立体构型是___ 。与SeO42-互为等电子体的分子有___ (写一种物质的化学式即可)。
(4)H2Se属于___ (填“极性”或“非极性”)分子;单质硒的熔点为217℃,它属于___ 晶体。
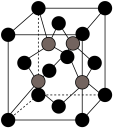
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___ ;若该晶胞的密度为ρg⋅cm-3,硒化锌的摩尔质量为Mg·mol-1。NA代表阿伏加 德罗常数的值,则晶胞参数a为___ pm。
(1)基态硒原子的价层电子排布式为
(2)锗(Ge)、砷(As)、硒的第一电离能大小排序为
(3)H2SeO3的中心原子杂化类型是
(4)H2Se属于
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为

您最近一年使用:0次
名校
解题方法
3 . 卤素的单质和化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。回答下列问题:
(1)溴原子的价层电子排布图为_______ 。根据下表提供的第一电离能数据,判断最有可能生成较稳定的单核阳离子的卤素原子是________ (填元素符号)。
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合[(HF)2]形式存在,使氟化氢分子缔合的相互作用是____________ 。碘在水中溶解度小,但在碘化钾溶液中明显增大,这是由于发生反应:I-+I2=I3-,CsICl2与KI3类似,受热易分解,倾向于生成晶格能更大的物质,试写出CsICl2受热分解的化学方程式:_________________________________ 。
(3)ClO2-中心氯原子的杂化轨道类型为________ ,与ClO2-具有相同立体构型和键合形式的物质的化学式为____________ (写出一个即可)。
(4)如图甲为碘晶体晶胞结构,平均每个晶胞中有________ 个碘原子,碘晶体中碘分子的配位数为____________ 。


(5)已知NA为阿伏加 德罗常数,CaF2晶体密度为ρ g·cm-3,其晶胞如图乙所示,两个最近Ca2+核间距离为a nm,则CaF2的相对分子质量可以表示为____________ 。
(1)溴原子的价层电子排布图为
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能/ (kJ·mol-1) | 1 681 | 1 251 | 1 140 | 1 008 |
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合[(HF)2]形式存在,使氟化氢分子缔合的相互作用是
(3)ClO2-中心氯原子的杂化轨道类型为
(4)如图甲为碘晶体晶胞结构,平均每个晶胞中有


(5)已知NA为阿伏加 德罗常数,CaF2晶体密度为ρ g·cm-3,其晶胞如图乙所示,两个最近Ca2+核间距离为a nm,则CaF2的相对分子质量可以表示为
您最近一年使用:0次
2019-11-22更新
|
210次组卷
|
3卷引用:云南省楚雄市紫溪中学2019-2020学年高三上学期期末考试理综化学试题
名校
4 . 分子中存在π 键,且碳原子全部以sp杂化轨道成键的是( )
| A.CH3CH3 | B.CH2=CH2 | C.CH≡CH | D.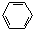 |
您最近一年使用:0次
2019-09-24更新
|
295次组卷
|
3卷引用:云南省楚雄州南华县第一中学2019-2020学年高二9月考试化学试题
名校
5 . A,B,C,D是四种短周期元素,E是过渡元素。A,B,C同周期,C,D同主族,A的原子结构示意图为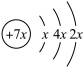 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A________ ,B________ ,C________ ,D________ 。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是________ ,碱性最强的是__________ 。
(3)用元素符号表示D所在周期第一电离能最大的元素是________ ,电负性(除稀有气体外)最大的元素是_________ 。
(4)E元素原子的核电荷数是_________ ,E元素在周期表的第_______ 周期第_______ 族,在________ 区。
(5)写出D元素原子构成单质的电子式___________ ,该分子中有_______ 个σ键,_______ 个π键。
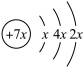 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期第一电离能最大的元素是
(4)E元素原子的核电荷数是
(5)写出D元素原子构成单质的电子式
您最近一年使用:0次
2019-08-13更新
|
210次组卷
|
8卷引用:云南省武定县第一中学2018-2019学年高二上学期12月份考试化学试题
名校
6 . 金属钛(Ti)是一种具有许多优良性能的金属,钛和钛合金被认为是21世纪的重要金属材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为_____ 。
②与BH4-互为等电子体的阳离子的化学式为_____ 。
③H、B、Ti原子的第一电离能由小到大的顺序为_____ 。
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。
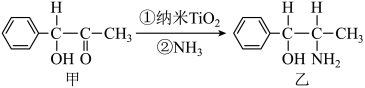
化合物乙的分子中采取sp3杂化方式的原子个数为_____ 。
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为____ 。
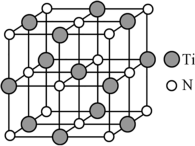
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是_____ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态电子排布式可表示为
②与BH4-互为等电子体的阳离子的化学式为
③H、B、Ti原子的第一电离能由小到大的顺序为
(2)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。纳米TiO2催化的一个实例如图所示。

化合物乙的分子中采取sp3杂化方式的原子个数为
(3)水溶液中并没有[Ti(H2O)6)]4+离子,而是[Ti(OH)2(H2O)4]2+离子,1mol[Ti(OH)2(H2O)4]2+中σ键的数目为
(4)氮化钛(TiN)具有典型的NaCl型结构,某碳氮化钛化合物,结构是用碳原子取代氮化钛晶胞(结构如图)顶点的氮原子,则此碳氮化钛化合物的化学式是

您最近一年使用:0次
2019-06-01更新
|
521次组卷
|
4卷引用:云南省楚雄姚安一中2020届高三3月线上模拟理综化学试题
名校
7 . 在解释下列物质性质的变化规律与物质结构间的因果关系中,与键的强弱无关的变化规律是( )
| A.HF、HCl、HBr、HI的热稳定性依次减弱 | B.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C.F2、Cl2、Br2、I2的熔、沸点逐渐升高 | D.H2S的稳定性小于H2O的稳定性 |
您最近一年使用:0次
2019-03-30更新
|
541次组卷
|
4卷引用:云南省禄丰县一中2019-2020学年高二12月月考化学试题
10-11高二下·福建三明·阶段练习
名校
解题方法
8 . 下列各说法中正确的是
| A.分子中键能越高,键长越大,则分子越稳定 |
| B.元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子间不能形成共价键 |
| C.水分子可表示为HO—H,分子中键角为180° |
| D.H—O键键能为463KJ/mol,即18克H2O分解成H2和O2时,消耗能量为2×463KJ |
您最近一年使用:0次
2019-01-30更新
|
756次组卷
|
9卷引用:云南省禄丰县一中2019-2020学年高二12月月考化学试题
云南省禄丰县一中2019-2020学年高二12月月考化学试题(已下线)2010—2011学年福建省清流一中高二3月月考化学试卷(已下线)2012年鲁科版高中化学选修3 2.1共价键模型练习卷(已下线)2012-2013学年山西省晋中市昔阳中学高二下学期期末考试化学试卷(已下线)2014年高二鲁科版选修3化学规范训练 2.1.2键参数练习卷云南省玉溪市峨山一中2018-2019学年高二12月份考试化学考试【全国百强校】宁夏回族自治区育才中学勤行校区2018-2019学年高二下学期3月月考化学试题四川省平昌县驷马中学2020-2021学年高二上学期九月月考化学试题(已下线)第2.1.2讲 键参数——键能、键长与键角-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
真题
名校
9 . 我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:
HCHO+O2 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是
HCHO+O2
 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是| A.该反应为吸热反应 | B.CO2分子中的化学键为非极性键 |
| C.HCHO分子中既含σ键又含π键 | D.每生成1.8g H2O消耗2.24L O2 |
您最近一年使用:0次
2019-01-30更新
|
2124次组卷
|
19卷引用:云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题
云南省双柏县第一中学2018-2019学年高二上学期期中考试化学试题2013年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷)(已下线)2012-2013学年福建省师大附中高二下学期期末考试化学试卷(已下线)2014届高考化学二轮复习必做训练 物质结构与性质练习卷(已下线)2013-2014广西桂林十八中高二下学期开学考试化学试卷(已下线)2014-2015学年四川成都树德协进中学高二10月阶段性考试化学试卷2014-2015山西省忻州市第一中学高二下学期期中考试化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2015-2016学年山西太原五中高二下3月第二次周练化学卷2015-2016学年贵州省习水县一中高二下学期期中考试化学试卷2015-2016学年山西省怀仁一中高二下第三次月考化学试卷(已下线)2019年3月5日 《每日一题》人教选修3-共价键的类型吉林省长春汽车经济开发区第三中学2018-2019学年高二下学期4月月考化学试题山西省太原市第二十一中学2020届高三上学期期中考试化学试题广东省梅州市五华县2018-2019学年高二上学期第六次质量监测化学试题(已下线)【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二6月阶段性测试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期期末考试化学试题河南省宏力学校2020-2021学年高二上学期期末考试化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高二4月月考化学试题
12-13高二上·云南德宏·期中
名校
10 . 下列各组微粒中不属于等电子体的是( )
| A.CH4、NH4+ | B.H2S、HCl | C.CO2、N2O | D.CO32﹣、NO3﹣ |
您最近一年使用:0次
2019-01-14更新
|
184次组卷
|
10卷引用:云南省楚雄州南华县民族中学2018-2019学年高二上学期期中考试化学试题
云南省楚雄州南华县民族中学2018-2019学年高二上学期期中考试化学试题(已下线)2012-2013学年云南省芒市中学高二上学期期中考试化学试卷2015-2016学年河北邢台一中高二上学期期中测试化学试卷2016-2017学年河北省张家口一中高二12月月考化学卷云南省玉溪市易门中学2017-2018学年高二上学期期中考试化学试题贵州省息烽县一中2018-2019学年高二上学期期中考试化学试题云南省玉溪市峨山一中2018-2019学年高二12月份考试化学考试云南省景谷一中2018-2019学年高二下学期期末考试化学试题四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题新疆哈密市第八中学2019-2020学年高二下学期期中考试化学试题



