名校
1 . 从实验测得不同物质中氧氧之间的键长和键能的数据:
其中x、y的键能数据尚未测定,但可根据规律推导键能的大小顺序为w>z>y>x;该规律是
O | O | O2 | O | |
| 键长(10-12m) | 149 | 128 | 121 | 112 |
| 键能(kJ·mol-1) | x | y | z=494 | w=628 |
| A.成键的电子数越多,键能越大 | B.键长越长,键能越小 |
| C.成键所用的电子数越少,键能越小 | D.成键时电子对越偏移,键能越大 |
您最近一年使用:0次
2022-04-02更新
|
817次组卷
|
11卷引用:河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.1 第2课时
河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.1 第2课时第2章 化学键与分子间作用力——易错疑难集训(一)——A学习区 夯实基础(鲁科版选修3)云南省宣威市第三中学2021-2022学年高二下学期3月份考试化学试题(已下线)2.1.2 键参数——键能、键长和键角-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)第2.1.2讲 键参数——键能、键长与键角-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)四川省成都市龙泉驿区教育科学研究院2021-2022学年高二下学期期中考试化学试卷(已下线)第39练 共价键-2023年高考化学一轮复习小题多维练(全国通用)(已下线)2022年北京高考真题变式题15-19四川省成都市武侯高级中学2021-2022学年高二下学期期中考试化学试题第二章 分子结构与性质(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)(已下线)2022年北京高考真题化学试题变式题(选择题6-10)
名校
解题方法
2 . 目前我国研制的稀土催化剂催化转化汽车尾气示意图如图:

(1)Zr原子序数为40,价电子排布式为___ 。图1中属于非极性的气体分子是___ 。
(2)①氟化硼(BF3)是石油化工的重要催化剂。BF3中B-F比BF 中B—F的键长短,原因是
中B—F的键长短,原因是___ 。
②乙硼烷(B2H6)是用作火箭和导弹的高能燃料,氨硼烷(H3NBH3)是最具潜力的储氢材料之一。

B2H6的分子结构如图2所示,其中B原子的杂化方式为___ 。
③H3NBH3的相对分子质量与B2H6相差不大,但是H3NBH3的沸点却比B2H6高得多,原因是__ 。
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,该晶体中含有的化学键有__ 。
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,[Ni(CO)4]的配体中配位原子是___ 。
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图4所示,则与每个Sr2+紧邻的O2-有___ 个。
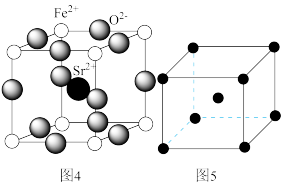
(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径为apm,相对原子质量为b,阿伏加 德罗常数为NA,试计算晶体铌的密度为___ g·cm-3(用来a、b、NA表示计算结果)。

(1)Zr原子序数为40,价电子排布式为
(2)①氟化硼(BF3)是石油化工的重要催化剂。BF3中B-F比BF
 中B—F的键长短,原因是
中B—F的键长短,原因是②乙硼烷(B2H6)是用作火箭和导弹的高能燃料,氨硼烷(H3NBH3)是最具潜力的储氢材料之一。

B2H6的分子结构如图2所示,其中B原子的杂化方式为
③H3NBH3的相对分子质量与B2H6相差不大,但是H3NBH3的沸点却比B2H6高得多,原因是
④硼酸盐是重要的防火材料。图3是硼酸钠晶体中阴离子(含B、O、H三种元素)的结构,该晶体中含有的化学键有
A.离子键 B.极性键 C.非极性键 D.配位键 E.金属键
(3)CO与Ni可生成羰基镍[Ni(CO)4],已知其中镍的化合价为0,[Ni(CO)4]的配体中配位原子是
(4)为了节省贵金属并降低成本,也常用钙钛矿型复合氧化物作为催化剂。一种复合氧化物结构如图4所示,则与每个Sr2+紧邻的O2-有

(5)与Zr相邻的41号元素Nb金属的晶格类型为体心立方晶格(如图5所示),原子半径为apm,相对原子质量为b,阿伏加 德罗常数为NA,试计算晶体铌的密度为
您最近一年使用:0次
2020-07-02更新
|
290次组卷
|
2卷引用:山东师范大学附属中学2020届普通高等学校招生全国统一考试化学试题(模拟一)
名校
3 . 1个C原子的单键氢化物分子是CH4,2个C原子的单键氢化物分子则为C2H6,以下各对分子间不存在类似关系的是( )
| A.NH3与N2H4 | B.H2O与H2O2 | C.SF6与S2F10 | D.SCl4与S2Cl2 |
您最近一年使用:0次
2020-01-17更新
|
394次组卷
|
10卷引用:云南省曲靖市陆良县第十中学2019-2020学年高二上学期期末考试化学试题
云南省曲靖市陆良县第十中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市沾益县炎方一中2019-2020学年高二上学期期末考试化学试题宁夏吴忠中学2017-2018学年高二上学期期末考试化学试题宁夏吴忠市吴忠中学2017-2018学年第一学期高二化学期末考试试卷云南省绿春县高级中学2019-2020学年高二上学期期末考试化学试题2020年人教版高二化学选修5有机化学第一章《认识有机物练》习3-1广西河池市都安第五高中2019-2020学年高二上学期期末考试化学试题广西壮族自治区河池市环江县第三中学2019-2020学年高二上学期期末考试化学试题(已下线)上海市浦东新区2014届高考预测(二模)化学试题(已下线)押新高考卷04题 有机化学基础-备战2022年高考化学临考题号押题(新高考通版)
名校
4 . A,B,C,D是四种短周期元素,E是过渡元素。A,B,C同周期,C,D同主族,A的原子结构示意图为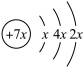 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A________ ,B________ ,C________ ,D________ 。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是________ ,碱性最强的是__________ 。
(3)用元素符号表示D所在周期第一电离能最大的元素是________ ,电负性(除稀有气体外)最大的元素是_________ 。
(4)E元素原子的核电荷数是_________ ,E元素在周期表的第_______ 周期第_______ 族,在________ 区。
(5)写出D元素原子构成单质的电子式___________ ,该分子中有_______ 个σ键,_______ 个π键。
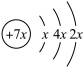 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期第一电离能最大的元素是
(4)E元素原子的核电荷数是
(5)写出D元素原子构成单质的电子式
您最近一年使用:0次
2019-08-13更新
|
210次组卷
|
8卷引用:云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题
9-10高二下·江苏·期末
名校
解题方法
5 . 已知A,B,C,D,E,F均为周期表中前36号元素,且原子序数依次增大.A,B,C为同一周期的主族元素,B原子p能级电子总数与s能级电子总数相等.A,F原子未成对电子是同周期中最多的,且F基态原子中电子占据三种不同形状的原子轨道.D和E原子的第一至第四电离能如下表所示:
(1)A,B,C三种元素的电负性最大的是__ (填写元素符号),D,E两元素中D的第一电离能较大的原因是__ .
(2)F基态原子的核外电子排布式是__ ;在一定条件下,F原子的核外电子从基态跃迁到激发态产生的光谱属于__ 光谱(填“吸收”或“发射”).
(3)根据等电子原理,写出AB+的电子式:__ .
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为__ .
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| D | 738 | 1451 | 7733 | 10540 |
| E | 578 | 1817 | 2745 | 11578 |
(2)F基态原子的核外电子排布式是
(3)根据等电子原理,写出AB+的电子式:
(4)已知:F3+可形成配位数为6的配合物.组成为FCl3•6H2O的配合物有3种,分别呈紫色、蓝绿色、绿色,为确定这3种配合物的成键情况,分别取等质量的紫色、蓝绿色、绿色3种物质的样品配成溶液,分别向其中滴入过量的AgNO3溶液,均产生白色沉淀且质量比为3:2:1.则绿色配合物的化学式为
A [CrCl(H2O)5]Cl2•H2O B [CrCl2(H2O)4]Cl•2H2O
C [Cr(H2O)6]Cl3 D [CrCl3(H2O)3]•3H2O
您最近一年使用:0次
2019-07-03更新
|
74次组卷
|
4卷引用:云南省麒麟高中2018-2019学年高二6月考试化学试题
6 . 硫化氢(H2S)分子中两个共价键的夹角接近90°,其原因是( )
①共价键的饱和性 ②S原子的电子排布 ③共价键的方向性 ④S原子中p轨道的形状
①共价键的饱和性 ②S原子的电子排布 ③共价键的方向性 ④S原子中p轨道的形状
| A.①② | B.①③ | C.②③ | D.③④ |
您最近一年使用:0次
2018-08-02更新
|
209次组卷
|
5卷引用:云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题
云南省曲靖市沾益二中2017-2018学年高二下学期期末考试化学试题贵州省息烽县一中2018-2019学年高二上学期期中考试化学试题云南省河口县高级中学2019-2020学年高二上学期期末考试化学试题(已下线)练习19 共价键-2020-2021学年【补习教材·寒假作业】高二化学(人教版)云南省易门一中2020-2021学年高二6月月考化学试题
解题方法
7 . 钛及其化合物的应用越来越受到人们的关注。
(1)基态Ti原子核外电子排布的最高能级符号是________ 。与钛同周期元素中,基态原子的未成对电子数与钛相同的有_______ 种。
(2)钛比钢轻,比铝硬,是种新兴的结构材料。钛硬度比铝大的原因是_________
(3)催化剂M能催化乙烯、丙烯、米乙烯等的聚合,其结构如图所示。

①M中,碳原子的杂化形式有__________ 种。
②M中,不含___________ (填标号)。
a.π键 b.σ键 c.配位键 d.氢键 e.离子键
(4)金红石(TiO2)是含钛的主要矿物之一,具有典型的四方晶系结构。其晶胞结构(晶胞中相同位置的原子相同)如图所示。

①4个微粒A、B、C、D中,属于氧原子的是______
②若A、B、C的原子坐标分别为A(0,0,0)、(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,___________ ,_____________ );钛氧键键长d=_________ (用代数式表示)。
(1)基态Ti原子核外电子排布的最高能级符号是
(2)钛比钢轻,比铝硬,是种新兴的结构材料。钛硬度比铝大的原因是
(3)催化剂M能催化乙烯、丙烯、米乙烯等的聚合,其结构如图所示。

①M中,碳原子的杂化形式有
②M中,不含
a.π键 b.σ键 c.配位键 d.氢键 e.离子键
(4)金红石(TiO2)是含钛的主要矿物之一,具有典型的四方晶系结构。其晶胞结构(晶胞中相同位置的原子相同)如图所示。

①4个微粒A、B、C、D中,属于氧原子的是
②若A、B、C的原子坐标分别为A(0,0,0)、(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,
您最近一年使用:0次
2018-05-28更新
|
211次组卷
|
2卷引用:【全国市级联考】山东省潍坊市2018届高三第三次高考模拟考试理综化学试题
8 . 氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为________ 个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为________ 。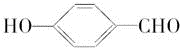 的沸点比
的沸点比 高,原因是
高,原因是__________________________ 。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________ 杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为_____________________________________ 。
(1)氧元素基态原子核外未成对电子数为
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为
 的沸点比
的沸点比 高,原因是
高,原因是(3)H+可与H2O形成H3O+,H3O+中O原子采用
您最近一年使用:0次
9 . 铀是原子反应堆的原料,常见铀的化合物有UF4、UO2及(NH4)4[UO2(CO3)3等。
回答下列问题:
(1)UF4用Mg或Ca 还原可得金属铀。基态钙原子的核外电子排布式为__________________ ;熔点:MgO(2852℃)高于CaO(2614℃),原因是_______________________________ ;金属铀的一种堆积方式为体心立方堆积,该堆积方式的空间利用率为_______________________________ 。
(2)已知:2UO2+5NH4HF2 2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是
2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是________ (填选项字母)。
a.氢键 b.配位键 c.共价键 d.离子键 e.金属键
(3)已知:3[(NH4)4[UO2(CO3)3] 3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑
3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑
①NH4+的空间构型为_____________________ ,与NH4+互为等电子体的分子或离子有_____ (任写两种)。
②CO32-中碳原子的杂化轨道类型为___________________________ 。
③分解产物中属于非极性分子的是____________________ (填选项字母)。
a.NH3 b. CO2 C.N2 d. H2O
(4)UO2的晶胞结构及晶胞参数如图所示:
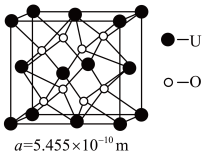
①晶胞中U 的配位数为__________________________ 。
②UO2晶体的密度为_____________ g·cm-3(列出计算式即可。设NA表示阿伏伽德罗常数的值)。
回答下列问题:
(1)UF4用Mg或Ca 还原可得金属铀。基态钙原子的核外电子排布式为
(2)已知:2UO2+5NH4HF2
 2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是
2UF4·NH4F+3NH3↑+ 4H2O↑,NH4HF2中含有的作用力是a.氢键 b.配位键 c.共价键 d.离子键 e.金属键
(3)已知:3[(NH4)4[UO2(CO3)3]
 3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑
3UO2+10NH3 ↑+9CO2 ↑+N2 ↑+9H2O↑①NH4+的空间构型为
②CO32-中碳原子的杂化轨道类型为
③分解产物中属于非极性分子的是
a.NH3 b. CO2 C.N2 d. H2O
(4)UO2的晶胞结构及晶胞参数如图所示:

①晶胞中U 的配位数为
②UO2晶体的密度为
您最近一年使用:0次
2018-03-08更新
|
514次组卷
|
2卷引用:广东省茂名市五大联盟学校2018届高三3月联考理综化学试题
名校
10 . 已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大。A的基态原子2p能级上有2个单电子;C是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是热和电最佳导体之一;D与F不同周期,但最外能层电子数相等。
(1)写出基态C原子的电子排布式:____________ 。
(2)A、B、C三种元素第一电离能最大的是____________ 。(用元素符号表示),其原因是____________ 。
(3)B、C两元素形成的化合物B2C的分子空间构型为____________ 。与B2C互为等电子体的粒子的化学式为____________ 。(填一种)。
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=_______ g/cm3(用含n、NA的计算式表示)。
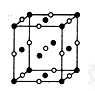
(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:__________________ (不要求计算结果)。

(1)写出基态C原子的电子排布式:
(2)A、B、C三种元素第一电离能最大的是
(3)B、C两元素形成的化合物B2C的分子空间构型为
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏伽德罗常数为NA,求晶胞的密度ρ=

(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:

您最近一年使用:0次



