名校
1 . 下列化学用语表示正确的是
A.NH3中N的杂化轨道表示式: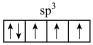 |
B.SO2分子的空间填充模型: |
C. 的形成过程: 的形成过程: |
| D.基态Br原子的价层电子排布式:3d104s24p5 |
您最近一年使用:0次
名校
2 . 下列说法错误的有
①乙醇、苯等有机溶剂易挥发且易被引燃,使用时需远离明火,用毕立即塞紧瓶塞
②第四周期元素中,未成对电子数最多的元素位于钾元素后面第五位
③高分子分离膜根据膜孔大小分为微滤膜、超滤膜、纳滤膜和反渗透膜等
④聚乳酸具有良好的生物相容性和生物可吸收性,可以用于手术缝合线等
⑤价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
⑥H2O比H2S稳定是因为水分子间存在氢键
⑦卤素单质、卤素氢化物、卤素碳化物(CX4)的熔、沸点均随着相对分子质量增大而升高
⑧邻羟基苯甲醛容易形成分子间氢键
①乙醇、苯等有机溶剂易挥发且易被引燃,使用时需远离明火,用毕立即塞紧瓶塞
②第四周期元素中,未成对电子数最多的元素位于钾元素后面第五位
③高分子分离膜根据膜孔大小分为微滤膜、超滤膜、纳滤膜和反渗透膜等
④聚乳酸具有良好的生物相容性和生物可吸收性,可以用于手术缝合线等
⑤价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
⑥H2O比H2S稳定是因为水分子间存在氢键
⑦卤素单质、卤素氢化物、卤素碳化物(CX4)的熔、沸点均随着相对分子质量增大而升高
⑧邻羟基苯甲醛容易形成分子间氢键
| A.①③⑥⑧ | B.③④⑤⑥ | C.⑥⑦⑧ | D.②⑦⑧ |
您最近一年使用:0次
名校
3 . 回答下列问题
(1)基态Mg原子的能量最高的电子占据的原子轨道呈___________ 形,原子中运动的电子有两种相反的自旋状态,若有一种自旋状态用 ,则与之相反的用
,则与之相反的用 ,称为电子的自旋磁量子数,基态Mg原子核外电子自旋磁量子数的代数和为
,称为电子的自旋磁量子数,基态Mg原子核外电子自旋磁量子数的代数和为___________ 。
(2)三氯化硼是一种重要的化工原料。形成 分子时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式为___________(填序号)。
分子时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式为___________(填序号)。
(3)与Sc同周期且其基态原子的未成对电子数与基态Sc原子相同的元素有___________ 种。
(4)已知元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(ev)。Sc的三种气态离子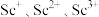 的电离势分别为
的电离势分别为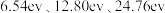 ,上述三种气态离子的电离势依次增大的原因为
,上述三种气态离子的电离势依次增大的原因为___________ 。
(5) 分子的空间构型为
分子的空间构型为___________ 。固态 能以无限长链形式存在(如图所示),长链结构中,连接2个S原子的O原子称为桥氧,连接1个S原子的O原子称为端基氧,则与S原子形成化学键键长更大的是
能以无限长链形式存在(如图所示),长链结构中,连接2个S原子的O原子称为桥氧,连接1个S原子的O原子称为端基氧,则与S原子形成化学键键长更大的是___________ (填“桥氧”或“端基氧”)。

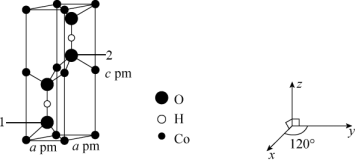
(6)已知Co可形成晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可表示晶胞中各原子的位置,称作原子的分数坐标,已知晶胞含对称中心,其中1号O原子的分数坐标为(0.6667,0.3333,0.1077),2号O原子的分数坐标为___________ 。
(1)基态Mg原子的能量最高的电子占据的原子轨道呈
 ,则与之相反的用
,则与之相反的用 ,称为电子的自旋磁量子数,基态Mg原子核外电子自旋磁量子数的代数和为
,称为电子的自旋磁量子数,基态Mg原子核外电子自旋磁量子数的代数和为(2)三氯化硼是一种重要的化工原料。形成
 分子时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式为___________(填序号)。
分子时,基态B原子价电子层上的电子先进行激发,再进行杂化,激发时B原子的价电子轨道表示式为___________(填序号)。A. | B. | C. | D.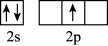 |
(4)已知元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(ev)。Sc的三种气态离子
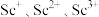 的电离势分别为
的电离势分别为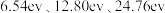 ,上述三种气态离子的电离势依次增大的原因为
,上述三种气态离子的电离势依次增大的原因为(5)
 分子的空间构型为
分子的空间构型为 能以无限长链形式存在(如图所示),长链结构中,连接2个S原子的O原子称为桥氧,连接1个S原子的O原子称为端基氧,则与S原子形成化学键键长更大的是
能以无限长链形式存在(如图所示),长链结构中,连接2个S原子的O原子称为桥氧,连接1个S原子的O原子称为端基氧,则与S原子形成化学键键长更大的是
(6)已知Co可形成晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可表示晶胞中各原子的位置,称作原子的分数坐标,已知晶胞含对称中心,其中1号O原子的分数坐标为(0.6667,0.3333,0.1077),2号O原子的分数坐标为

您最近一年使用:0次
名校
4 . 前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式___________ ,黄血盐晶体中各种微粒间的作用力不涉及___________ (填序号)。
a.金属键 b.共价键 c.配位键 d.离子键 e.氢键 f.分子间的作用力
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是___________ 。
(3)金属C、F晶体的晶胞如下图(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为___________ 。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,根据硬球接触模型,则r = ___________ a,列式表示F原子在晶胞中的空间占有率___________ (不要求计算结果)。

(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式
a.金属键 b.共价键 c.配位键 d.离子键 e.氢键 f.分子间的作用力
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是
(3)金属C、F晶体的晶胞如下图(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为

您最近一年使用:0次
名校
5 . 下列分子的中心原子采用sp3杂化,但分子的空间结构不同的一组是
①SO3;②SO2;③H2S;④CS2;⑤NH3;⑥CCl4
①SO3;②SO2;③H2S;④CS2;⑤NH3;⑥CCl4
| A.①②③ | B.①⑤⑥ | C.②③④ | D.③⑤⑥ |
您最近一年使用:0次
2023-03-23更新
|
358次组卷
|
4卷引用:甘肃省张掖市高台县第一中学2022-2023学年高二下学期4月月考化学试题
名校
6 . 下列说法正确的是
A.124g 含有的P—P键的个数为 含有的P—P键的个数为 |
B. 结构与过氧化氢相似,是直线形分子 结构与过氧化氢相似,是直线形分子 |
C. 分子中σ键和π键数目比是4:1 分子中σ键和π键数目比是4:1 |
D. 的空间结构是平面三角形 的空间结构是平面三角形 |
您最近一年使用:0次
2022-05-18更新
|
150次组卷
|
2卷引用:甘肃省张掖市 高台县第一中学2022-2023学年高二下学期3月月考化学试题
7 . 向盛有硫酸铜蓝色溶液的试管里滴加氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色溶液,再加无水乙醇得到深蓝色晶体 。溶液和晶体呈现深蓝色都是因为
。溶液和晶体呈现深蓝色都是因为 的存在。下列说法不正确的是
的存在。下列说法不正确的是
 。溶液和晶体呈现深蓝色都是因为
。溶液和晶体呈现深蓝色都是因为 的存在。下列说法不正确的是
的存在。下列说法不正确的是A.配离子 中 中 为中心离子, 为中心离子, 为配体,配位数为4 为配体,配位数为4 |
| B.加入乙醇的目的是降低配合物的溶解度 |
C. 空间构型为正四面体形,和VSEPR模型不一致 空间构型为正四面体形,和VSEPR模型不一致 |
D.配离子中N原子属于 杂化,4个杂化轨道分别形成1个配位键和3个N-H σ键 杂化,4个杂化轨道分别形成1个配位键和3个N-H σ键 |
您最近一年使用:0次
2022-04-22更新
|
144次组卷
|
2卷引用:甘肃省张掖市校际联考2021-2022学年高二下学期期中考试化学试题
名校
8 . 一种医药中间体的结构如图所示,X、Y、Z、W、Q为原子序数依次递增的短周期元素,其中只有Y、Z、W位于同一周期,且Y原子s能级上的电子总数是p能级上电子总数的2倍,下列说法错误 的是

| A.X分别与Y、Z、W都可形成10电子分子 |
B.Z、W最简单氢化物分子的键角: |
C.Y、Q的最高价含氧酸酸性: |
D.Y、Z、W的基态原子的第一电离能大小: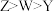 |
您最近一年使用:0次
2022-04-22更新
|
489次组卷
|
5卷引用:甘肃省张掖市校际联考2021-2022学年高二下学期期中考试化学试题
甘肃省张掖市校际联考2021-2022学年高二下学期期中考试化学试题湖北省第七届2022届高三 4月调研模拟考试化学试题(已下线)三轮冲刺卷2-【赢在高考黄金20卷】备战2022年高考化学模拟卷(湖北专用)黑龙江省哈尔滨市德强高中2021-2022学年高二下学期期中考试化学试题(已下线)选择题11-14
名校
解题方法
9 . 下列说法正确的是
A.最外层都只有 个电子的元素原子性质一定相似 个电子的元素原子性质一定相似 |
| B.同一周期元素中,第一电离能随原子序数增加而增大 |
C. 晶体中存在 晶体中存在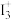 离子, 离子,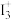 离子的几何构型为 离子的几何构型为 形 形 |
D. 是一种含有极性键和非极性键的非极性分子 是一种含有极性键和非极性键的非极性分子 |
您最近一年使用:0次
2022-03-22更新
|
156次组卷
|
3卷引用:甘肃省高台县第一中学2021-2022学年高二下学期3月月考化学试题
名校
解题方法
10 . 下列叙述正确的是
A. 是极性分子,分子中氮原子是在3个氢原子所构成的三角形的中心 是极性分子,分子中氮原子是在3个氢原子所构成的三角形的中心 |
B. 是非极性分子,分子中碳原子处在4个氯原子所构成的正方形的中心 是非极性分子,分子中碳原子处在4个氯原子所构成的正方形的中心 |
C. 是极性分子,分子中氧原子不处在2个氢原子所连成的直线的中间 是极性分子,分子中氧原子不处在2个氢原子所连成的直线的中间 |
D. 是非极性分子,分子中碳原子不处在2个氧原子所连成的直线的中间 是非极性分子,分子中碳原子不处在2个氧原子所连成的直线的中间 |
您最近一年使用:0次
2021-02-16更新
|
933次组卷
|
39卷引用:甘肃省临泽一中2018-2019学年高二下学期期末模拟化学试题
甘肃省临泽一中2018-2019学年高二下学期期末模拟化学试题(已下线)2010年福建省华安一中高二下学期期末考试化学试题(已下线)2011届上海市南汇中学高三上学期期中考试化学卷(已下线)2010-2011学年山西省吕梁市高二下学期期中考试化学试卷(已下线)2011-2012学年江苏省泰州中学高二上学期期中考试化学(选修)试卷(已下线)2011-2012学年甘肃省甘谷一中高二下学期期中考试化学试卷(已下线)2011-2012学年福建省四地六校高二下学期第三次月考化学试卷2014-2015黑龙江省哈尔滨六中高二上期末化学试卷2014-2015学年辽宁实验分校高二下6月阶段测试化学试卷2015-2016学年湖北省黄石市有色一中高二下学期期中考试化学试卷河北省蠡县中学2016-2017学年高二6月月考化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--分子空间结构与物质性质河南省济源第一中学2017-2018学年高二下期6月月考化学试题(已下线)2018年11月30日 《每日一题》一轮复习-键的极性与分子的极性云南省彝良县民族中学2018-2019学年高二上学期12月份考试化学试题【全国百强校】吉林省长春外国语学校2018-2019学年高二下学期第一次月考化学试题(已下线)2019年4月12日 《每日一题》选修3-分子的极性判断吉林省吉林市第五十五中学2018-2019学年高二下学期3月月考化学试题【全国百强校】贵州省思南中学2018-2019学年高二下学期期中考试化学试题黑龙江省哈尔滨市呼兰一中、阿城二中、宾县三中、尚志五中四校2018-2019学年高二下学期期中考试化学试题【校级联考】福建省宁德市高中同心顺联盟校2018-2019学年高二下学期期中考试化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题贵州省罗甸县第一中学2019-2020学年高二上学期期末考试化学试题河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题课时3 分子的空间构型与分子性质——A学习区 夯实基础(鲁科版选修3)宁夏回族自治区银川一中2019-2020学年高二下学期期中考试化学试题山西省太原市实验中学校2019-2020学年高二下学期期中考试化学试题河北省唐山市开滦第二中学2019-2020学年高二6月月考化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第三节 分子结构与物质的性质 第1课时 共价键的极性高二选择性必修2(人教版2019)第二章 分子结构与性质 第三节 分子结构与物质的性质 课时1 共价键的极性(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构 第2课时 分子的空间结构与分子性质山东省泰安市宁阳一中2020-2021学年高二下学期3月月考化学试题人教2019选择性必修2第二章第三节 分子结构与物质的性质课后习题(已下线)第31讲 分子结构与性质(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题安徽省滁州市定远县炉桥中学2021-2022学年高二下学期期末考试化学试卷2019鲁科版高中化学选择性必修2第2章第2节 共价键与分子的空间结构课后习题福建省宁德第一中学2022-2023学年高二下学期3月月考化学试题



