名校
解题方法
1 . ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_____ ;

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为_____ ;
Se原子序数为_____ ,其核外M层电子的排布式为_____ ;
 离子的立体构型为
离子的立体构型为_____ ;
ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为_____ g·cm-3(列式并计算)。
(2)
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为
Se原子序数为
 离子的立体构型为
离子的立体构型为ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为
(2)

您最近一年使用:0次
解题方法
2 . 回答下列问题
(1)铁及其化合物用途非常广泛,也是人体含量最多的一种必需微量元素。
配合物离子 中Fe的配位数为
中Fe的配位数为_______ , 的结构有两种可能的写法,分别为
的结构有两种可能的写法,分别为 、
、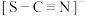 ,则
,则 中
中 键与
键与 键数之比为
键数之比为_______ , 中C原子的杂化方式为
中C原子的杂化方式为_______ 。
(2) 晶体的晶胞结构如图所示:
晶体的晶胞结构如图所示:

①氮原子的最高能级中电子云的形状为_______ 。
②晶体中,每个 周围与它距离最近且相等的
周围与它距离最近且相等的 共有
共有_______ 个。
③设阿伏加德罗常数的值为 ,晶胞参数为a pm,则
,晶胞参数为a pm,则 晶体的密度为
晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)铁及其化合物用途非常广泛,也是人体含量最多的一种必需微量元素。
配合物离子
 中Fe的配位数为
中Fe的配位数为 的结构有两种可能的写法,分别为
的结构有两种可能的写法,分别为 、
、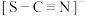 ,则
,则 中
中 键与
键与 键数之比为
键数之比为 中C原子的杂化方式为
中C原子的杂化方式为(2)
 晶体的晶胞结构如图所示:
晶体的晶胞结构如图所示:
①氮原子的最高能级中电子云的形状为
②晶体中,每个
 周围与它距离最近且相等的
周围与它距离最近且相等的 共有
共有③设阿伏加德罗常数的值为
 ,晶胞参数为a pm,则
,晶胞参数为a pm,则 晶体的密度为
晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
名校
解题方法
3 . 氮的相关化合物在材料等方面有重要用途。回答下列问题:
(1)基态N原子的核外电子排布式为_______ ,第一电离能:I1(N)_______ I1(O)(填“大于”或“小于”)。
(2)N及其同族的P、As均可形成类似的氢化物,NH3、PH3、AsH3的沸点由高到低的顺序为_______ (填化学式)。
(3)[N5]+[AsF6]-是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为_______ 。

(4)科学家近期首次合成了具有极性对称性的氮化物钙钛矿材料-LaWN3,其立方晶胞结构如图所示,晶胞中La、W、N分别处于顶角、体心、面心位置,晶胞参数为a nm。

①La与N间的最短距离为_______ nm,与La紧邻的N个数为_______ 。
②在LaWN3晶胞结构的另一种表示中,W处于各顶角位置,则在新的晶胞中,La处于_______ 位置,N处于_______ 位置。
③设LaWN3的式量为Mr,阿伏加德罗常数的值为NA,则该晶体的密度为_______ g·cm-3(列出计算表达式)。
(1)基态N原子的核外电子排布式为
(2)N及其同族的P、As均可形成类似的氢化物,NH3、PH3、AsH3的沸点由高到低的顺序为
(3)[N5]+[AsF6]-是一种全氮阳离子形成的高能物质,其结构如图所示,其中N原子的杂化轨道类型为

(4)科学家近期首次合成了具有极性对称性的氮化物钙钛矿材料-LaWN3,其立方晶胞结构如图所示,晶胞中La、W、N分别处于顶角、体心、面心位置,晶胞参数为a nm。

①La与N间的最短距离为
②在LaWN3晶胞结构的另一种表示中,W处于各顶角位置,则在新的晶胞中,La处于
③设LaWN3的式量为Mr,阿伏加德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
2022-04-22更新
|
1259次组卷
|
4卷引用:江西省景德镇一中2022-2023学年高二上学期期中考试化学试题
江西省景德镇一中2022-2023学年高二上学期期中考试化学试题广东省广州市2022届高三下学期二模综合测试化学试题(已下线)化学-2022年高考押题预测卷03(天津卷)广东省茂名高州市校际联盟2021-2022学年高二5月联考化学试题
名校
解题方法
4 . 碳(C)、铜(Cu)、锡(Sn)及其化合物有许多用途。回答下列问题。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为_______ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)___ I2(S)(填“>”、“<”或“=”),原因是_ 。PH3分子的热稳定性比NH3______ (填“强”或“弱”)。
(3)1mol苯中含 键的数目为
键的数目为______ 。CH3CH2COOH中C的杂化方式有______ ;
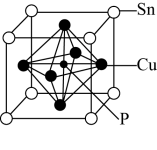
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为__________ nm,该晶体密度为______ g cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。

(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)
(3)1mol苯中含
 键的数目为
键的数目为(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为
 cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。
您最近一年使用:0次
2021-04-14更新
|
210次组卷
|
3卷引用:江西省重点校联盟2022-2023学年高三上学期8月联考化学试题



