名校
解题方法
1 . 铜及其化合物在科学研究和工业生产中具有许多用途,请回答下列问题:
(1)写出基态Cu原子的价电子排布式_______ 。
(2)已知高温下 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因_______ 。
(3)配合物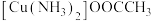 中碳原子的杂化类型是
中碳原子的杂化类型是_______ ,配体的空间构型为_______ 。配合物所含元素的电负性由大到小的顺序是_______ (用元素符号表示)。
(4)M原子的价电子排布式为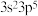 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
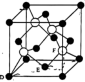
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为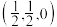 ,则F原子的坐标参数为
,则F原子的坐标参数为_______ 。
②已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为_______ pm(写出计算式)。
(1)写出基态Cu原子的价电子排布式
(2)已知高温下
 比CuO稳定,从核外电子排布角度解释高温下
比CuO稳定,从核外电子排布角度解释高温下 更稳定的原因
更稳定的原因(3)配合物
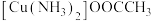 中碳原子的杂化类型是
中碳原子的杂化类型是(4)M原子的价电子排布式为
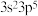 ,铜与M形成化合物的晶胞如图所示。
,铜与M形成化合物的晶胞如图所示。
①原子坐标参数,表示晶胞内部各原子的相对位置。上图晶胞中,其中原子坐标参数D为(0,0,0),E为
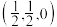 ,则F原子的坐标参数为
,则F原子的坐标参数为②已知该晶体的密度为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体中Cu原子和M原子之间的最短距离为
,则该晶体中Cu原子和M原子之间的最短距离为
您最近一年使用:0次
2022-10-12更新
|
459次组卷
|
4卷引用:辽宁省实验中学2023届高三上学期第一次阶段测试化学试题
名校
解题方法
2 . 氢、碳、氮、氧、钾、铜等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。请回答下列问题:
(1)基态N原子价层电子排布式为_______ 。原子中运动的电子有两种相反的自旋状态,若一种自旋状态用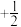 表示,则与之相反的用
表示,则与之相反的用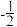 表示,这称为电子的自旋量子数。对于基态的N原子,其价电子的自旋量子数代数和为
表示,这称为电子的自旋量子数。对于基态的N原子,其价电子的自旋量子数代数和为_______ 。
(2)氢、碳、氧三种元素按原子数目比为2∶1∶1形成常温下呈气态的物质,其分子中键角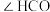
_______ 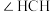 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
(3) 在水溶液中以
在水溶液中以 形式存在,向含
形式存在,向含 的溶液中加入足量氨水,可生成更稳定的
的溶液中加入足量氨水,可生成更稳定的 ,其原因是
,其原因是_______ 。若 离子中2个
离子中2个 被2个
被2个 替代可以得到2种不同的结构,则
替代可以得到2种不同的结构,则 离子的空间结构名称是
离子的空间结构名称是_______ (填“平面四边形”或“正四面体”)。
(4)碳的一种同素异形体的晶体可采取非密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞, 分子占据顶点和面心处,
分子占据顶点和面心处, 占据的是
占据的是 分子围成的正八面体空隙和正四面体空隙。若
分子围成的正八面体空隙和正四面体空隙。若 分子的坐标参数分别为A(0,0,0),B(
分子的坐标参数分别为A(0,0,0),B( ,0,
,0, ),C(1,1,1)等,则距离A位置最近的
),C(1,1,1)等,则距离A位置最近的 的原子坐标参数为
的原子坐标参数为_______ ,设晶胞参数为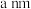 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  (列出表达式即可)。
(列出表达式即可)。

(1)基态N原子价层电子排布式为
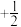 表示,则与之相反的用
表示,则与之相反的用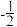 表示,这称为电子的自旋量子数。对于基态的N原子,其价电子的自旋量子数代数和为
表示,这称为电子的自旋量子数。对于基态的N原子,其价电子的自旋量子数代数和为(2)氢、碳、氧三种元素按原子数目比为2∶1∶1形成常温下呈气态的物质,其分子中键角
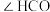
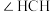 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(3)
 在水溶液中以
在水溶液中以 形式存在,向含
形式存在,向含 的溶液中加入足量氨水,可生成更稳定的
的溶液中加入足量氨水,可生成更稳定的 ,其原因是
,其原因是 离子中2个
离子中2个 被2个
被2个 替代可以得到2种不同的结构,则
替代可以得到2种不同的结构,则 离子的空间结构名称是
离子的空间结构名称是(4)碳的一种同素异形体的晶体可采取非密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,
 分子占据顶点和面心处,
分子占据顶点和面心处, 占据的是
占据的是 分子围成的正八面体空隙和正四面体空隙。若
分子围成的正八面体空隙和正四面体空隙。若 分子的坐标参数分别为A(0,0,0),B(
分子的坐标参数分别为A(0,0,0),B( ,0,
,0, ),C(1,1,1)等,则距离A位置最近的
),C(1,1,1)等,则距离A位置最近的 的原子坐标参数为
的原子坐标参数为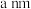 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 (列出表达式即可)。
(列出表达式即可)。
您最近一年使用:0次
名校
解题方法
3 . 铜及其化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)①将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解并得到深蓝色溶液,写出沉淀溶解的离子方程式:_______ 。
②向深蓝色溶液中继续加入乙醇,会析出深蓝色的晶体 。该晶体中含有的化学键类型为
。该晶体中含有的化学键类型为_______ 。在该晶体中 含有
含有 键的数目为
键的数目为_______ 。
③ 中各元素电负性由大到小的顺序为
中各元素电负性由大到小的顺序为_______ ,其中N原子的杂化轨道类型为_______ 。
④ 中
中 的键角比独立存在的
的键角比独立存在的 分子结构中的键角
分子结构中的键角_______ 。(填“大”“小”或“相等”)
(2)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示

①合金的化学式为_______ 。
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为_______ 。
③已知该合金晶体的密度为 ,则最近的两个Al原子间的距离为
,则最近的两个Al原子间的距离为_______ nm(阿伏加德罗常数的值用NA表示)。
(1)①将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解并得到深蓝色溶液,写出沉淀溶解的离子方程式:
②向深蓝色溶液中继续加入乙醇,会析出深蓝色的晶体
 。该晶体中含有的化学键类型为
。该晶体中含有的化学键类型为 含有
含有 键的数目为
键的数目为③
 中各元素电负性由大到小的顺序为
中各元素电负性由大到小的顺序为④
 中
中 的键角比独立存在的
的键角比独立存在的 分子结构中的键角
分子结构中的键角(2)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示

①合金的化学式为
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为
③已知该合金晶体的密度为
 ,则最近的两个Al原子间的距离为
,则最近的两个Al原子间的距离为
您最近一年使用:0次
4 . 含氮、磷的化合物在生活和生产中有许多重要用途,如 、磷化硼
、磷化硼 、磷青铜
、磷青铜 等.回答下列问题:
等.回答下列问题:
(1)铜 是第四周期元素,基态铜原子的价层电子轨道表示式为
是第四周期元素,基态铜原子的价层电子轨道表示式为_______ ;第四周期元素的基态原子中价层电子未成对最多的是_______ (填元素符号)
(2)键角
_______  (填“>、<、=”);化合物
(填“>、<、=”);化合物 能溶于水,其原因
能溶于水,其原因_______
(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层.磷化硼晶体晶胞如图所示:

①磷原子的配位数(与磷原子距离最近且相等的硼原子数)为_______
②已知原子坐标: 为
为 ,
, 为
为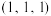 ,则图中B原子的坐标是
,则图中B原子的坐标是_______
③已知晶胞的密度为 ,阿伏加德罗常数的数值用
,阿伏加德罗常数的数值用 表示。则磷化硼晶体的晶胞边长为
表示。则磷化硼晶体的晶胞边长为_______ pm(列出计算式)
 、磷化硼
、磷化硼 、磷青铜
、磷青铜 等.回答下列问题:
等.回答下列问题:(1)铜
 是第四周期元素,基态铜原子的价层电子轨道表示式为
是第四周期元素,基态铜原子的价层电子轨道表示式为(2)键角

 (填“>、<、=”);化合物
(填“>、<、=”);化合物 能溶于水,其原因
能溶于水,其原因(3)磷化硼是一种耐磨涂料,它可用作金属的表面保护层.磷化硼晶体晶胞如图所示:

①磷原子的配位数(与磷原子距离最近且相等的硼原子数)为
②已知原子坐标:
 为
为 ,
, 为
为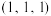 ,则图中B原子的坐标是
,则图中B原子的坐标是③已知晶胞的密度为
 ,阿伏加德罗常数的数值用
,阿伏加德罗常数的数值用 表示。则磷化硼晶体的晶胞边长为
表示。则磷化硼晶体的晶胞边长为
您最近一年使用:0次



