名校
1 . 下列有关物质性质与应用的对应关系正确的是
| 选项 | 性质 | 实际应用 |
| A | 小苏打不稳定,受热分解生成CO2 | 用于泡沫灭火器 |
| B | 聚乙炔是无限延伸的线状结构 | 用于导电材料 |
| C | Al(OH)3受热分解,生成高熔点物质和水 | 用作塑料的阻燃剂 |
| D | 石墨是混合型晶体,含大π键 | 用作润滑剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-22更新
|
1373次组卷
|
7卷引用:山东省济南市2022届高三3月高考模拟考试(一模)化学试题
山东省济南市2022届高三3月高考模拟考试(一模)化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)(已下线)秘籍02 化学与STSE-备战2022年高考化学抢分秘籍(全国通用)湖北省随州市曾都区第一中学2022届高三下学期第二次学业水平选择性模拟考试化学试题(已下线)专项06 元素及其化合物-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)专题05 元素及其化合物-三年(2020-2022)高考真题分项汇编河北省五个一联盟2022-2023学年高三上学期12月联考化学试题
名校
2 . 锰及其化合物用途非常广泛,也是人体的重要微量元素。请回答下列问题:
(1)锰在元素周期表中的位置为_______ 。
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
(3)锰能形成多种化合物如 、
、 、
、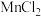 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是_______ 。(已知 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是_______ 原子;该配合物中除氢以外的元素,第一电离能从小到大的顺序为_______ (用元素符号表示)。
(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与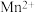 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是_______ (填“A”或“B”),原因是_______ 。
A.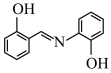 B.
B.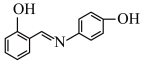
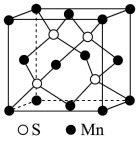
(6)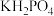 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大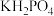 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
,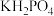 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
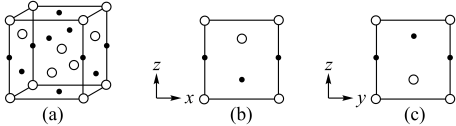
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度_______ 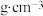 (写出表达式)。
(写出表达式)。
②晶胞在x轴方向的投影图为_______ (填标号)。
A.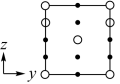 B.
B.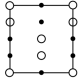 C.
C. D.
D.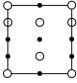
(1)锰在元素周期表中的位置为
(2)下列状态的锰原子或离子中,能用原子发射光谱捕捉以鉴别锰元素的是_______(填序号)。
A.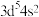 | B.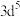 | C.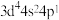 | D.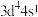 |
 、
、 、
、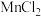 、
、 ,其中磁矩
,其中磁矩 最大的是
最大的是 ,其中n为金属离子核外的单电子数)
,其中n为金属离子核外的单电子数)(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]。配体
 与中心原子形成配位键时,提供孤对电子的原子是
与中心原子形成配位键时,提供孤对电子的原子是(5)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与
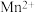 形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩邻氨基苯酚(B),沸点较高的是A.
 B.
B.

(6)
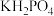 晶体具有优异的非线性光学性能。我国科学工作者制备的超大
晶体具有优异的非线性光学性能。我国科学工作者制备的超大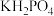 晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示
晶体已应用于大功率固体激光器,填补了国家战略空白。分别用○、●表示 和
和 ,
,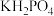 晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是
晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是 、
、 在晶胞xz面、yz面上的位置:
在晶胞xz面、yz面上的位置:
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度
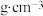 (写出表达式)。
(写出表达式)。②晶胞在x轴方向的投影图为
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解题方法
3 . 第VIII族元素(Fe、Co、Ni等)在生产、生活中用途广泛。回答下列问题:
(1)第四周期基态原子与基态Ni3+未成对电子数相同的元素有_______ 种。
(2)邻二氮菲(phen,结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+,该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中Fe2+的配位数为_______ ;实验表明,邻二氮菲检验Fe2+的适宜pH范围是2~9,其原因是_______ 。

(3)草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸_______ 甲酸(填“>”“<”或“=”),其原因是_______ 。
(4)Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。

①Fe3+填充在O2-围成的_______ 空隙处(填“正四面体”或“正八面体”)。
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为_______ 。
(1)第四周期基态原子与基态Ni3+未成对电子数相同的元素有
(2)邻二氮菲(phen,结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+,该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中Fe2+的配位数为

(3)草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸
(4)Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。

①Fe3+填充在O2-围成的
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为
您最近一年使用:0次
名校
解题方法
4 . 卤族元素及其化合物种类繁多,有着非常重要的用途。回答下列问题:
(1)基态Br原子的电子排布式为[Ar]_______ 。
(2)HF分子的极性_______ (填“大于”、“等于”或“小于”,以下同)HCl,同一条件下,HF在水中的溶解度_______ HCl,HF的沸点_______ HCl。SOCl2中心S原子VSEPR模型为_______ 。1mol氟硼酸铵(NH4BF4)中含有_______ mol配位键。
(3)下列对IF3分子的空间结构推断最合理的是_______ (填标号)(已知:电子对之间的最小夹角为90°时,排斥力最小的更稳定)。
A. B.
B.  C.
C. 
(4)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为a pm、a pm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,坐标原点见图,标记为n的原子分数坐标为 ,则m的原子分数坐标为
,则m的原子分数坐标为_______ ,距离Hg最近的Ag有_______ 个。设NA为阿伏加德罗常数的值,Ag2HgI4的摩尔质量为M g•mol-1,该晶体的密度为_______ g·cm-3(用代数式表示)。

(1)基态Br原子的电子排布式为[Ar]
(2)HF分子的极性
(3)下列对IF3分子的空间结构推断最合理的是
A.
 B.
B.  C.
C. 
(4)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为a pm、a pm和2apm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影,坐标原点见图,标记为n的原子分数坐标为
 ,则m的原子分数坐标为
,则m的原子分数坐标为
您最近一年使用:0次
名校
解题方法
5 . 过渡元素用途广泛。回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ 。
(2)Co与Ca位于同一周期、且最外层电子数相等,但Co的熔点、沸点均比Ca高,原因是_______ 。
(3) 1mol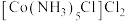 中含有的σ键数目为
中含有的σ键数目为_______ , 分子与
分子与 形成配合物后
形成配合物后 键角
键角_______ (填“变大”“变小”或“不变”)。
(4) 中配体
中配体 的空间结构为
的空间结构为_______ ,N、O原子相比,第二电离能与第一电离能差值更大的是_______ (填元素符号)。
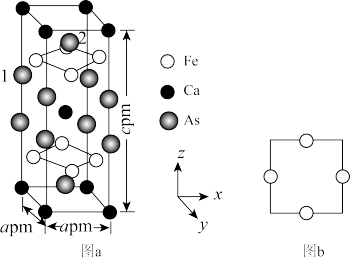
(5)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为_______ ,已知体心与顶点的Ca原子有着相同的化学环境,晶胞中As原子1分数坐标为(0,0,0.628),则As原子2的分数坐标为_______ ,体心Ca原子与As原子1之间的距离为_______ pm。
(1)基态
 的价电子排布式为
的价电子排布式为(2)Co与Ca位于同一周期、且最外层电子数相等,但Co的熔点、沸点均比Ca高,原因是
(3) 1mol
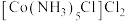 中含有的σ键数目为
中含有的σ键数目为 分子与
分子与 形成配合物后
形成配合物后 键角
键角(4)
 中配体
中配体 的空间结构为
的空间结构为(5)一种铁基超导材料晶胞结构如图a所示,铁原子沿z轴方向的投影如图b所示。该材料的化学式为

您最近一年使用:0次
2022-12-18更新
|
480次组卷
|
2卷引用:山东省淄博市2022-2023学年高三上学期12月月考化学试题
6 . 氮族元素及其化合物种类繁多,有着非常重要的用途,回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为
___________ 。
(2) 和
和 两种分子键角较小的是
两种分子键角较小的是___________ ,原因是:___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ 。
(4) 中三种元素电负性由大到小的顺序为
中三种元素电负性由大到小的顺序为___________ ,N杂化方式是___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5) 的立方晶胞结构如图所示:
的立方晶胞结构如图所示:

若砷化镓晶胞边长为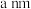 ,则该晶体密度为
,则该晶体密度为___________  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态
 原子的电子排布式为
原子的电子排布式为
(2)
 和
和 两种分子键角较小的是
两种分子键角较小的是(3)
 分子的空间构型为
分子的空间构型为(4)
 中三种元素电负性由大到小的顺序为
中三种元素电负性由大到小的顺序为 的沸点高于
的沸点高于 的原因是
的原因是(5)
 的立方晶胞结构如图所示:
的立方晶胞结构如图所示:
若砷化镓晶胞边长为
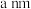 ,则该晶体密度为
,则该晶体密度为 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
7 . 镍、铜等金属及其化合物在工农业生产上有重要用途。回答下列问题:
(1)基态Ni的核外电子排布式为_______ ,Ni位于元素周期表中_______ 区(填“s”“p”“d”或“ds”),其核外电子占据的最高能层符号为_______ 。
(2)Ni与CO能形成如图所示的配合物 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为_______ 。 易溶于
易溶于_______ (填标号)。
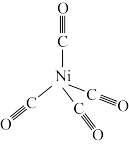
A.水 B.四氯化碳 C.苯 D.稀
(3)将Cu粉加入浓氨水中,并通入 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为_______ 。
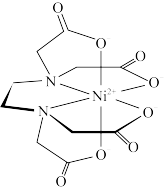
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有_______ 个,其中提供孤对电子的原子为_______ (写元素符号)。
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_______ 。
②已知晶胞参数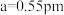 ,则该晶体的密度为
,则该晶体的密度为_______  (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
(1)基态Ni的核外电子排布式为
(2)Ni与CO能形成如图所示的配合物
 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为 易溶于
易溶于
A.水 B.四氯化碳 C.苯 D.稀

(3)将Cu粉加入浓氨水中,并通入
 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为②已知晶胞参数
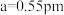 ,则该晶体的密度为
,则该晶体的密度为 (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
您最近一年使用:0次
8 . 铁、钴及其化合物在生活、生产中用途广泛。请回答下列问题:
(1)基态 的核外电子排布式为
的核外电子排布式为_______ ;第四周期元素中,基态原子未成对电子数与Co相等的有_______ (填元素符号)。
(2) 在氨水中能形成多种配合物。八面体配合物
在氨水中能形成多种配合物。八面体配合物 的结构有
的结构有_______ 种,其中极性分子有_______ 种;取 ,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为_______ 。
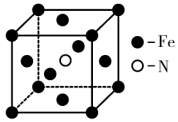
(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为_______ 。
(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,晶体中 占据
占据 形成的
形成的_______ (填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为_______ g/cm3(列计算式)。

(1)基态
 的核外电子排布式为
的核外电子排布式为(2)
 在氨水中能形成多种配合物。八面体配合物
在氨水中能形成多种配合物。八面体配合物 的结构有
的结构有 ,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为
,加入足量硝酸银溶液,得到1mol白色沉淀。该物质在溶液中形成的配合离子化学式为(3)铁和氨在640℃时可发生置换反应,一种产物的晶胞结构如图所示,该反应的化学方程式为

(4)钴蓝晶体的立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其结构如下图,晶体中
 占据
占据 形成的
形成的
您最近一年使用:0次
名校
解题方法
9 . 氟及其化合物用途非常广泛。回答下列问题:
(1)基态氟原子的价层电子排布图(轨道表示式)为_______ 。
(2)制备NSF3的反应为FCONSF2+2AgF2⇌NSF3+2AgF+COF2。
①F、O、N、S的第一电离能从小到大的顺序是_______ 。
②化工生产中NSF3可用作SF6的替代品,SF6分子的空间构型为_______ 。
③COF2分子中σ键和π键的个数比为_______ 。
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是_______ 。
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是_______ 。
③下列说法正确的是_______ (填标号)。
A.NHF2、CO2均是极性分子
B.H2O与NHF2中心原子的价层电子对数相同
C.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):

已知AC=BE,则C、D(Cs与F)间的距离为_______ pm(用含a、c、s的代数式表示,列出计算式,下同);设NA为阿伏加德罗常数的值,则晶体的密度为_______ g·cm-3。
(1)基态氟原子的价层电子排布图(轨道表示式)为
(2)制备NSF3的反应为FCONSF2+2AgF2⇌NSF3+2AgF+COF2。
①F、O、N、S的第一电离能从小到大的顺序是
②化工生产中NSF3可用作SF6的替代品,SF6分子的空间构型为
③COF2分子中σ键和π键的个数比为
(3)NHF2的一种制备方法是CO(NH2)2+2F2+H2O=NHF2+CO2+NH4HF2。
①CO(NH2)2中C的杂化方式是
②CO(NH2)2的熔沸点比CH3CONH2的高,其原因是
③下列说法正确的是
A.NHF2、CO2均是极性分子
B.H2O与NHF2中心原子的价层电子对数相同
C.NH4HF2中存在离子键、配位键和氢键
(4)由Cs、Ag及F三种元素组成的一种超导材料的晶体结构如下图所示(Ag不是+1价):

已知AC=BE,则C、D(Cs与F)间的距离为
您最近一年使用:0次
10 . Be、Mg、Ca均为ⅡA族元素,这些元素及其化合物在人类生产、生活和科学研究中具有广泛的用途。回答下列问题:
(1)金属单质的熔点:Mg_______ Ca(填“>”或“<”),原因是_______ ;最高价氧化物对应水化物的碱性:
_______ 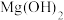 (填“>”或“<”)。
(填“>”或“<”)。
(2)氯化铍晶体易吸湿、水解、升华,可溶于有机溶剂。一定条件下有下列存在形式:
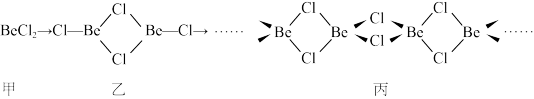
氯化铍晶体的晶体类型是_______ ,甲的空间构型是_______ ,乙中Be的杂化轨道类型是_______ ,从化学键角度分析形成丙的原因:_______ 。
(3) 是某些太阳能薄膜电池的材料,有人认为这种太阳能电池将取代硅基太阳能电池的统治地位。下图所示为
是某些太阳能薄膜电池的材料,有人认为这种太阳能电池将取代硅基太阳能电池的统治地位。下图所示为 的晶胞结构:
的晶胞结构:
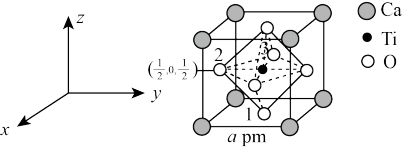
1、3号O的坐标分别为_______ 、_______ (用分数坐标表示),与Ca等距离且最近的O有_______ 个,若 的密度为
的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 =
=_______  (列出计算式)。
(列出计算式)。
(1)金属单质的熔点:Mg

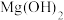 (填“>”或“<”)。
(填“>”或“<”)。(2)氯化铍晶体易吸湿、水解、升华,可溶于有机溶剂。一定条件下有下列存在形式:

氯化铍晶体的晶体类型是
(3)
 是某些太阳能薄膜电池的材料,有人认为这种太阳能电池将取代硅基太阳能电池的统治地位。下图所示为
是某些太阳能薄膜电池的材料,有人认为这种太阳能电池将取代硅基太阳能电池的统治地位。下图所示为 的晶胞结构:
的晶胞结构:
1、3号O的坐标分别为
 的密度为
的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数 =
= (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2022-05-26更新
|
752次组卷
|
3卷引用:山东省潍坊市2022届高三下学期三模统考(5月)化学试题



