名校
解题方法
1 . 碳族元素及其化合物在国家工业领域有非常重要用途。回答下列问题:
(1)基态锗原子价层电子排布式为_______ 。
(2)我国提出力争在2030年前实现碳达峰、2060年前实现碳中和,我国科学家研发的“液态阳光”项目利用了太阳能产生的电能电解水制氢,再选择高效催化剂将二氧化碳加氢合成甲醇等液体燃料,这将为实现碳达峰、碳中和提供了科学的方法,其中CO2分子中有_______ σ键和_______ π键,在干冰晶体中每个CO2分子周围有_______ 个CO2分子相邻。

(3)关于C、Si及其化合物的结构和性质,下列叙述正确的是_______(填序号)。
(4) 中碳原子的杂化轨道类型有
中碳原子的杂化轨道类型有_______ 。
(5)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。

①b为X的晶胞,该晶胞中粒子个数比Hg:Ge:Sb=_______ 。
②设X的最简式的式量为Mr,则X晶体的密度为_______ g/cm3(列出计算式)。
(1)基态锗原子价层电子排布式为
(2)我国提出力争在2030年前实现碳达峰、2060年前实现碳中和,我国科学家研发的“液态阳光”项目利用了太阳能产生的电能电解水制氢,再选择高效催化剂将二氧化碳加氢合成甲醇等液体燃料,这将为实现碳达峰、碳中和提供了科学的方法,其中CO2分子中有

(3)关于C、Si及其化合物的结构和性质,下列叙述正确的是_______(填序号)。
| A.分子稳定性:C2H6<Si2H6 |
| B.SiC是原子晶体,硬度:SiC>C(金刚石) |
| C.还原性:SiH4<CH4 |
| D.Si的原子半径大于C原子半径,难以形成π键 |
 中碳原子的杂化轨道类型有
中碳原子的杂化轨道类型有(5)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。

①b为X的晶胞,该晶胞中粒子个数比Hg:Ge:Sb=
②设X的最简式的式量为Mr,则X晶体的密度为
您最近一年使用:0次
2022-06-06更新
|
320次组卷
|
2卷引用:贵州省贵阳市五校2021-2022学年高三下学期联合考试(六)理科综合化学试题
2 . 镍及其化合物用途广泛,可用作催化剂、合金、电器元件等。回答下列问题:
(1)基态Ni原子价电子排布图为_______ 。
(2)某镍配合物由1个Ni2+与2个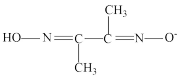 形成。
形成。
①形成该镍配合物的元素中,第二周期元素的第一电离能最大的为_______ (用元素符号表示) ,配合物中N采用的杂化类型为_______ 。
②已知该配合物中只有一种元素的原子与Ni2+配位,则与镍配位的原子为_______ (填“C”、“N"”或“O"),原因为_______ 。
(3)Ni(CO)4是常温下呈液态的镍的重要配合物,易溶于CCl4、苯等有机溶剂,则Ni(CO)4的空间构型为_______ ,Ni(CO)4中含有的σ键与π键的数目之比为_______ 。
(4)由Mg、C和Ni组成的新型超导材料晶体的立方晶胞结构如图所示。
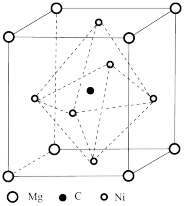
①该新型超导材料的化学式为_______ 。
②若晶胞参数为a nm,阿伏加德罗常数的值为NA,则该晶体的密度为_______ g·cm-3。
(1)基态Ni原子价电子排布图为
(2)某镍配合物由1个Ni2+与2个
 形成。
形成。①形成该镍配合物的元素中,第二周期元素的第一电离能最大的为
②已知该配合物中只有一种元素的原子与Ni2+配位,则与镍配位的原子为
(3)Ni(CO)4是常温下呈液态的镍的重要配合物,易溶于CCl4、苯等有机溶剂,则Ni(CO)4的空间构型为
(4)由Mg、C和Ni组成的新型超导材料晶体的立方晶胞结构如图所示。

①该新型超导材料的化学式为
②若晶胞参数为a nm,阿伏加德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
3 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为__________ ,基态S原子电子占据最高能级的电子云轮廓图为_________ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是_________ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________ 。
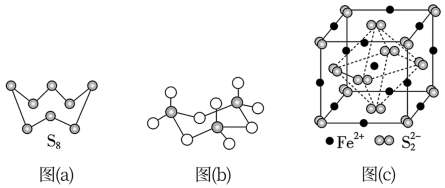
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为_____ 形,其中共价键的类型有______ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为___________ g·cm−3;晶胞中Fe2+位于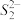 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为______ nm。
| H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | −85.5 | 115.2 | >600(分解) | −75.5 | 16.8 | 10.3 |
| 沸点/℃ | −60.3 | 444.6 | −10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为
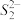 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
2018-06-09更新
|
13134次组卷
|
19卷引用:贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题
贵州省贵阳市2022-2023学年高三上学期10月质量监测化学试题贵州省黔南布依族苗族自治州龙里中学2019-2020学年高三上学期期末考试理综化学试题云南省玉溪市民族中学2021-2022学年高三下学期开学测试理综化学部分(已下线)专题18物质结构与性质(选修)-五年(2018~2022)高考真题汇编(全国卷)2018年全国普通高等学校招生统一考试化学(新课标II卷)(已下线)2018年高考题及模拟题汇编 专题18 物质结构与性质(选修)(已下线)《2019年高考总复习巅峰冲刺》专题12 物质结构与性质应试策略吉林省吉林市第五十五中学2018-2019学年高二下学期期中考试化学试题云南省富宁县第一中学2020届高三第一学期开学考试化学试题河南省南阳市第一中学2020届高三上学期第一次月考化学试题四川省自贡市田家炳中学2020届高三上学期期中考试化学试题四川省成都市北大成都附属实验中学2019-2020学年度高三上学期1月月考理科综合化学试题河北省2020届高三高考模拟理综化学试题(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编黑龙江省大庆市第四中学2020届高三下学期4月月考理综化学试题辽宁省锦州市渤海大学附属中学、育明高级中学2021届高三上学期第二次月考化学试题河南省长葛市第一高级中学2021届高三上学期10月阶段性测试化学试题四川邻水石永中学2021-2022学年高三上学期入学考试理科综合化学试题湖南省长沙市宁乡市2020-2021学年高二下学期期末调研考试化学试题



