解题方法
1 . (NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。回答下列问题:
(1)基态Fe原子价层电子的电子排布式为_______ 。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是_______ 。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是_______ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(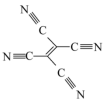 )。
)。
①CH3CN中碳原子的杂化方式是_______ 。
②TCNE中第一电离能较大的是_______ (填元素符号),分子中所有原子_______ (填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是_______ 。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成,Fe3C的晶胞结构如图所示(NA代表阿伏加德罗常数的数值):

Fe3C的密度为_______ (列出计算式)g·cm-3(1Å=10-8 cm)。
(1)基态Fe原子价层电子的电子排布式为
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE(
 )。
)。①CH3CN中碳原子的杂化方式是
②TCNE中第一电离能较大的是
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成,Fe3C的晶胞结构如图所示(NA代表阿伏加德罗常数的数值):

Fe3C的密度为
您最近一年使用:0次
名校
解题方法
2 . 第VA族元素氮、磷、砷的化合物用途广泛。回答下列问题:
(1)实验中常用 检验
检验 ,
, 中
中 的配位数为
的配位数为_______ ,其中碳原子的杂化轨道类型为_______ 杂化。1mol 中含有
中含有 键的数目为
键的数目为_______ 。
(2)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:_______ 。

(3)阿伏加德罗常数的值为 ,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为
,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为_______  (写出表达式即可)。
(写出表达式即可)。
(4)用铬原子代替部分铜原子,可以形成一系列铜—铬合金。其中两种铜—铬合金的晶体结构如图所示。

①晶体a中铬原子的配位数为_______ 。
②晶体b中铬原子填充在由铜原子构成的_______ (填“四面体”“六面体”或“八面体”)空隙中, 表示阿伏加德罗常数的值,铜原子半径为
表示阿伏加德罗常数的值,铜原子半径为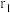 cm,铬原子半径为
cm,铬原子半径为 cm,则晶体b的空间利用率为
cm,则晶体b的空间利用率为_______ 。(写出表达式即可)
(1)实验中常用
 检验
检验 ,
, 中
中 的配位数为
的配位数为 中含有
中含有 键的数目为
键的数目为(2)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:

(3)阿伏加德罗常数的值为
 ,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为
,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为 (写出表达式即可)。
(写出表达式即可)。(4)用铬原子代替部分铜原子,可以形成一系列铜—铬合金。其中两种铜—铬合金的晶体结构如图所示。

①晶体a中铬原子的配位数为
②晶体b中铬原子填充在由铜原子构成的
 表示阿伏加德罗常数的值,铜原子半径为
表示阿伏加德罗常数的值,铜原子半径为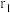 cm,铬原子半径为
cm,铬原子半径为 cm,则晶体b的空间利用率为
cm,则晶体b的空间利用率为
您最近一年使用:0次
解题方法
3 . 在元素周期表中,铜副族(IB族)包括铜、银、金等元素,在生产、生活和科研中都有着广泛用途和重要的研究价值。
(1)Ag元素在元素周期表分区中属于_______ 区,基态Ag原子的价电子排布式为_______ 。
(2)硫代硫酸银(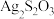 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。
①依据 理论推测
理论推测 的空间构型为
的空间构型为_______ ,中心原子S的杂化方式为_______ 。
②在 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是_______ 。
(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
_______  (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是_______ 。
(4)在离子晶体中,当 (阳离子)∶r(阴离子)
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为_______ ,造成AgI晶体结构不同于NaCl晶体结构的原因不可能是_______ (填标号)。
a.几何因素 b.电荷因素 c.键性因素
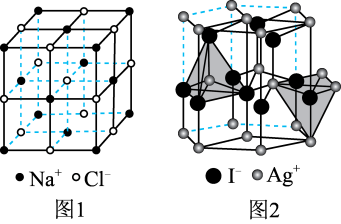
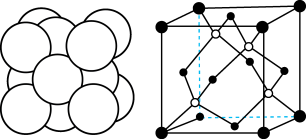
(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为_______ ;若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_______ (储氢能力 )
)
(1)Ag元素在元素周期表分区中属于
(2)硫代硫酸银(
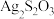 )是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(
)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠( )溶液生成
)溶液生成 等络阴离子。
等络阴离子。①依据
 理论推测
理论推测 的空间构型为
的空间构型为②在
 中配位原子是S原子而非O原子,其原因是
中配位原子是S原子而非O原子,其原因是(3)碘化银常用于做人工增雨剂。其中碘元素形成的最高价氧化物对应水化物有
 (偏高碘酸,不稳定)和
(偏高碘酸,不稳定)和 (正高碘酸)等多种形式,它们的酸性
(正高碘酸)等多种形式,它们的酸性
 (填“弱于”、“等于”或“强于”)。而
(填“弱于”、“等于”或“强于”)。而 、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是
、HBr、HCl的水溶液酸性的排序为由强到弱,其结构原因是(4)在离子晶体中,当
 (阳离子)∶r(阴离子)
(阳离子)∶r(阴离子) 时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知
时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知 ,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为
,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为a.几何因素 b.电荷因素 c.键性因素

(5)Cu与Au的某种合金可形成面心立方最密堆积的晶体(密度为
 ),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为
),在该晶胞中Cu原子处于面心,用NA表示阿伏加德罗常数的值。该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图)相似,该晶体储氢后的化学式为 )
)
您最近一年使用:0次
2022-04-25更新
|
1258次组卷
|
4卷引用:内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题
内蒙古包头市2022届高三第二次模拟考试理综试卷化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2022年高考化学临考题号押题(课标全国卷)(已下线)【直抵名校】01-备战2022年高考化学名校进阶模拟卷(通用版)河南省南阳市2021-2022学年高二下学期期末考试化学试题
名校
解题方法
4 . 铬及其化合物用途广泛。回答下列问题:
(1)基态Cr原子价电子排布式为____ ,有____ 个未成对电子。
(2)重铬酸铵[(NH4)2Cr2O7]为桔黄色单斜结晶,常用作有机合成催化剂, 的结构如图。(NH4)2Cr2O7 中N、O、Cr三种元素第一电离能由大到小的顺序是
的结构如图。(NH4)2Cr2O7 中N、O、Cr三种元素第一电离能由大到小的顺序是____ (填元素符号),1 mol该物质中含σ键的数目为_____ NA

(3)铬能形成多种配合物。
①配合物a、b、c的化学式如下:
a, [Cr(H2O)4Cl2]Cl∙2H2O b. [Cr(H2O)5Cl]Cl2∙H2O c. [Cr(H2O)6 ]Cl3
相同物质的量的a、b、c分别与足量AgNO3溶液反应,生成AgCl的物质的量之比为___ 。
②Reinecke salt的结构如图所示:

其中配位原子为__ (填元素符号);阳离子的空间结构为___ ,NCS-中碳原子杂化方式为___ 。
(4)一种半金属磁体的结构如图所示,其晶胞参数为a pm。

①距离每个Cr最近的Al有___ 个,距离Cr(0,0,0)最近的Co的原子坐标为____ 。
②该晶体的密度为___ g∙cm-3(NA表示阿伏加德罗常数的值)。
(1)基态Cr原子价电子排布式为
(2)重铬酸铵[(NH4)2Cr2O7]为桔黄色单斜结晶,常用作有机合成催化剂,
 的结构如图。(NH4)2Cr2O7 中N、O、Cr三种元素第一电离能由大到小的顺序是
的结构如图。(NH4)2Cr2O7 中N、O、Cr三种元素第一电离能由大到小的顺序是
(3)铬能形成多种配合物。
①配合物a、b、c的化学式如下:
a, [Cr(H2O)4Cl2]Cl∙2H2O b. [Cr(H2O)5Cl]Cl2∙H2O c. [Cr(H2O)6 ]Cl3
相同物质的量的a、b、c分别与足量AgNO3溶液反应,生成AgCl的物质的量之比为
②Reinecke salt的结构如图所示:

其中配位原子为
(4)一种半金属磁体的结构如图所示,其晶胞参数为a pm。

①距离每个Cr最近的Al有
②该晶体的密度为
您最近一年使用:0次
2021-03-14更新
|
1093次组卷
|
6卷引用:内蒙古海拉尔第二中学2021-2022学年高三上学期期末考试理科综合化学试题
5 . 铜及其化合物用途非常广泛,请回答下列问题:
(1)基态Cu+的核外电子排布式为______ 。
(2)Cu2+与 OH‑反应能生成 ,
, 中的配位原子是
中的配位原子是______ (填元素符号),配位数是______ 。
(3)胆矾的结构如图所示,其中既含有配位键,又含有氢键,则胆矾的化学式用配合物的形式可表示为______ 。1 mol胆矾所含σ键的数目为______ 。

(4)Cu与 Cl形成的一种化合物的立方晶胞如图所示。
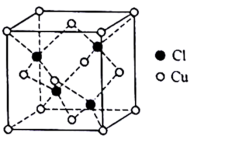
该化合物的化学式为______ ,已知晶胞参数a=0.542 nm,此晶体的密度为______ g·cm-3(写出计算式,不要求计算结果,阿伏加德罗常数的值为 NA)。
(1)基态Cu+的核外电子排布式为
(2)Cu2+与 OH‑反应能生成
 ,
, 中的配位原子是
中的配位原子是(3)胆矾的结构如图所示,其中既含有配位键,又含有氢键,则胆矾的化学式用配合物的形式可表示为

(4)Cu与 Cl形成的一种化合物的立方晶胞如图所示。

该化合物的化学式为
您最近一年使用:0次
2021-02-01更新
|
115次组卷
|
2卷引用:内蒙古自治区阿拉善盟第一中学2021-2022学年高二下学期期末考试化学试题



