1 .  是一种重要的盐,其水溶液中存在平衡:
是一种重要的盐,其水溶液中存在平衡: 。下列说法
。下列说法不正确 的是
 是一种重要的盐,其水溶液中存在平衡:
是一种重要的盐,其水溶液中存在平衡: 。下列说法
。下列说法A. 溶液中加入淀粉溶液,溶液显蓝色 溶液中加入淀粉溶液,溶液显蓝色 |
B. 溶液呈棕褐色溶液,加入 溶液呈棕褐色溶液,加入 后,振荡,上层溶液显紫红色 后,振荡,上层溶液显紫红色 |
C. 溶液中滴加少量 溶液中滴加少量 溶液,溶液酸性增强 溶液,溶液酸性增强 |
D.利用 溶液可以除去硫粉中的少量碘单质 溶液可以除去硫粉中的少量碘单质 |
您最近一年使用:0次
解题方法
2 . 下列说法不正确的是
| A.蒸馏、萃取、重结晶和色谱法都可用于分离、提纯有机物 |
| B.核苷酸通过缩聚反应可以得到核酸,核酸属于生物大分子 |
| C.根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花 |
| D.糖类都含有醛基,对氢氧化铜等弱氧化剂表现出还原性 |
您最近一年使用:0次
3 . 某化学小组模拟工业生产原理:以废铁屑(含少量 、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
已知:①乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇;该螯合型配合物稳定性好
②氢氧化铁沉淀通常呈胶体状态,有较强的吸附性
Ⅰ.制备乙二胺四乙酸铁钠晶体
实验原理:
实验流程:
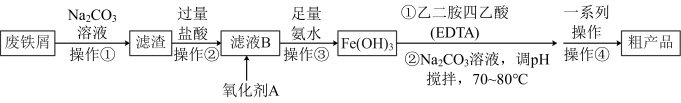
方案1:
(1)由 制乙二胺四乙酸铁钠可以选择
制乙二胺四乙酸铁钠可以选择_________ (填“酒精灯直接加热”或“水浴加热”)。
(2)氧化剂A可以选择 ,试写出该步反应的离子方程式
,试写出该步反应的离子方程式___________ 。
(3)下列说法正确的是___________ 。
A.为避免 沉淀中裹入过多杂质,可以采用一次性加入氨水
沉淀中裹入过多杂质,可以采用一次性加入氨水
B.该流程中两次用到 溶液,均可用
溶液,均可用 溶液代替
溶液代替
C.操作④洗涤时宜采用冷水洗涤
D.“一系列的操作”是指“蒸发浓缩,趁热过滤、洗涤、干燥”
E.乙二胺四乙酸铁钠溶液中滴入KSCN溶液不一定会显红色
方案2:用EDTA、 与
与 反应,制备乙二胺四乙酸铁钠,此法EDTA先被
反应,制备乙二胺四乙酸铁钠,此法EDTA先被 中和后再和
中和后再和 直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
(4)为使沉淀颗粒增大,实验中往往可以采取___________ (填实验条件)。
(5)方案2的缺点:产品中含杂质多,纯度不好。方案2后剩余废液可用层柱法(利用筛网孔径与微粒孔径不同的一种分离方法)可得到反应的副产物___________ (填名称)。
Ⅱ.测定所制取样品中铁的含量(EDTA标准溶液滴定法)
取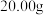 样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成
样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成 溶液,取出
溶液,取出 加入过量的
加入过量的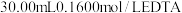 标准溶液并加热煮沸,充分反应后,再用
标准溶液并加热煮沸,充分反应后,再用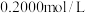 的
的 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液体积为
标准溶液体积为 。
。
已知: 、
、 与EDTA反应的化学计量比均为
与EDTA反应的化学计量比均为 。
。
(6)实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示___________。
(7)计算铁元素的质量分数___________ 。
 、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。
、Mn、C等杂质)为原料生产配合物乙二胺四乙酸铁钠(EDTA铁钠盐),并测定所制取的样品中铁元素的含量。已知:①乙二胺四乙酸铁钠,易溶于水和稀酸,微溶于乙醇;该螯合型配合物稳定性好
②氢氧化铁沉淀通常呈胶体状态,有较强的吸附性
Ⅰ.制备乙二胺四乙酸铁钠晶体
实验原理:

实验流程:
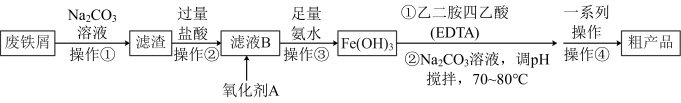
方案1:
(1)由
 制乙二胺四乙酸铁钠可以选择
制乙二胺四乙酸铁钠可以选择(2)氧化剂A可以选择
 ,试写出该步反应的离子方程式
,试写出该步反应的离子方程式(3)下列说法正确的是
A.为避免
 沉淀中裹入过多杂质,可以采用一次性加入氨水
沉淀中裹入过多杂质,可以采用一次性加入氨水B.该流程中两次用到
 溶液,均可用
溶液,均可用 溶液代替
溶液代替C.操作④洗涤时宜采用冷水洗涤
D.“一系列的操作”是指“蒸发浓缩,趁热过滤、洗涤、干燥”
E.乙二胺四乙酸铁钠溶液中滴入KSCN溶液不一定会显红色
方案2:用EDTA、
 与
与 反应,制备乙二胺四乙酸铁钠,此法EDTA先被
反应,制备乙二胺四乙酸铁钠,此法EDTA先被 中和后再和
中和后再和 直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。
直接反应。两个方案都有不足之处,方案1的缺点:氢氧化铁沉淀成胶体状态,难以过滤和洗涤。(4)为使沉淀颗粒增大,实验中往往可以采取
(5)方案2的缺点:产品中含杂质多,纯度不好。方案2后剩余废液可用层柱法(利用筛网孔径与微粒孔径不同的一种分离方法)可得到反应的副产物
Ⅱ.测定所制取样品中铁的含量(EDTA标准溶液滴定法)
取
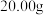 样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成
样品溶于水,然后将其中的铁元素用萃取剂从配合物中“反萃取”出来并配成 溶液,取出
溶液,取出 加入过量的
加入过量的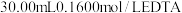 标准溶液并加热煮沸,充分反应后,再用
标准溶液并加热煮沸,充分反应后,再用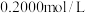 的
的 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液体积为
标准溶液体积为 。
。已知:
 、
、 与EDTA反应的化学计量比均为
与EDTA反应的化学计量比均为 。
。(6)实验室进行萃取操作时,需要打开分液漏斗活塞放气,正确的放气图示___________。
A.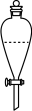 | B. | C.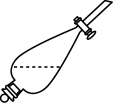 | D. |
(7)计算铁元素的质量分数
您最近一年使用:0次
解题方法
4 . 海水中蕴含着丰富的化学物质,可从海水中提取Na、Mg等物质,下列说法正确的是。
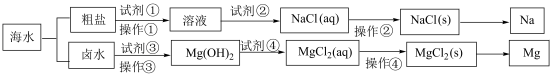
A.已知粗盐中含有 、 、 、 、 等杂质离子,试剂①可依次加入足量的 等杂质离子,试剂①可依次加入足量的 、 、 |
B.试剂②④均为盐酸,工业上试剂③为 溶液 溶液 |
| C.操作①③相同,操作②④完全相同 |
D.工业制Na、Mg的副产品 可循环使用 可循环使用 |
您最近一年使用:0次
2023-12-06更新
|
246次组卷
|
4卷引用:专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
(已下线)专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省金丽衢十二校2023-2024学年高三上学期联考模拟预测化学试题(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)福建省福州九师教学联盟2023-2024学年高一上学期1月联考化学试题
解题方法
5 . 下列说法正确的是
| A.只含有一个碳原子的有机物,不可能存在同分异构现象 |
| B.苯酚和苯甲酸的混合物,可通过蒸馏的方法进行分离 |
| C.乙烯在较高压力与较高温度和引发剂作用下,通过加聚反应可得到高密度聚乙烯 |
| D.由于氧的电负性比碳和氢要大,所以醇在发生化学反应时,H-O或C-O易断裂 |
您最近一年使用:0次
6 . 某研究小组用磷酸和碳酸钠制备 ,按如下流程开展实验。
,按如下流程开展实验。

已知:常温下 为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃,
为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃, 的电离常数:
的电离常数: ,
,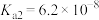 ,
,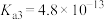 ;
; 的电离常数:
的电离常数: ,
, 。
。
回答下列问题:
(1)步骤Ⅱ蒸发浓缩时,将溶液转移至___________ (填仪器名称)进行加热。
(2)下列说法不正确 的是___________。
(3)步骤Ⅰ用pH试纸检测溶液的pH=4.2~4.6的具体操作如下,请将操作补充完整:将广泛pH试纸置于玻璃片上,用玻璃棒蘸取溶液点在试纸中部,与标准比色卡对照、读数;___________ 。
(4)一系列操作包括:操作A.洗涤和干燥。
①写出操作A的名称___________ 。
②洗涤时,下列洗涤剂最合适的是___________ (填序号)。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
(5)为测定 产品的纯度,可用已知浓度的NaOH标准溶液滴定。已知弱酸的浓度c和
产品的纯度,可用已知浓度的NaOH标准溶液滴定。已知弱酸的浓度c和 值满足
值满足 在
在 附近时,才能被准确的滴定,否则不能被滴定。
附近时,才能被准确的滴定,否则不能被滴定。
室温下称取产品试样3.900g溶于水并定容至250mL。取试样溶液25.00mL于锥形瓶中,用 的NaOH溶液滴定。平行滴定三次,平均消耗NaOH溶液20.00mL。该产品的纯度为
的NaOH溶液滴定。平行滴定三次,平均消耗NaOH溶液20.00mL。该产品的纯度为___________ %(保留小数点后两位)。
 ,按如下流程开展实验。
,按如下流程开展实验。
已知:常温下
 为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃,
为无色晶体,易溶于水,不溶于乙醇,熔点60℃,热至100℃时失去全部结晶水。磷酸易溶于乙醇。25℃, 的电离常数:
的电离常数: ,
,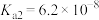 ,
,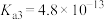 ;
; 的电离常数:
的电离常数: ,
, 。
。回答下列问题:
(1)步骤Ⅱ蒸发浓缩时,将溶液转移至
(2)下列说法
| A.步骤Ⅰ,碳酸钠固体宜缓慢分批加入 |
| B.步骤Ⅱ,蒸发浓缩时溶液出现大量晶体时停止加热 |
| C.步骤Ⅲ,洗涤时加入洗涤剂,并用玻璃棒轻轻搅拌 |
| D.步骤Ⅲ,干燥时宜采取真空干燥 |
(3)步骤Ⅰ用pH试纸检测溶液的pH=4.2~4.6的具体操作如下,请将操作补充完整:将广泛pH试纸置于玻璃片上,用玻璃棒蘸取溶液点在试纸中部,与标准比色卡对照、读数;
(4)一系列操作包括:操作A.洗涤和干燥。
①写出操作A的名称
②洗涤时,下列洗涤剂最合适的是
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
(5)为测定
 产品的纯度,可用已知浓度的NaOH标准溶液滴定。已知弱酸的浓度c和
产品的纯度,可用已知浓度的NaOH标准溶液滴定。已知弱酸的浓度c和 值满足
值满足 在
在 附近时,才能被准确的滴定,否则不能被滴定。
附近时,才能被准确的滴定,否则不能被滴定。室温下称取产品试样3.900g溶于水并定容至250mL。取试样溶液25.00mL于锥形瓶中,用
 的NaOH溶液滴定。平行滴定三次,平均消耗NaOH溶液20.00mL。该产品的纯度为
的NaOH溶液滴定。平行滴定三次,平均消耗NaOH溶液20.00mL。该产品的纯度为
您最近一年使用:0次
解题方法
7 . 下列说法正确的是
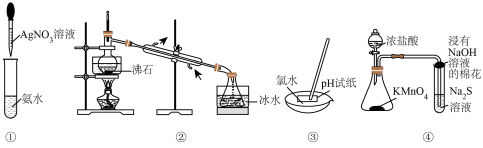
| A.图①操作配制银氨溶液 | B.图②装置可用于分离溴苯和苯 |
| C.图③操作测定氯水的pH | D.图④装置可用于比较Cl、S元素的非金属性 |
您最近一年使用:0次
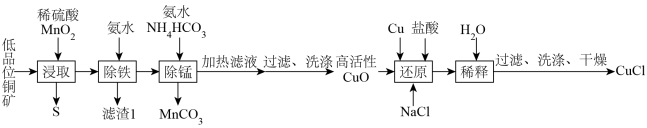
8 . 氯化亚铜(CuCl)是石油工业常用的脱硫剂和脱色剂,以低品位铜矿(主要成分为CuS。CuS2和铁的氧化物)为原料制备CuCl步骤如下: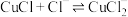 )。
)。
请回答:
(1)还原过程中所得产物的主要溶质的化学式是___________ 。
(2)下列有关说法不正确 的是___________。
(3)“稀释”过程中,pH对CuCl产率的影响如图所示: 左右的原因
左右的原因___________ 。
(4)为测定CuCl产品纯度进行如下实验:
a.称量所得CuCl产品 g溶于硝酸,配制成250mL溶液;取出
g溶于硝酸,配制成250mL溶液;取出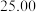 mL,加入足量的
mL,加入足量的 mL
mL  mol/L
mol/L  溶液,充分反应;
溶液,充分反应;
b.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
c.加入指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;
d.重复实验操作三次,消耗 mol/L
mol/L  溶液的体积平均为
溶液的体积平均为 mL。
mL。
已知 ,
,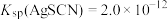 。
。
①加入硝基苯的作用是________ 。
②滴定选用的指示剂是________ 。
A. B.
B. C.
C. D.
D.
③CuCl的纯度为________ 。
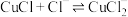 )。
)。请回答:
(1)还原过程中所得产物的主要溶质的化学式是
(2)下列有关说法
| A.“浸取”过程中稀硫酸可以用浓硫酸代替 |
B.滤渣1的成分是 |
C.“除锰”后的滤液中Cu元素主要以 形式存在 形式存在 |
D.“除锰”后滤液加热的主要目的是除去多余的氨水和 |
(3)“稀释”过程中,pH对CuCl产率的影响如图所示:
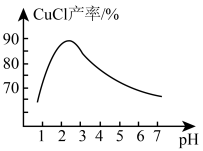
 左右的原因
左右的原因(4)为测定CuCl产品纯度进行如下实验:
a.称量所得CuCl产品
 g溶于硝酸,配制成250mL溶液;取出
g溶于硝酸,配制成250mL溶液;取出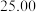 mL,加入足量的
mL,加入足量的 mL
mL  mol/L
mol/L  溶液,充分反应;
溶液,充分反应;b.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
c.加入指示剂,用
 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;d.重复实验操作三次,消耗
 mol/L
mol/L  溶液的体积平均为
溶液的体积平均为 mL。
mL。已知
 ,
,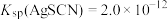 。
。①加入硝基苯的作用是
②滴定选用的指示剂是
A.
 B.
B. C.
C. D.
D.
③CuCl的纯度为
您最近一年使用:0次
9 . 实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
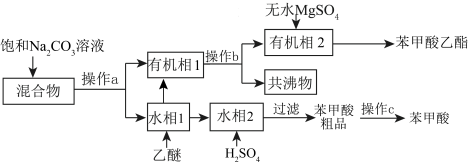
已知:苯甲酸乙酯的沸点为 ,“乙醚-环己烷-水共沸物”的沸点为
,“乙醚-环己烷-水共沸物”的沸点为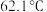 。
。
下列说法不正确 的是

已知:苯甲酸乙酯的沸点为
 ,“乙醚-环己烷-水共沸物”的沸点为
,“乙醚-环己烷-水共沸物”的沸点为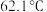 。
。下列说法
| A.操作a为分液,操作c为重结晶 | B.操作b中需用到直形冷凝管 |
| C.可用冷水洗涤苯甲酸粗品 | D.无水 可以用浓硫酸代替 可以用浓硫酸代替 |
您最近一年使用:0次
2023-11-15更新
|
1216次组卷
|
5卷引用:浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题
浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题03 化学实验基础(3大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题云南省红河哈尼族彝族自治州蒙自市第一高级中学2023-2024学年高二上学期12月月考化学试题(已下线)热点11 微型工艺流程
10 . 废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO2.某研究小组设计如图所示工艺流程制备硫酸镍晶体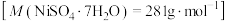 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
(1)“滤渣2”的成分是___________ (用化学式表示)。溶液中加入H2O2的目的是___________ (用离子方程式表示)。
(2)“调pH”可选用的物质___________ (填序号)。
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为___________ 。
(3)下列有关说法不正确 的是___________。
(4)测定产品的纯度。
计算产品的纯度为___________ 。
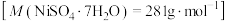 。
。
①镍的化学性质与铁相似,能与酸缓慢反应。
②一定条件下,一些金属氢氧化物沉淀时的pH如下表:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀的pH | 7.2 | 4.0 | 2.2 | 7.5 |
| 沉淀完全的pH | 9.0 | 5.6 | 3.2 | 9.0 |
(1)“滤渣2”的成分是
(2)“调pH”可选用的物质
A.Na2CO3 B.NiCO3 C.H2SO4 D.NiSO4
“调pH”的范围为
(3)下列有关说法
| A.酸浸步骤可用水浴加热,以加速反应 |
| B.操作A中的有机溶剂可选用乙醇 |
| C.调pH后过滤,需用玻璃棒对漏斗中的混合物充分搅拌 |
| D.操作B中包含“结晶、过滤、洗涤、煅烧”等操作 |
(4)测定产品的纯度。
| 操作步骤 | 涉及反应 |
| ①准确称取制备的硫酸镍样品5.620g,加入含0.0200molEDTA的二钠盐溶液(用H2Y2-表示),充分反应后定容成100mL。 | 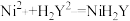 |
②取25.00mL上述溶液于锥形瓶中,加二甲酚橙作指示剂,用 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 标准液滴定到终点,平行实验三次,平均消耗20.00mLZn2+标准液。 |  |
您最近一年使用:0次



