名校
解题方法
1 . 亚硝酸钠(NaNO2)的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是____ ,装置乙的作用是____ 。
(2)甲中滴入稀硝酸前需先通入N2,原因是____ 。
(3)甲装置中发生反应的离子方程式为____ 。
(4)反应过程中观察到丙中的现象为___ 。
(5)丁中酸性KMnO4的作用是____ 。
(6)设计实验证明丙装置有NaNO2生成____ (写出操作、试剂和现象)。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是
(2)甲中滴入稀硝酸前需先通入N2,原因是
(3)甲装置中发生反应的离子方程式为
(4)反应过程中观察到丙中的现象为
(5)丁中酸性KMnO4的作用是
(6)设计实验证明丙装置有NaNO2生成
您最近一年使用:0次
2022-07-12更新
|
335次组卷
|
2卷引用:江西省抚州市2021-2022学年高一下学期期末考化学试题
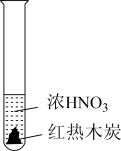
2 . 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
| ① | ② | ③ |
| A.由①中的红棕色气体,推断产生的气体一定是混合气体 |
| B.由②中的红棕色气体不能表明木炭与浓硝酸发生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 |
| D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应 |
您最近一年使用:0次
2022-06-29更新
|
3784次组卷
|
81卷引用:江西省吉安市2021-2022学年高二下学期期末检测化学试题
江西省吉安市2021-2022学年高二下学期期末检测化学试题河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省衡水中学2018届高三上学期一调考试化学试题山东省淄博第一中学2018届高三上学期开学考试化学试题四川省德阳市三校2018届高三联合测试化学试题(已下线)黄金30题系列 高一化学 小题好拿分【提升版】北京市清华大学附属中学2018届高三10月月考化学试题广西陆川县中学2018届高三12月月考化学试题北京市一零一中学2018届高三10月月考化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题云南省峨山彝族自治县第一中学2018届高三上学期期末考试仿真化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题河南省三门峡市2017-2018学年高一上学期期末考试化学试题广西陆川县中学2018届高三3月月考化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】云南省玉溪市峨山一中2019届高三9月月考化学试题江苏省常州市第一中学2019届高三第一学期期初(8月)考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一下学期2月模块诊断化学试题福建省泉州市泉港区第一中学2018-2019学年高一下学期期中考试化学试题百所名校联考-非金属及其化合物内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题(已下线)2019年12月11日 《每日一题》化学人教版(必修1)——硝酸的强氧化性2020届高三化学二轮冲刺新题专练——硝酸的性质及应用(提升练)贵州省黔南布依族苗族自治州龙里中学2019-2020学年高三上学期期末考试理综化学试题贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题(已下线)专题3.5 氮及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》福建省福州市第一中学2020年高一在线自测自评质检化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷安徽省六安市舒城中学2019-2020学年高一下学期第一次月考化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第12讲 氮及其化合物-2021年高考化学一轮复习名师精讲练2019年上海市高中生化学竞赛初赛试题(“华理一化工杯”)初赛试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关高一必修第一册(鲁科2019)第3章 第3节 氮的循环 高考帮(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)湖南省长沙市雅礼中学2021届高三上学期第一次月考化学试题北京一零一中2021届高三上学期第三次统练化学试题(已下线)【浙江新东方】48安徽省滁州市定远县重点中学2021届高三上学期11月质量检测化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】陕西省西安市长安区第一中学2019-2020学年高一上学期期末考试化学试题专题7 第一~二单元 综合拔高练-高中化学必修第二册苏教版2019(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物(已下线)【浙江新东方】高中化学20210304-015黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题浙江省诸暨市2021届高三5月适应性考试化学试题福建省泉州科技中学2020-2021学年高一下学期期中考试化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区安徽省芜湖市2020-2021学年高一下学期期末质量检测联考化学试题(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第12讲 氮及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)河南部分学校2022届新高三8月份摸底联考化学试题北京市中国农业大学附属中学2020-2021学年高一上学期期末学业水平调研化学试题(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)课后-5.2.3 硝酸 酸雨及防治-人教2019必修第二册云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题辽宁省沈阳市第二十中学2019-2020学年高一下学期第一次月考化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 氮及其化合物(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高一下学期第一次阶段化学试题北京市首师附密云中学2021-2022学年高一下学期等级考化学试题山东省菏泽市单县第二中学2021-2022学年高一上学期(实验班)12月段考化学试题第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系巩固训练12(已下线)题型61 硝酸、硝酸盐的性质安徽省合肥市第一中学2022-2023学年高一下学期第4次月考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
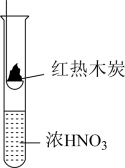
3 . 熔融的金属锡(熔点231℃)在300℃左右能直接与氯气作用生成无水四氯化锡:Sn+2Cl2 SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
回答下列问题:
(1)装置A中烧瓶内反应的离子方程式为____ ;仪器①中导管的作用是___ 。
(2)B、C、F、G盛装的试剂应依次选用下列中的____ (填标号)。
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)取少量Sn片切成丝状,放入D装置反应器②中。冷阱③和小烧杯⑤内都装入冷水,按图将仪器连接好后,再一次检验整个装置,确证系统不漏气。先打开恒压滴液漏斗活塞使反应发生,排尽装置中的空气后,再加热D装置中试管②使Sn丝熔化,并与Cl2发生反应。能说明装置中的空气被排尽的现象是____ ;生成的SnCl4经冷凝后,收集于E装置的试管④中,该液体常常呈黄绿色,原因是___ 。
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和____ (填化学式)。
(5)0.500gSn完全反应,制得SnCl41.03g,产率为____ 。
 SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
SnCl4。纯SnCl4是无色液体(沸点114℃),在空气中极易水解生成SnO2•xH2O。某化学小组利用如图装置制备SnCl4,并对其性质进行探究。
回答下列问题:
(1)装置A中烧瓶内反应的离子方程式为
(2)B、C、F、G盛装的试剂应依次选用下列中的
a.浓H2SO4 b.饱和NaHCO3溶液 c.饱和NaCl溶液 d.NaOH浓溶液
(3)取少量Sn片切成丝状,放入D装置反应器②中。冷阱③和小烧杯⑤内都装入冷水,按图将仪器连接好后,再一次检验整个装置,确证系统不漏气。先打开恒压滴液漏斗活塞使反应发生,排尽装置中的空气后,再加热D装置中试管②使Sn丝熔化,并与Cl2发生反应。能说明装置中的空气被排尽的现象是
(4)用玻璃棒蘸取少量产物SnCl4,放置在空气中,片刻即产生白色烟雾,产物为SnO2•xH2O和
(5)0.500gSn完全反应,制得SnCl41.03g,产率为
您最近一年使用:0次
2022-06-25更新
|
277次组卷
|
4卷引用:江西省宜春市丰城市2022-2023学年高二上学期期中考试化学试题
解题方法
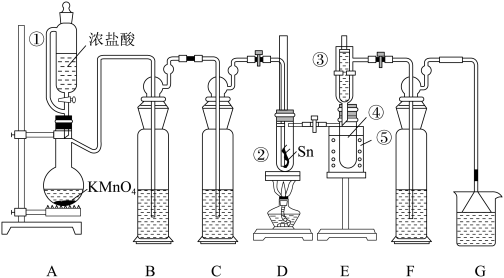
4 . 次氯酸(HClO)的浓溶液呈黄色,是极强氧化剂,常用作消毒剂及除甲醛(HCHO)的试剂。某学习小组设计下列装置制备HClO并验证其氧化性(夹持仪器及降温装置已省略)。
已知:Cl2O为棕黄色气体,极易溶于水并迅速反应生成HClO。
回答下列问题:
(1)HClO的结构式为____ ,仪器a的名称为____ 。
(2)制备HClO时要打开活塞K1、K3,关闭K2,待装置A中反应结束时再通入一段时间N2。
①仪器C中制备Cl2O时,发生反应的化学方程式为2Cl2+2Na2CO3+H2O-=Cl2O+2NaCl+2____ (填化学式),仪器B、D中的试剂分别为____ (填字母)。
a.浓H2SO4、CCl4
b.饱和食盐水、CCl4
c.饱和食盐水、浓H2SO4
②反应结束后再通入一段时间N2的目的是____ 。
(3)验证HClO的氧化性时要向F中加入过量HClO并充分搅拌,待溶液变澄清时停止搅拌。
①将E中HClO溶液转移到F中的具体操作为____ (答出对开关的操作)。
②反应结束时,F的溶液中含有的离子主要有Fe3+、Cl-、SO 、H+,该反应的离子方程式为
、H+,该反应的离子方程式为____ 。
(4)HClO可用于除去HCHO,生成一种常见强酸和两种常见无污染的氧化物。
①该反应的化学方程式为____ 。
②若除去15gHCHO,则转移电子的个数为____ NA(NA表示阿伏加德罗常数)。
已知:Cl2O为棕黄色气体,极易溶于水并迅速反应生成HClO。

回答下列问题:
(1)HClO的结构式为
(2)制备HClO时要打开活塞K1、K3,关闭K2,待装置A中反应结束时再通入一段时间N2。
①仪器C中制备Cl2O时,发生反应的化学方程式为2Cl2+2Na2CO3+H2O-=Cl2O+2NaCl+2
a.浓H2SO4、CCl4
b.饱和食盐水、CCl4
c.饱和食盐水、浓H2SO4
②反应结束后再通入一段时间N2的目的是
(3)验证HClO的氧化性时要向F中加入过量HClO并充分搅拌,待溶液变澄清时停止搅拌。
①将E中HClO溶液转移到F中的具体操作为
②反应结束时,F的溶液中含有的离子主要有Fe3+、Cl-、SO
 、H+,该反应的离子方程式为
、H+,该反应的离子方程式为(4)HClO可用于除去HCHO,生成一种常见强酸和两种常见无污染的氧化物。
①该反应的化学方程式为
②若除去15gHCHO,则转移电子的个数为
您最近一年使用:0次
名校
解题方法
5 . 实验小组制备硫代硫酸钠并探究其性质。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2↑,制备硫代硫酸钠,装置如图。
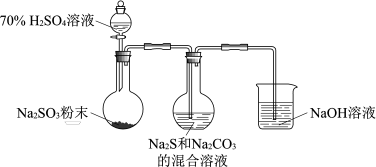
①加入化学试剂之前,应____ ,烧杯中NaOH溶液主要作用是____ 。
②用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:____ 、____ 。
③为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:____ (写出一条)。
(2)探究Na2S2O3的性质:
实验小组研究S产生的原因:(已知:Na2S2O3中S元素的化合价分别为-2和+6价)
假设1:
假设2:空气中的O2氧化了-2价硫元素
假设3:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素
设计实验方案:
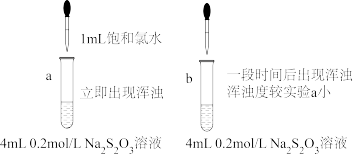
①假设1为____ 。
②向试管b中加入____ 。
③依据现象,S产生的主要原因是____ 。
④步骤3,继续加入氯水,沉淀消失的原因是____ (写化学方程式)。
(1)实验室可利用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2↑,制备硫代硫酸钠,装置如图。

①加入化学试剂之前,应
②用化学用语解释Na2S和Na2CO3的混合溶液呈碱性的原因:
③为了保证Na2S2O3的产量,实验中通入的SO2不能过量。要控制SO2的生成速率,可以采取的措施有:
(2)探究Na2S2O3的性质:
| 步骤1 | 取Na2S2O3晶体溶解,配成0.2 mol/L溶液。 |
| 步骤2 | 取4 mL溶液,向其中加入1 mL饱和氯水(pH=2.4),溶液立即出现浑浊,经检验浑浊物为S |
| 步骤3 | 继续滴加氯水,浑浊度增大,最后消失,溶液变澄清。 |
假设1:
假设2:空气中的O2氧化了-2价硫元素
假设3:Cl2、HClO等含氯的氧化性微粒氧化了-2价硫元素
设计实验方案:

①假设1为
②向试管b中加入
③依据现象,S产生的主要原因是
④步骤3,继续加入氯水,沉淀消失的原因是
您最近一年使用:0次
解题方法
6 . 下图是制备和研究乙炔性质的实验装置图,有关说法不正确的是
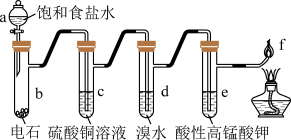

| A.d、e中溶液褪色的原理不同 |
| B.c(过量)的作用是除去影响后续实验的杂质 |
| C.用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净 |
| D.f处产生明亮、伴有浓烟的火焰 |
您最近一年使用:0次
名校
解题方法
7 . 某化学小组为测定有机物G的组成和结构,设计如图实验装置:
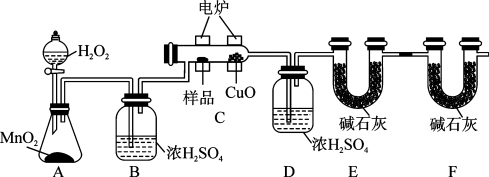
回答下列问题:
(1)实验开始时,先打开分液漏斗活塞,一段时间后再加热反应管C,目的是_______ 。
(2)装置B和装置D中浓硫酸的作用分别是_______ 和_______ 。
(3)装置E和装置F中碱石灰的作用分别是_______ 和_______ 。
(4)若准确称取2.2g样品G(只含C、H、O三种元素),经充分燃烧后(CuO的作用是确保有机物充分氧化,最终生成CO2和H2O),装置D质量增加1.8g,U形管E质量增加4.4g。又知有机物G的质谱图如图所示。

该有机物的分子式为_______ 。
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为1:1:6。综上所述,G的结构简式为_______ 。

回答下列问题:
(1)实验开始时,先打开分液漏斗活塞,一段时间后再加热反应管C,目的是
(2)装置B和装置D中浓硫酸的作用分别是
(3)装置E和装置F中碱石灰的作用分别是
(4)若准确称取2.2g样品G(只含C、H、O三种元素),经充分燃烧后(CuO的作用是确保有机物充分氧化,最终生成CO2和H2O),装置D质量增加1.8g,U形管E质量增加4.4g。又知有机物G的质谱图如图所示。

该有机物的分子式为
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为1:1:6。综上所述,G的结构简式为
您最近一年使用:0次
2022-05-28更新
|
322次组卷
|
9卷引用:江西省铜鼓中学2022-2023学年高二下学期4月月考化学试题
江西省铜鼓中学2022-2023学年高二下学期4月月考化学试题陕西省西安市长安区第一中学2020-2021学年高二上学期期末考试化学(理)试题(已下线)1.2 研究有机化合物的一般方法(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)专题二 研究有机化合物的一般方法-2020-2021学年高二《新题速递·化学》(人教版2019选择性必修3)2月刊 (同步课堂必刷题)(已下线)1.2.2 确定有机化合物的实验式与分子结构-2020-2021学年高二化学课时同步练(人教版2019选择性必修3)湖北省部分示范高中六校联考2021-2022学年高二下学期期中考试化学试题江苏省盐城市响水中学2021-2022学年高一下学期第二次学情分析考试化学试题安徽省蚌埠市第二中学2022-2023学年高一上学期第一次月考化学试题广东省广州市第十六中学2022-2023学年高二下学期5月月考化学试题
名校
解题方法
8 . 部分含氮物质的“价—类”二维图如下:
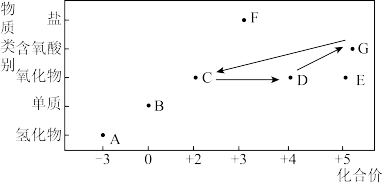
根据图示信息,回答下列问题:
(1)E的化学式为_______ 。写出B的用途:_______ (列举一种)。
(2)在常温条件下实现 的循环转化,其中有颜色变化且属于化合反应的化学方程式为
的循环转化,其中有颜色变化且属于化合反应的化学方程式为_______ 。
(3)实验室可选择甲、乙装置制备A,利用收集的A用丙装置探究A的性质。
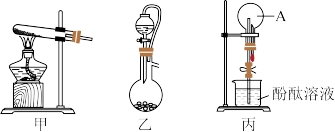
①若选择乙制备A,则反应物是_______ (填名称)。
②若选择甲装置制备A,则化学方程式为_______ 。
③若顺利完成丙装置实验,可观察到_______ 色喷泉。
(4)若F是一种钠盐,取少量F溶于蒸馏水,将溶液分成两份,进行实验,测得结果如下:
已知 水溶液呈无色,由此推断,F具有_______(填字母)。
水溶液呈无色,由此推断,F具有_______(填字母)。

根据图示信息,回答下列问题:
(1)E的化学式为
(2)在常温条件下实现
 的循环转化,其中有颜色变化且属于化合反应的化学方程式为
的循环转化,其中有颜色变化且属于化合反应的化学方程式为(3)实验室可选择甲、乙装置制备A,利用收集的A用丙装置探究A的性质。

①若选择乙制备A,则反应物是
②若选择甲装置制备A,则化学方程式为
③若顺利完成丙装置实验,可观察到
(4)若F是一种钠盐,取少量F溶于蒸馏水,将溶液分成两份,进行实验,测得结果如下:
| 实验 | 操作 | 现象 |
| Ⅰ | 向一份溶液中滴加稀硫酸酸化的 溶液,再滴加淀粉溶液,振荡 溶液,再滴加淀粉溶液,振荡 | 溶液由无色变为蓝色 |
| Ⅱ | 向另一份溶液中滴加少量的稀硫酸酸化的 溶液,振荡 溶液,振荡 | 溶液由紫红色变为无色 |
 水溶液呈无色,由此推断,F具有_______(填字母)。
水溶液呈无色,由此推断,F具有_______(填字母)。| A.氧化性 | B.还原性 | C.既有氧化性,又有还原性 | D.既无氧化性,又无还原性 |
您最近一年使用:0次
9 . Y形管是一种特殊的仪器。与其他仪器组合可以进行某些实验探究。利用如图装置可以探究 与
与 反应生成白色沉淀的条件。下列判断错误的是
反应生成白色沉淀的条件。下列判断错误的是
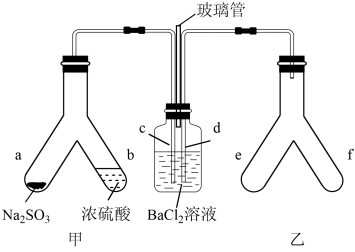
 与
与 反应生成白色沉淀的条件。下列判断错误的是
反应生成白色沉淀的条件。下列判断错误的是
A.e、f两管中的试剂可以分别是浓氨水和 固体 固体 |
| B.玻璃管的作用是连通大气,平衡压强 |
C.c、d两根导管可以插入 溶液中,保证气体与 溶液中,保证气体与 充分接触 充分接触 |
D.Y形管乙中产生的可能为氧化性气体,将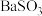 氧化为 氧化为 沉淀 沉淀 |
您最近一年使用:0次
名校
10 . 氨气是重要的化工原料,在工农业生产中有重要用途。
(1)工业上合成氨的反应原理为_______ 。
(2)氨气极易溶于水,这个性质可以利用如图装置进喷泉实验。
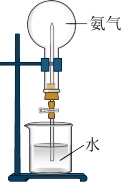
①完成喷泉实验的具体操作为_______ 。
②若该条件为标准状况,且水充满整个圆底烧瓶,则最终所得溶液的物质的量浓度为_______ 。
某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程。NH3的转化过程如图1所示。
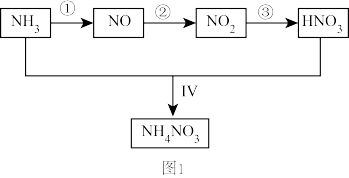
甲、乙两同学分别按图2所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30% H2O2溶液、蒸馏水、NaOH固体、MnO2。
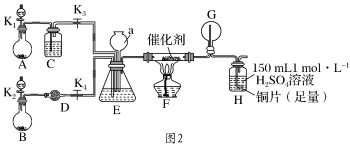
(3)装置A的圆底烧瓶中发生反应的化学方程式为_______ 。装置E有多种作用,下列关于装置E的作用或其中所盛液体的说法中,不正确的是_______ (填字母)。
a.使氨气和氧气充分混合
b.控制通入氨气和氧气的体积比
c.平衡装置内的压强
d.锥形瓶内液体是饱和食盐水
(4)甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,装置H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为_______ ,若制得的氨气仅按①→②→③的顺序完全转化为硝酸,欲使装置H中所得溶液为纯净的CuSO4溶液,理论上所需氨气在标准状况下的体积为_______ L(假设硝酸与铜反应产生的还原产物全部排出反应装置)。
(5)乙同学为模拟过程Ⅳ的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是_______ (填字母)。
a.关闭K3并熄灭酒精灯
b.关闭K4并熄灭酒精灯
c.关闭K3、K4并熄灭酒精灯
(6)丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷_______ 。
(1)工业上合成氨的反应原理为
(2)氨气极易溶于水,这个性质可以利用如图装置进喷泉实验。

①完成喷泉实验的具体操作为
②若该条件为标准状况,且水充满整个圆底烧瓶,则最终所得溶液的物质的量浓度为
某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程。NH3的转化过程如图1所示。

甲、乙两同学分别按图2所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30% H2O2溶液、蒸馏水、NaOH固体、MnO2。

(3)装置A的圆底烧瓶中发生反应的化学方程式为
a.使氨气和氧气充分混合
b.控制通入氨气和氧气的体积比
c.平衡装置内的压强
d.锥形瓶内液体是饱和食盐水
(4)甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,装置H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为
(5)乙同学为模拟过程Ⅳ的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是
a.关闭K3并熄灭酒精灯
b.关闭K4并熄灭酒精灯
c.关闭K3、K4并熄灭酒精灯
(6)丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷
您最近一年使用:0次
2022-04-14更新
|
114次组卷
|
2卷引用:江西省宜春市上高二中2021-2022学年高一下学期第七次月考化学试题