4. 合成氨是人类科学技术发展史上的一项重大突破,研究表明液氨是一种良好的储氢物质。
(1)化学家Gethard Ertl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意如下图:
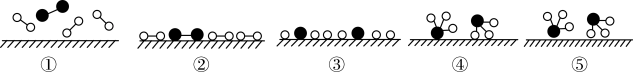
下列说法正确的是
____(选填字母)。
A.①表示N
2、H
2分子中均是单键
B.②→③需要吸收能量
C.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(2)氨气分解反应的热化学方程式如下:2NH
3(g)

N
2(g)+3H
2(g)
△H,若N三N键、H一H键和N一H键的键能分别记作
a、b和c(单位:kJ·mol
-l),则上述反应的
△H=
___kJ·mol
一1。
(3)研究表明金属催化剂可加速氨气的分解。下表为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率(m mol.min
一1)。
| 催化剂 | Ru | Rh | Ni | Pt | Pd | Fe |
| 初始速率 | 7.9 | 4.0 | 3.0 | 2.2 | 1.8 | 0.5 |
①不同催化剂存在下,氨气分解反应活化能最大的是
___(填写催化剂的化学式)。
②温度为T,在一体积固定的密闭容器中加入2 molNH
3,此时压强为P
0,用Ru催化氨气分解,若平衡时氨气分解的转化率为50%,则该温度下反应2NH
3(g)

N
2(g)十3H
2(g)用平衡分压代替平衡浓度表示的化学平衡常数K
p=
___。[已知:气体分压(p
分)=气体总压(p
总)x体积分数]
(4)关于合成氨工艺的理解,下列正确的是
___。
A.合成氨工业常采用的反应温度为500℃左右,可用勒夏特列原理解释
B.使用初始反应速率更快的催化剂Ru,不能提高平衡时NH
3的产量
C.合成氨工业采用10 MPa一30 MPa,是因常压下N
2和H
2的转化率不高
D.采用冷水降温的方法可将合成后混合气体中的氨液化
(5)下图为合成氨反应在不同温度和压强、使用相同催化剂条件下,初始时氮气、氢气的体积比为1:3时,平衡混合物中氨的体积分数[

(NH
3)]。
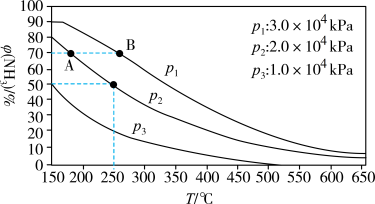
①若分别用v
A(NH
3)和v
B(NH
3)表示从反应开始至达平衡状态A、B时的化学反应速率,则v
A(NH
3)
____v
B(NH
3)(填“>”、“<”或“=”)。
②在250℃、1.0×10
4kPa下,H
2的转化率为
______%(计算结果保留小数点后1位)。
(6)N
2和H
2在铁作催化剂作用下从145℃就开始反应,随着温度上升,单位时间内NH
3产率增大,但温度高于900℃后,单位时间内NH
3产率逐渐下降的原因
________。