江苏省盐城市2021届高三上学期期中考试化学试题
江苏
高三
期中
2020-11-18
553次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.利用二氧化碳和环氧化合物合成可生物降解塑料 |
| B.开发光、电催化技术用H2O和O2直接合成H2O2 |
| C.推进大气污染治理、固体废物处置和资源化利用 |
| D.发展用水代替有机溶剂作为物质制备的分散介质 |
【知识点】 能源的充分利用解读 绿色化学与可持续发展解读
A.中子数为12的钠原子: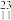 Na Na | B.N2H4的结构式: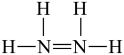 |
C.Cl-的结构示意图: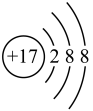 | D.NaClO的电子式: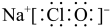 |
| A.FeSO4易溶于水,可用于制造红色颜料 |
| B.FeS是黑色粉末,可用于去除水体中Cu2+等重金属 |
| C.Fe2(SO4) 3水溶液显酸性,可用于去除天然气中H2S |
| D.Fe在冷的浓硫酸中钝化,可用于制造贮存浓硫酸的贮罐 |
【知识点】 铁盐 铁的其他化合物 几种铁的氧化物的物理性质及用途解读 铁的钝化
A.0.1mol·L-1HCl溶液:Al3+、Fe2+、SO 、Br- 、Br- |
B.0.1mol·L-1Ca(ClO)2溶液:K+、H+、Cl-、SO |
C.0.1mol·L-1Ba(OH)2溶液:Na+、NH 、NO 、NO 、HCO 、HCO |
D.0.1mol·L-1NaHSO3溶液:NH 、K+、CH3COO-、MnO 、K+、CH3COO-、MnO |
【知识点】 离子反应的发生条件解读 离子共存 限定条件下的离子共存解读
 、
、 、
、 、
、 及
及 )中回收
)中回收 并制
并制 ,氯化铁受热易升华,下列图示装置和原理不能达到实验目的的是
,氯化铁受热易升华,下列图示装置和原理不能达到实验目的的是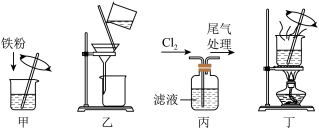
| A.用装置甲从废液中还原出Cu |
| B.用装置乙进行固液分离 |
C.用装置丙将 氧化为 氧化为 |
D.用装置丁将丙中反应后的溶液蒸干制取 |
【知识点】 化学实验基础操作解读 物质分离、提纯综合应用解读
| A.Cu与稀硝酸反应生成NO |
| B.Fe与H2O(g)加热生成Fe2O3 |
| C.Mg在CO2中燃烧生成MgCO3 |
| D.室温下,氨水中通入过量SO2生成(NH4)2SO3 |
| A.Na加入H2O中:Na + 2H2O=Na+ + 2OH-+ H2↑ |
| B.Fe(CH3COO)2溶液中加入稀硝酸:CH3COO-+H+ = CH3COOH |
C.[Ag(NH3)2]OH溶液中加入过量盐酸:[Ag(NH3)2]+ +OH- +3H+ +Cl-=AgCl↓+2NH +H2O +H2O |
D.Na2SO3溶液中通入过量Cl2:3SO +Cl2 + H2O = 2HSO +Cl2 + H2O = 2HSO +2Cl-+SO +2Cl-+SO |
【知识点】 离子反应的发生及书写 离子方程式的书写解读 离子方程式的正误判断解读
 HCN(g)+H2(g)。下列叙述正确的是
HCN(g)+H2(g)。下列叙述正确的是A.该反应的 <0、 <0、 <0 <0 |
B.该反应的平衡常数K =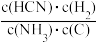 |
| C.单位时间内断裂N-H键数目是断裂H-H键数目的3倍时,该反应达到平衡状态 |
| D.强热下该反应每生成22.4LHCN气体转移电子数目为2×6.02×1023 |
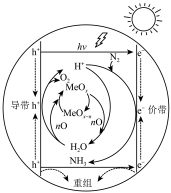
| A.光能转变为化学能 |
| B.H+是反应的中间体 |
| C.导带上发生的反应为2H2O +4h+= 4H++ O2↑ |
D.该过程总反应可表示为N2 +3H2 2NH3 2NH3 |
【知识点】 氧化还原反应方程式的配平解读 氧化还原反应的规律解读 能量的相互转化
| A.原子半径:r(Y)>r(Z)>r(X) |
| B.简单气态氢化物的热稳定性:X>Z>W |
| C.X、Y形成的化合物中一定不含共价键 |
| D.Z的氧化物的水化物与W的氧化物的水化物之间一定不能发生反应 |
二、多选题 添加题型下试题

| A.分子中有3种含氧官能团 |
| B.分子中有2个手性碳原子 |
| C.1mol该化合物至多与1molBr2发生反应 |
| D.1mol该化合物至多与含2mol NaOH的水溶液反应 |
三、单选题 添加题型下试题
选项 | 实验操作和现象 | 结论 |
A | 向盛有BaCl2溶液的试管中通入SO2,振荡,出现白色沉淀 | 白色沉淀为BaSO4 |
B | 向含碘废液X中加入FeCl3溶液,振荡,滴入淀粉溶液变蓝 | X中一定含有I- |
C | 向盛有乙醇的试管中放入新切的钠块,平缓放出气体,钠块未熔化 | 钠与乙醇的反应为吸热反应 |
D | 向试管中加入2mL10%CuSO4溶液,滴入4~5滴5%NaOH溶液,加入2mL10%麦芽糖溶液,加热,无红色沉淀 | 麦芽糖无还原性 |
| A.A | B.B | C.C | D.D |
四、多选题 添加题型下试题

下列说法
| A.H2A的Ka1=1×10-4 |
| B.溶液在X点和Z点时水的电离程度相同 |
| C.在Y点时,c(Na+)>3c(A2-) |
| D.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(H2A)>c(A2-) |
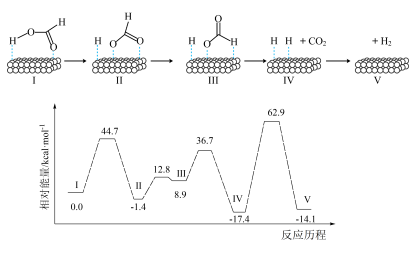
下列说法正确的是
A.在Pd催化剂表面HCOOH脱氢反应的 H >0 H >0 |
| B.在Pd催化剂表面离解O-H键比C-H键的活化能低 |
| C.在历程Ⅰ~Ⅴ中,生成Ⅴ的反应速率最慢 |
| D.用DCOOH或HCOOD代替HCOOH,得到的产物都有HD和CO2 |
五、解答题 添加题型下试题

(1)工业上常用NaOH溶液与Cl2反应制备NaClO。Cl2与冷的NaOH溶液反应的离子方程式为
(2)NaClO溶液在空气中易失效,其与空气中CO2反应的化学方程式为
(3)NaClO溶液可用于脱除黄磷生产尾气中PH3等有害气体。脱除PH3机理为:
H3O+ + ClO-= HClO + H2O
PH3 + HClO= [PH3O] + H++Cl-
[PH3O]+ClO-= H3PO2 + Cl-
室温下,用3%的NaClO溶液分别在pH=9、pH=11时处理含PH3的尾气,PH3的脱除率如图-3所示:

①下列措施能提高尾气中PH3的脱除率的是
A.增大尾气的流速
B.将吸收液加热到40℃以上
C.采用气、液逆流的方式吸收尾气
D.吸收尾气的过程中定期补加适量NaClO并调节合适的溶液pH
②已知PH3几乎不与NaOH溶液反应,黄磷生产尾气中除PH3外,还有大量的H2S等有害气体。黄磷尾气通过NaClO吸收液前需预先用30%NaOH溶液吸收处理,其目的是
③pH=9时PH3的脱除率总是比pH=11的大,其原因是
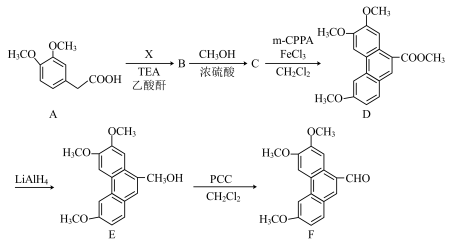
注:PCC为吡啶和CrO3在盐酸溶液中的络合盐,CH2=CHCH2OH
 CH2=CHCHO。
CH2=CHCHO。(1)A中的含氧官能团名称为
(2)X的分子式为C8H8O2,C→D是两苯环间脱2H成稠环,则X的结构简式为
(3)B→C的反应类型为
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①分子中只有两种含氧官能团。
②碱性水解后酸化,得到碳原子数相等的芳香化合物P和Q;P既能发生银镜反应又能与FeCl3溶液发生显色反应;P、Q中均只有四种不同化学环境的氢。
(5)写出以
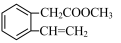 为原料制备
为原料制备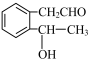 的合成路线流程图
的合成路线流程图(1)Co基态核外电子排布式为
(2)NO
 的空间结构为
的空间结构为(3)bte的分子式为C6H8N6,其结构简式如图所示。
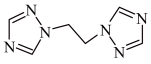
①[Co(bte)2(H2O)2]2+中,与Co2+形成配位键的原子是
②C、H、N的电负性从大到小顺序为
③bte分子中碳原子轨道杂化类型为
④1mol bte分子中含
 键的数目为
键的数目为
(1)700℃“焙烧”可使Cr2O3不溶于酸,焙烧的另一目的是
(2)配制“酸洗”所用100mL6mol·L-1硫酸需要的玻璃仪器有:量筒、烧杯、100mL容量瓶、
(3)为确定xNa2SO4·yCr2(SO4)3·zH2O的组成,进行下列实验:①称取样品1.9320g溶于水,加入足量盐酸酸化的BaCl2溶液,得到1.8640g沉淀。②另称取样品1.9320g溶于水,经H2O2在碱性条件下氧化、煮沸、酸化得Na2Cr2O7和Na2SO4的混合酸性溶液;加入稍过量的KI溶液(Cr2O
 +6I-+14H+ = 2Cr3++3I2+7H2O),暗处静置5min,立刻用0.5000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至溶液呈浅黄色,再加入1mL淀粉溶液,继续滴定至溶液蓝色刚好消失,消耗Na2S2O3溶液24.00mL。
+6I-+14H+ = 2Cr3++3I2+7H2O),暗处静置5min,立刻用0.5000mol·L-1Na2S2O3标准溶液滴定(2Na2S2O3+I2=2NaI+Na2S4O6)至溶液呈浅黄色,再加入1mL淀粉溶液,继续滴定至溶液蓝色刚好消失,消耗Na2S2O3溶液24.00mL。根据上述实验数据,确定xNa2SO4·yCr2(SO4)3·zH2O的化学式
(4)已知反应2[Cu(NH3)4]2+ + N2H4·H2O +4OH-= 2Cu↓+ N2↑+ 8NH3 + 5H2O。请补充完整由CuSO4溶液制备纯净铜粉的实验方案:
(1)Dennis等设计的电化学膜法脱除SO2的工艺如图-1所示。

多孔阳极上发生的电极反应为
2S2O
 +2e-=3SO
+2e-=3SO +SO2(g) 、
+SO2(g) 、 = 2S2O
= 2S2O 。
。(2)研究FeSO4液相催化氧化脱硫的实验流程如图-2所示,循环槽中循环液的pH变化如图-3所示(起始时在脱硫塔中加入9LFeSO4溶液并向循环槽中鼓入空气5min)。

①图-2中设置分析取样点A和B的目的是
②脱硫塔中发生的主要反应为
③图-3中430min后脱硫率基本稳定在93.5%左右的原因是
【知识点】 二氧化硫的化学性质 二氧化硫与氧气的反应解读 电解原理的应用
试卷分析
试卷题型(共 20题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 能源的充分利用 绿色化学与可持续发展 | |
| 2 | 0.94 | 化学用语综合判断 原子结构示意图、离子结构示意图 有机物的结构式、结构简式、比例模型、球棍模型、最简式 原子中相关数值及其之间的相互关系 | |
| 3 | 0.85 | 铁盐 铁的其他化合物 几种铁的氧化物的物理性质及用途 铁的钝化 | |
| 4 | 0.85 | 离子反应的发生条件 离子共存 限定条件下的离子共存 | |
| 5 | 0.65 | 化学实验基础操作 物质分离、提纯综合应用 | |
| 6 | 0.85 | 氨气 镁的结构与化学性质 铁与水蒸气的反应 铜与强氧化性酸的反应 | |
| 7 | 0.65 | 离子反应的发生及书写 离子方程式的书写 离子方程式的正误判断 | |
| 8 | 0.65 | 22.4L/mol适用条件 化学平衡状态的判断方法 化学平衡常数的概念及表达方式 熵判据 | |
| 9 | 0.85 | 氧化还原反应方程式的配平 氧化还原反应的规律 能量的相互转化 | |
| 10 | 0.85 | 氮气 氨气 铵盐 一氧化氮 | |
| 11 | 0.65 | 元素周期律、元素周期表的推断 同主族元素性质递变规律 微粒半径大小的比较方法 根据物质性质进行元素种类推断 | |
| 13 | 0.65 | 乙醇与钠反应的机理 糖类中醛基的性质 淀粉与碘的反应 | |
| 二、多选题 | |||
| 12 | 0.85 | 有机官能团的性质及结构 分子的手性 含有酚羟基的物质性质的推断 多官能团有机物的结构与性质 | |
| 14 | 0.4 | 酸碱中和滴定的综合考查 弱电解质的电离平衡 盐溶液中离子浓度大小的比较 | |
| 15 | 0.85 | 化学反应热的计算 碰撞理论及活化能 活化能及其对反应速率的影响 催化剂对化学反应速率的影响 | |
| 三、解答题 | |||
| 16 | 0.65 | 化学反应原理综合考查 弱电解质的电离平衡 电离平衡常数及影响因素 | 原理综合题 |
| 17 | 0.65 | 有机官能团的性质及结构 羧酸酯化反应 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |
| 18 | 0.4 | 物质结构与性质综合考查 等电子原理的应用 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 | 结构与性质 |
| 19 | 0.4 | 配制一定物质的量浓度的溶液实验的仪器 物质分离、提纯综合应用 探究物质组成或测量物质的含量 | 工业流程题 |
| 20 | 0.65 | 二氧化硫的化学性质 二氧化硫与氧气的反应 电解原理的应用 | 工业流程题 |







