20. 铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)=Fe(s)+CO
2(g) ΔH
1Fe
2O
3(s)+

CO(g)=

Fe
3O
4(s)+

CO
2(g) ΔH
2Fe
3O
4(s)+CO(g)=3FeO(s)+CO
2(g) ΔH
3Fe
2O
3(s)+3CO(g)=2Fe(s)+3CO
2(g) ΔH
4上述总反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如图:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为
_______,该温度下测得固体混合物中n(Fe):n(O)=5:1,则FeO被CO还原为Fe的百分率为
_______(设其它固体杂质中不含Fe、O元素)。
(2)铁系金属常用作CO加氢反应的催化剂。已知某种催化剂可用来催化反应CO(g)+3H
2(g)
⇌CH
4(g)+H
2O(g) ΔH<0。在T℃,压强为p时将1molCO和3molH
2加入容积为1L的密闭容器中。实验测得CO的体积分数χ(CO)如表:
| t/min | 0 | 10 | 20 | 30 | 35 |
| χ(CO) | 0.25 | 0.20 | 0.17 | 0.15 | 0.15 |
①前10min内,CO的平均反应速率υ(CO)=
_______(保留两位有效数字)。
②达到平衡时,体系的总压强p与初始压强之比p
0,p:p
0=
_______;
③如图是该反应CO的平衡转化率与温度、压强的关系。
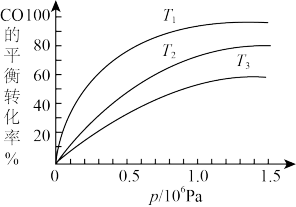
图中温度T
1、T
2、T
3由高到低的顺序是
_______,理由是
_______④45min时,保持容器的温度和体积不变,再加入1molCO和3molH
2,再次达到平衡时,CO的平衡转化率
_______(填“>”、“<”或“=”)30min时CO的平衡转化率。