18. 将CO
2转化为有经济价值的产物,可以推动经济高质量发展和生态环境质量的持续改善,实现“碳中和”。请回答:
(1)CO
2转化为甲醇有利于实现碳中和,该过程经历以下两步:
CO
2(g)+H
2(g)

CO(g)+H
2O(g) △H=+41kJ/mol
CO(g)+2H
2(g)

CH
3OH(g) △H=-90kJ/mol
①写出CO
2(g)合成CH
3OH(g)总反应的热化学方程式
_______。
②能说明反应CO(g)合成CH
3OH(g)总反应已达平衡状态的是
_______ (填字母)。
A. CO
2、H
2、CH
3OH分子数之比为1:3:1的状态
B.在恒温恒容的容器中,混合气体的平均摩尔质量保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,气体的密度不再变化
③在一定条件下,向体积为2L的恒容密闭容器中通入1molCO
2和3molH
2发生CO
2合成CH
3OH的总反应,测得10min达到平衡时氢气的平均速率为0.12mol/(L·min),则该反应的平衡常数为
_______(保留一位小数)。
该反应中v
正=k
正c(CO
2)·c
3(H
2),v
逆=k
逆c(CH
3OH)·c(H
2O),其中k
正、k
逆为速率常数,仅与温度有关,则当反应过程中CO
2的物质的量为0.5mol时,v
正:v
逆=
_______。
(2)CO
2催化加氢生成乙烯也是CO
2的热点研究领域。2CO
2(g)+6H
2(g)

C
2H
4(g)+4H
2O(g) △H<0。
①达到平衡后,欲增加乙烯的产率,并提高反应的速率,可采取的措施
_______(写出其中符合条件的一种)。
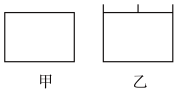
②如图所示,关闭活塞,向甲乙两个密闭容器分别充入lmolCO
2和3molH
2,发生反应CO
2催化加氢生成乙烯,起始温度体积相同(T
1℃、4L密闭容器)。达到平衡时,乙的容器容积为2.8L,则平衡时甲容器中CO
2的物质的量
_______0.2mol(填“大于、小于、等于、无法确定”)。