I.工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,反应为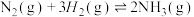
 ,
,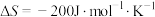 。请回答下列问题:
。请回答下列问题:
(1)常温下,合成氨反应________ (填“能”或“不能”)自发进行,其平衡常数表达式K=________ 。
(2)________ 温(填“高”或“低”)有利于提高反应速率,________ 温(填“高”或“低”)有利于提高平衡转化率,综合考虑催化剂活性等因素,工业常采用400∼500℃。
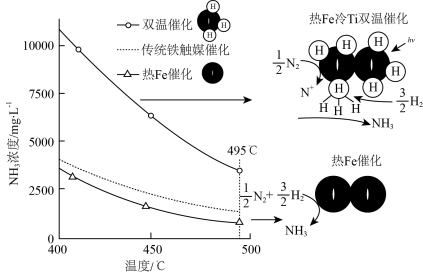
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用Fe-TiO2·xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2·xHy的温度为415℃)。(纵坐标为反应达平衡时NH3的浓度)________________ 。
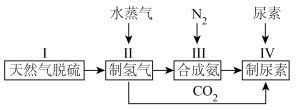
Ⅱ.合成氨工艺可以进一步优化,实现尿素的合成,简易流程图如下: ,
, ,恒容容器中,对于以上反应,能加快反应速率的是
,恒容容器中,对于以上反应,能加快反应速率的是________ 。
A.升高温度 B.充入He C.加入催化剂
(5)已知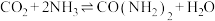 ,整个合成尿素的流程中,甲烷的利用率为80%,100吨甲烷为原料能够合成
,整个合成尿素的流程中,甲烷的利用率为80%,100吨甲烷为原料能够合成________ 吨尿素。
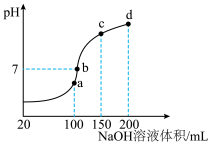
Ⅲ.NH4HSO4在分析试剂、医药、电子工业中用途广泛。室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:________ ;
(7)在b点,溶液中各离子浓度由大到小的排列顺序是________ ;
(8)在cd段发生反应的离子方程式为________ 。
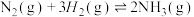
 ,
,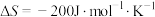 。请回答下列问题:
。请回答下列问题:(1)常温下,合成氨反应
(2)
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用Fe-TiO2·xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2·xHy的温度为415℃)。(纵坐标为反应达平衡时NH3的浓度)
Ⅱ.合成氨工艺可以进一步优化,实现尿素的合成,简易流程图如下:
 ,
, ,恒容容器中,对于以上反应,能加快反应速率的是
,恒容容器中,对于以上反应,能加快反应速率的是A.升高温度 B.充入He C.加入催化剂
(5)已知
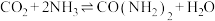 ,整个合成尿素的流程中,甲烷的利用率为80%,100吨甲烷为原料能够合成
,整个合成尿素的流程中,甲烷的利用率为80%,100吨甲烷为原料能够合成Ⅲ.NH4HSO4在分析试剂、医药、电子工业中用途广泛。室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
(7)在b点,溶液中各离子浓度由大到小的排列顺序是
(8)在cd段发生反应的离子方程式为
更新时间:2024-05-05 23:20:19
|
相似题推荐
【推荐1】从富钒废渣( 、
、 、
、 )中回收
)中回收 的工艺过程可表示为
的工艺过程可表示为
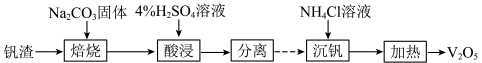
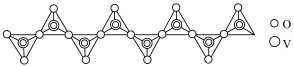
(1)“焙烧”所得钠盐的阴离子呈如图(其中钒为+5价)的无限链状结构,写出“焙烧”的化学方程式:___________ 。
(2)“沉钒”反应是向含有 的溶液中加入
的溶液中加入 溶液,析出
溶液,析出 沉淀。
沉淀。
①写出“沉钒”反应的离子方程式:___________ 。
②已知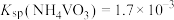 。室温下,测得“分离”后所得溶液中
。室温下,测得“分离”后所得溶液中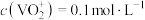 ,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中
,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中 不低于
不低于___________  。
。
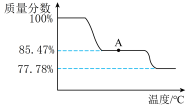
③为研究 受热发生的化学变化,某化学兴趣小组称取一定质量的
受热发生的化学变化,某化学兴趣小组称取一定质量的  在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为___________ 。
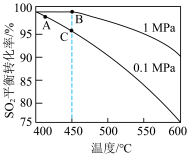
(3)一定温度下,恒压密闭容器中发生反应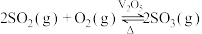 ,
, 反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是___________ 。
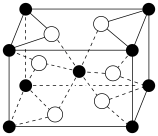
(4)还原V2O5 可以制备VO2 ,VO2的晶胞结构如图,该晶胞中矾的配位数为___________ 。
 、
、 、
、 )中回收
)中回收 的工艺过程可表示为
的工艺过程可表示为
(1)“焙烧”所得钠盐的阴离子呈如图(其中钒为+5价)的无限链状结构,写出“焙烧”的化学方程式:

(2)“沉钒”反应是向含有
 的溶液中加入
的溶液中加入 溶液,析出
溶液,析出 沉淀。
沉淀。①写出“沉钒”反应的离子方程式:
②已知
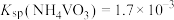 。室温下,测得“分离”后所得溶液中
。室温下,测得“分离”后所得溶液中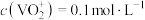 ,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中
,为使“沉钒”时钒元素的沉淀率达到99%,应使“沉钒”后的溶液中 不低于
不低于 。
。③为研究
 受热发生的化学变化,某化学兴趣小组称取一定质量的
受热发生的化学变化,某化学兴趣小组称取一定质量的  在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
在空气中加热,剩余固体质量分数(剩余固体质量/起始质量)随温度变化的曲线如图所示,则点A所得物质的化学式为
(3)一定温度下,恒压密闭容器中发生反应
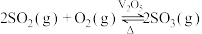 ,
, 反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
反应温度和压强的关系如图所示。实际生产选择图中C点的反应条件,不选择A、B点的理由分别是
(4)还原V2O5 可以制备VO2 ,VO2的晶胞结构如图,该晶胞中矾的配位数为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】含钒化合物广泛用于冶金、化工行业。由富钒废渣(含 、
、 和
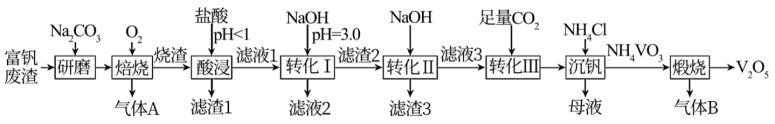
和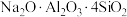 、FeO)制备
、FeO)制备 的一种流程如下:
的一种流程如下:
查阅资料:
部分含钒物质在水溶液中的主要存在形式如下:
本工艺中,生成氢氧化物沉淀的pH如下:
回答下列问题:
(1)“焙烧”中,将“研磨”所得粉末与 逆流混合的目的为
逆流混合的目的为_______ ;所生成的气体A可在_______ 工序中再利用。
(2)“酸浸”V元素发生的离子反应方程式_______ 。
(3)滤渣2含有的物质为_______ 。
(4)“转化Ⅱ”需要调整pH范围为_______ ,“转化Ⅲ”中含钒物质反应的离子方程式为_______ 。
(5)“沉钒”中加入过量 有利于晶体析出,其原因为
有利于晶体析出,其原因为_______ 。
 、
、 和
和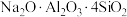 、FeO)制备
、FeO)制备 的一种流程如下:
的一种流程如下:
查阅资料:
部分含钒物质在水溶液中的主要存在形式如下:
| pH | <1 | 1~4 | 4~6 | 6~8.5 | 8.5~13 | >13 |
| 主要形式 |  |  | 多矾酸根 |  | 多矾酸根 |  |
| 备注 | 多矾酸盐在水中溶解度较小 | |||||
| 4~6 | 6~8.5 | 8.5~13 | >13 |
| 多矾酸根 |  | 多矾酸根 |  |
本工艺中,生成氢氧化物沉淀的pH如下:
| 物质 |  |  |  |
| 开始沉淀pH | 7.0 | 1.9 | 3.2 |
| 沉淀完全pH | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)“焙烧”中,将“研磨”所得粉末与
 逆流混合的目的为
逆流混合的目的为(2)“酸浸”V元素发生的离子反应方程式
(3)滤渣2含有的物质为
(4)“转化Ⅱ”需要调整pH范围为
(5)“沉钒”中加入过量
 有利于晶体析出,其原因为
有利于晶体析出,其原因为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】炼油厂烷基化反应产生的废液中含硫酸91%、难挥发有机物7%。实验室以软锰矿(主要含 ,还含少量Fe、Al等元素)处理废液并制取
,还含少量Fe、Al等元素)处理废液并制取 晶体,其实验流程如下:
晶体,其实验流程如下:
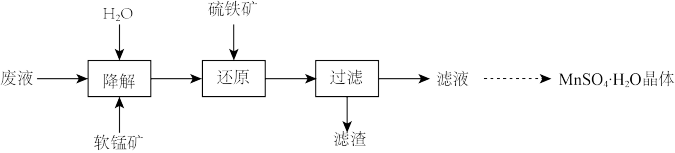
已知:① 时,
时, 和
和 沉淀完全;
沉淀完全; 时,
时, 开始沉淀;②
开始沉淀;② 分解温度为
分解温度为 。
。
(1)研究温度对“降解”过程中有机物去除率的影响,实验在如图1所示的装置中进行。
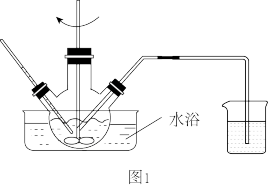
①在不同温度下反应相同时间,发现温度从 升高到
升高到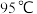 时,有机物去除率从29%增大到58%,其可能的原因是
时,有机物去除率从29%增大到58%,其可能的原因是 的氧化能力随温度升高而增强;
的氧化能力随温度升高而增强;_______ 。
②废液因含有机物而呈现黑红色。有机物降解速率慢,难以观察气泡产生速率。降解一段时间,判断有机物浓度基本不变的依据是:三颈烧瓶内_______ 。烧杯中盛放的试剂可以是_______ 。
(2)降解一段时间后,加入硫铁矿(主要成分 )将剩余
)将剩余 还原,所得溶液中的主要离子有
还原,所得溶液中的主要离子有 等,其离子方程式为
等,其离子方程式为_______ 。
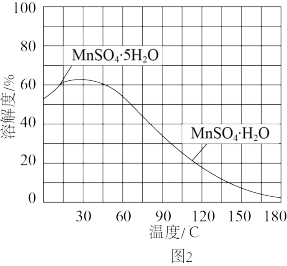
(3) 的溶解度曲线如图2所示。设计以过滤所得滤液为原料,进一步除去有机物等杂质并制取
的溶解度曲线如图2所示。设计以过滤所得滤液为原料,进一步除去有机物等杂质并制取 晶体的实验方案:
晶体的实验方案:_______ ,趁热过滤,用热的硫酸锰溶液洗涤, 烘干。(实验中须使用的试剂:石灰石粉末、活性炭)。
烘干。(实验中须使用的试剂:石灰石粉末、活性炭)。
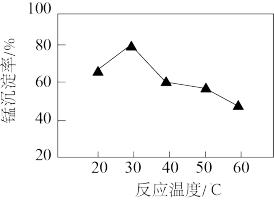
(4)若将流程中“过滤”后的滤液调节 除去
除去 后,再加入
后,再加入 溶液,可生成
溶液,可生成 沉淀,反应温度对锰沉淀率的影响关系如图所示。
沉淀,反应温度对锰沉淀率的影响关系如图所示。
①该过程中沉淀剂选用 溶液,而不用
溶液,而不用 溶液的原因是
溶液的原因是_______ 。
②当温度超过 ,沉锰反应的锰沉淀率随温度升高而下降的原因是
,沉锰反应的锰沉淀率随温度升高而下降的原因是_______ 。
 ,还含少量Fe、Al等元素)处理废液并制取
,还含少量Fe、Al等元素)处理废液并制取 晶体,其实验流程如下:
晶体,其实验流程如下:
已知:①
 时,
时, 和
和 沉淀完全;
沉淀完全; 时,
时, 开始沉淀;②
开始沉淀;② 分解温度为
分解温度为 。
。(1)研究温度对“降解”过程中有机物去除率的影响,实验在如图1所示的装置中进行。

①在不同温度下反应相同时间,发现温度从
 升高到
升高到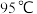 时,有机物去除率从29%增大到58%,其可能的原因是
时,有机物去除率从29%增大到58%,其可能的原因是 的氧化能力随温度升高而增强;
的氧化能力随温度升高而增强;②废液因含有机物而呈现黑红色。有机物降解速率慢,难以观察气泡产生速率。降解一段时间,判断有机物浓度基本不变的依据是:三颈烧瓶内
(2)降解一段时间后,加入硫铁矿(主要成分
 )将剩余
)将剩余 还原,所得溶液中的主要离子有
还原,所得溶液中的主要离子有 等,其离子方程式为
等,其离子方程式为(3)
 的溶解度曲线如图2所示。设计以过滤所得滤液为原料,进一步除去有机物等杂质并制取
的溶解度曲线如图2所示。设计以过滤所得滤液为原料,进一步除去有机物等杂质并制取 晶体的实验方案:
晶体的实验方案: 烘干。(实验中须使用的试剂:石灰石粉末、活性炭)。
烘干。(实验中须使用的试剂:石灰石粉末、活性炭)。
(4)若将流程中“过滤”后的滤液调节
 除去
除去 后,再加入
后,再加入 溶液,可生成
溶液,可生成 沉淀,反应温度对锰沉淀率的影响关系如图所示。
沉淀,反应温度对锰沉淀率的影响关系如图所示。
①该过程中沉淀剂选用
 溶液,而不用
溶液,而不用 溶液的原因是
溶液的原因是②当温度超过
 ,沉锰反应的锰沉淀率随温度升高而下降的原因是
,沉锰反应的锰沉淀率随温度升高而下降的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】乙烯是合成多种塑料的单体,我国科学家开发的特殊催化剂还原 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。
反应原理:
主反应:

副反应: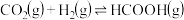

(1)已知: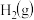 、
、 的燃烧热(
的燃烧热( )分别是
)分别是 、
、 。
。

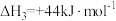 。
。


______  。
。
(2)在一定温度下,向恒容密闭容器中充入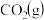 和
和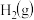 ,若只发生主反应,下列情况不能说明主反应达到平衡的是
,若只发生主反应,下列情况不能说明主反应达到平衡的是______ (填标号)。
A.混合气体密度保持不变B.混合气体总压强保持不变
C.乙烯体积分数保持不变D.气体平均摩尔质量保持不变
达到平衡后能提高 平衡转化率的措施是
平衡转化率的措施是______ (任填一条)。
(3)在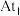 、
、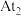 、
、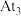 三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率(
三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率( )与温度关系如图1所示。
)与温度关系如图1所示。
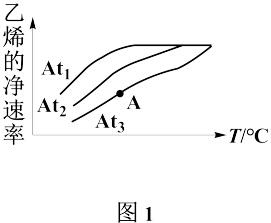
催化效率最高的是______ (填“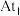 ”、“
”、“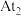 ”或“
”或“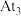 ”),A点的正反应速率
”),A点的正反应速率______ (填“大于”、“小于”或“等于”)逆反应速率。
(4)一定温度下,在容积为2L的恒容密闭容器中充入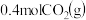 和
和 ,同时发生了主反应和副反应,达到平衡时
,同时发生了主反应和副反应,达到平衡时 的转化率为45%,
的转化率为45%,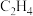 的选择性为80%,则该温度下,副反应的平衡常数
的选择性为80%,则该温度下,副反应的平衡常数
______ (结果保留2位小数)。
提示: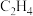 的选择性
的选择性
(5)常盖下,HCOOH的电离常数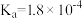 ,将
,将 的NaOH溶液和
的NaOH溶液和 的HCOOH溶液等体积混合,得到混合溶液的pH
的HCOOH溶液等体积混合,得到混合溶液的pH______ (填“>”“<”或“=”)7。
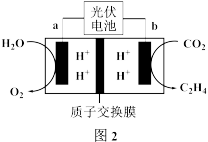
(6)以光伏电池为能源,采用电催化还原 制备乙烯,装置如图2所示,该装置阴极上的电极反应式为
制备乙烯,装置如图2所示,该装置阴极上的电极反应式为______ 。
 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。反应原理:
主反应:


副反应:
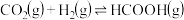

(1)已知:
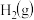 、
、 的燃烧热(
的燃烧热( )分别是
)分别是 、
、 。
。
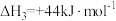 。
。

 。
。(2)在一定温度下,向恒容密闭容器中充入
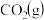 和
和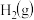 ,若只发生主反应,下列情况不能说明主反应达到平衡的是
,若只发生主反应,下列情况不能说明主反应达到平衡的是A.混合气体密度保持不变B.混合气体总压强保持不变
C.乙烯体积分数保持不变D.气体平均摩尔质量保持不变
达到平衡后能提高
 平衡转化率的措施是
平衡转化率的措施是(3)在
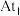 、
、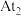 、
、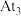 三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率(
三种不同催化剂作用下(其他条件相同)只发生主反应,测得乙烯的净速率( )与温度关系如图1所示。
)与温度关系如图1所示。
催化效率最高的是
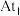 ”、“
”、“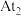 ”或“
”或“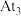 ”),A点的正反应速率
”),A点的正反应速率(4)一定温度下,在容积为2L的恒容密闭容器中充入
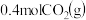 和
和 ,同时发生了主反应和副反应,达到平衡时
,同时发生了主反应和副反应,达到平衡时 的转化率为45%,
的转化率为45%,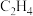 的选择性为80%,则该温度下,副反应的平衡常数
的选择性为80%,则该温度下,副反应的平衡常数
提示:
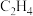 的选择性
的选择性
(5)常盖下,HCOOH的电离常数
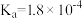 ,将
,将 的NaOH溶液和
的NaOH溶液和 的HCOOH溶液等体积混合,得到混合溶液的pH
的HCOOH溶液等体积混合,得到混合溶液的pH(6)以光伏电池为能源,采用电催化还原
 制备乙烯,装置如图2所示,该装置阴极上的电极反应式为
制备乙烯,装置如图2所示,该装置阴极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】处理再利用H2S有多种方法。
(1)碱法脱硫
用K2CO3溶液吸收H2S。
已知:氢硫酸和碳酸的电离常数如表。
①用化学用语表示K2CO3溶液显碱性的原因:____ 。
②用过量的K2CO3溶液吸收H2S的离子方程式是____ 。
(2)热分解法脱硫
在密闭容器中发生反应2H2S(g) S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。
S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。
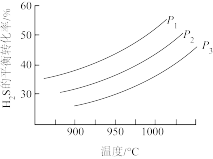
①P3>P2>P1,反应中S2____ (填‘“是”或“不是”)气态,理由是____ 。
②实际反应在高温下进行的原因是____ 。
(3)间接电解法脱硫
间接电解法脱硫过程的示意图如图。
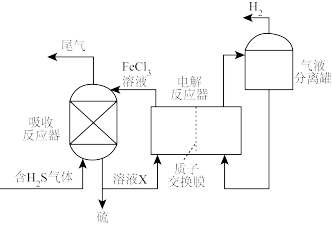
①溶液X的主要溶质是____ 。
②简述在电解反应器中FeCl3溶液再生的原理:____ 。
③不考虑其他副反应,理论上5molH2S反应能生成____ gH2。
(1)碱法脱硫
用K2CO3溶液吸收H2S。
已知:氢硫酸和碳酸的电离常数如表。
| Ka1 | Ka2 | |
| H2S | 1.1×10-7 | 1.3×10-13 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
②用过量的K2CO3溶液吸收H2S的离子方程式是
(2)热分解法脱硫
在密闭容器中发生反应2H2S(g)
 S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。
S2(?)+2H2(g)。其他条件不变时,H2S的平衡转化率随温度和压强的变化如图。
①P3>P2>P1,反应中S2
②实际反应在高温下进行的原因是
(3)间接电解法脱硫
间接电解法脱硫过程的示意图如图。

①溶液X的主要溶质是
②简述在电解反应器中FeCl3溶液再生的原理:
③不考虑其他副反应,理论上5molH2S反应能生成
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】2022年北京冬奥会主火炬首次采用以氢气为燃料的微火形式,体现了绿色奥运理念。工业上,利用天然气制备氢气,还可得到乙烯、乙炔等化工产品,有关反应原理如下:
反应l:2CH4(g) C2H2(g)+3H2(g) △H1
C2H2(g)+3H2(g) △H1
反应2:2CH4(g) C2H4(g)+2H2(g) △H2
C2H4(g)+2H2(g) △H2
请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
能表示C2H2(g)燃烧热的热化学方程式为_______ 。
(2)向恒温恒容密闭容器中充入适量CH4,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
(3)实验测得2CH4(g) C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1
C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1_______ (填“>”、“<”或“=”)T2。
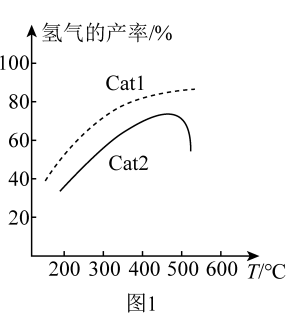
(4)在密闭容器中充入CH4,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图1。在其他条件相同时,催化效率较高的是_______ (填“Cat1”或“Cat2”)。在Cat2作用下,温度高于500°C时,H2的产率降低的可能原因是_______ 。
(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由CH4和N2组成的混合气体(N2不参与反应),同时发生反应1和反应2,测得CH4的平衡转化率与通入气体中CH4的物质的量分数的关系如图2。
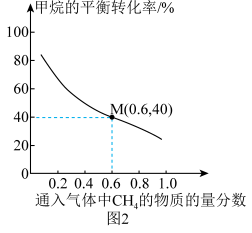
①图2中,随着通入气体中CH4的物质的量分数增大,甲烷的平衡转化率降低的主要原因是_______ 。
②已知M点对应的乙炔的选择性为75%[乙炔的选择性=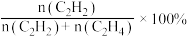 ]。该温度下,生成的H2的分压为
]。该温度下,生成的H2的分压为_______ kPa。
反应l:2CH4(g)
 C2H2(g)+3H2(g) △H1
C2H2(g)+3H2(g) △H1反应2:2CH4(g)
 C2H4(g)+2H2(g) △H2
C2H4(g)+2H2(g) △H2请回答下列问题:
(1)已知几种物质的燃烧热数据如下:
| 物质 | CH4(g) | C2H2(g) | C2H4(g) | H2(g) |
| 燃烧热(ΔH/kJ·mol-1) | -890.3 | -1299.5 | -1411.0 | -285.8 |
(2)向恒温恒容密闭容器中充入适量CH4,发生上述反应1和反应2。下列情况不能说明上述反应达到平衡状态的是_______(填标号)。
| A.气体总压强不随时间变化 | B.气体密度不随时间变化 |
| C.气体平均摩尔质量不随时间变化 | D.H2体积分数不随时间变化 |
 C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1
C2H2(g)+3H2(g)的速率方程:v正=k正c2(CH4),v逆=k逆·c(C2H2)·c3(H2)(k正、k逆分别为正、逆反应速率常数,只与温度、催化剂有关)。T1℃下反应达到平衡时k正=1.5k逆,T2℃下反应达到平衡时k正=3k逆。由此推知,T1(4)在密闭容器中充入CH4,发生上述反应1和反应2。在不同催化剂Cat1、Cat2作用下,测得单位时间内H2的产率与温度的关系如图1。在其他条件相同时,催化效率较高的是

(5)一定温度下,总压强恒定为121kPa时,向密闭容器中充入由CH4和N2组成的混合气体(N2不参与反应),同时发生反应1和反应2,测得CH4的平衡转化率与通入气体中CH4的物质的量分数的关系如图2。

①图2中,随着通入气体中CH4的物质的量分数增大,甲烷的平衡转化率降低的主要原因是
②已知M点对应的乙炔的选择性为75%[乙炔的选择性=
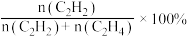 ]。该温度下,生成的H2的分压为
]。该温度下,生成的H2的分压为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】2023 年杭州亚运会主火炬创新使用了绿色“零碳甲醇”作为燃料,这不仅在亚运史上是第一次,在全球大型体育赛事上也是首次实现了废碳的再生利用。“零碳甲醇”是符合“碳中和”属性的绿色能源。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g) CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 ___________ K(用含a、b的代数式表示)。
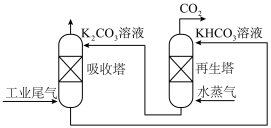
(2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示: 后,
后, 则该溶液的pOH=
则该溶液的pOH=___________ (该温度下H2CO3的Ka1=4.6×10-7,Ka2=5.0×10-11 Kw=1×10-a,用含a的代数式表示)。
(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g) CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
Ⅲ.CO(g)+2H2(g) 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1
①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是___________ (填字母)。___________ 。
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =___________ bar,反应I的平衡常数Kp= ___________ bar-2(Kp为用分压表示的平衡常数,分压=总压×物质的量分数,用含a的代数式表示)。
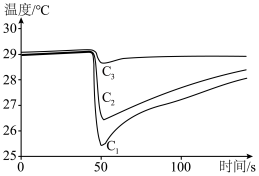
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是___________ ,理由是___________ 。
请回答下列问题:
(1)工业上主要利用以下反应合成甲醇: CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。已知在一定条件下该反应的
CH3OH(g)+H2O(g)。已知在一定条件下该反应的 = -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围
= -akJ⋅mol-1,ΔS=-bJ⋅mol-1⋅K-1(a>0,b >0),假设该反应的焓变和熵变不随温度的改变而改变,请计算该反应能够发生的适宜温度T的取值范围 (2)目前有多种用于工业捕集CO2的方法,主要分为吸收(物理吸收、化学吸收、生物吸收)、吸附、深冷分离和膜分离等,也有将不同捕集方法相结合的方法。一种模拟脱除工业尾气中CO2的示意图如图所示:
 后,
后, 则该溶液的pOH=
则该溶液的pOH=(3)CO2合成甲醇的工艺主要分为两类,一类称为直接法:CO2直接加H2合成甲醇;一类称为间接法:CO2和H2通过逆水煤气反应,先合成CO后,CO和H2再合成甲醇。
I.CO2 (g)+3H2 (g)
 CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1
CH3OH(g)+H2O(g) ΔH1=-48.9kJ⋅mol-1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1
CO(g)+H2O(g) ΔH2= +41.1 kJ·mol-1Ⅲ.CO(g)+2H2(g)
 3CH3OH(g) ΔH3=-90kJ⋅mol-1
3CH3OH(g) ΔH3=-90kJ⋅mol-1①若利用间接工艺法合成甲醇,反应的决速步为逆水煤气反应,下列示意图中能体现上述反应体系能量变化的是
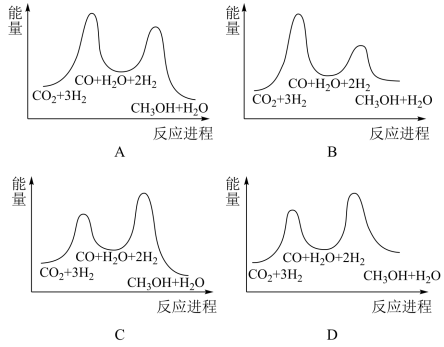
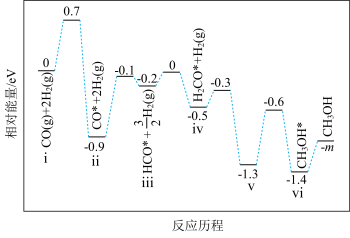
③工业生产中测定体系的压强具有实际意义。一定温度下,仅利用反应Ⅰ直接合成甲醇,将体积分数为a% CO2、3a% H2 的进料气(含杂质气体),以 Cu/Zn/Al/Zr纳米纤维为催化剂,控制压强为50 bar(1 bar=100 kPa)发生反应I,进料气中杂质气体不反应,达到平衡时二氧化碳的转化率为90%,达到平衡时, p(H2) =
(4)甲醇便于运输,是一种具有前景的液体燃料,利用手持技术,通过测定甲醇、乙醇、正丙醇等三种物质在温度传感器尖头处蒸发时的温度变化曲线,根据曲线下降的幅度和速率的快慢,可以比较它们之间的分子间作用力的大小。请判断表示甲醇的曲线是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】氨的合成原理为:N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图。回答下列问题:
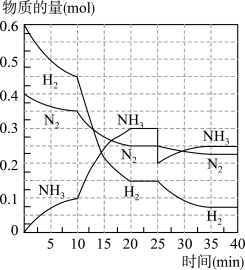
(1)10min内以NH3表示的平均反应速率为_________
(2)在10~20min内,NH3浓度变化的原因可能是_____________
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡:平衡常数K1=__________ (带数据的表达式),第2次平衡时NH3的体积分数为_____________ 。
(4)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fc2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)⇌2NH3+1.5O2(g)∆H=akJ·mol-1,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
①此合成反应的a______ 0,△S_______ 0;(填“>”、“<”或一”)
②已知N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1,2 H2(g)+ O2(g)=2H2O(l) ∆H=-571.kJ·mol-1 则常温下氮气与水反应生成氨气与氧气的热化学方程式为_____________________________

(1)10min内以NH3表示的平均反应速率为
(2)在10~20min内,NH3浓度变化的原因可能是
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡:平衡常数K1=
(4)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fc2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)⇌2NH3+1.5O2(g)∆H=akJ·mol-1,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a
②已知N2(g)+3H2(g)⇌2NH3(g)∆H=-92.4kJ·mol-1,2 H2(g)+ O2(g)=2H2O(l) ∆H=-571.kJ·mol-1 则常温下氮气与水反应生成氨气与氧气的热化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
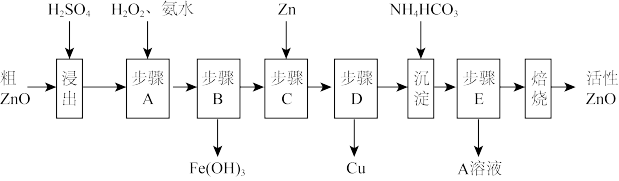
已知:几种离子生成氢氧化物沉淀时的pH如表:
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是______ ,该步骤需控制溶液pH的范围是______ 。
(2)A溶液中主要含有的溶质是______ 。
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS______ (选填“=”、“>”或“<”)0。
(4)若经处理后的废水pH=8,此时Zn2+的浓度为______ mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。

已知:几种离子生成氢氧化物沉淀时的pH如表:
| 待沉淀离子 | Fe2+ | Fe3+ | Zn2+ | Cu2+ |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
请回答下列问题:
(1)步骤A加H2O2发生反应的离子方程式是
(2)A溶液中主要含有的溶质是
(3)碱式碳酸锌经焙烧制得活性ZnO的反应ΔH>0,该反应能自发进行的原因是ΔS
(4)若经处理后的废水pH=8,此时Zn2+的浓度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,一种生产NaClO2的工艺如下:
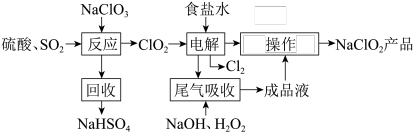
已知:①ClO2是一种强氧化性气体,浓度大时易分解爆炸。在生产使用时要用稀有气体或空气等进行稀释,同时避免光照、震动等。②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·33H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。回答下列问题:
(1)最近科学家又在“反应”步骤的基础上研究出用H2C2O4代替SO2制备ClO2的新方法,该方法的化学方程式为______________________ 。
(2)获得产品NaClO2的“操作”包括以下步骤:
①减压,55℃蒸发结晶;②趁热过滤;③___________________________ ④低于60℃干燥,得到产品。
(3)为了测定产品NaClO2的纯度,取上述所得产品12.5g溶于水配成1L溶液,取出10.00mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(ClO2-被还原为Cl-杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol•L﹣1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度_________________________ (提示:2Na2S2O3+I2=Na2S4O6+2NaI)
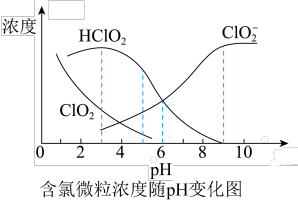
(4)NaClO2溶液中存在ClO2、HClO2、ClO2-、Cl-四种含氯微粒。经测定 25℃各含氯微粒浓度随 pH 的变化情况如图所示(Cl-没有画出)
①酸性条件下NaClO2溶液中存在Cl-的原因是_______________________ (用离子方程式解释)。
②pH=5时,NaClO2溶液中ClO2、HClO2、ClO2-、Cl-四种含氯微粒的浓度由大到小的顺序是___________________________________________________ 。

已知:①ClO2是一种强氧化性气体,浓度大时易分解爆炸。在生产使用时要用稀有气体或空气等进行稀释,同时避免光照、震动等。②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·33H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。回答下列问题:
(1)最近科学家又在“反应”步骤的基础上研究出用H2C2O4代替SO2制备ClO2的新方法,该方法的化学方程式为
(2)获得产品NaClO2的“操作”包括以下步骤:
①减压,55℃蒸发结晶;②趁热过滤;③
(3)为了测定产品NaClO2的纯度,取上述所得产品12.5g溶于水配成1L溶液,取出10.00mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后(ClO2-被还原为Cl-杂质不参加反应),加入2~3滴淀粉溶液,用0.25mol•L﹣1Na2S2O3标准液滴定,达到滴定终点时用去标准液20.00mL,试计算产品NaClO2的纯度

(4)NaClO2溶液中存在ClO2、HClO2、ClO2-、Cl-四种含氯微粒。经测定 25℃各含氯微粒浓度随 pH 的变化情况如图所示(Cl-没有画出)
①酸性条件下NaClO2溶液中存在Cl-的原因是
②pH=5时,NaClO2溶液中ClO2、HClO2、ClO2-、Cl-四种含氯微粒的浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】燃料燃烧产生的二氧化碳有多种捕捉方式,在自然界中存在着二氧化碳气体与其他物质的反应过程,而实验室中一般使用碱溶液来吸收二氧化碳气体。
(1)向1L 1 的NaOH溶液中通入0.5mol二氧化碳气体,最终所得溶液中各离子浓度关系正确的选项有(假设溶液体积不发生变化):___________。
的NaOH溶液中通入0.5mol二氧化碳气体,最终所得溶液中各离子浓度关系正确的选项有(假设溶液体积不发生变化):___________。
(2)已知:25℃时,① 的电离平衡常数
的电离平衡常数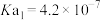 ,
,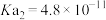 。
。
②盐类水解常数 可以表示盐溶液水解平衡的限度,书写方式与电离平衡常数一致。
可以表示盐溶液水解平衡的限度,书写方式与电离平衡常数一致。
写出 溶液中
溶液中 水解的平衡常数的表达式,并根据上述数据计算出
水解的平衡常数的表达式,并根据上述数据计算出 的数值:
的数值:
___________ (表达式)=___________ (数值)。
(3)根据 的
的 数值和
数值和 电离平衡常数的数值,判断至下
电离平衡常数的数值,判断至下 溶液的酸碱性,并结合适当的化学语言说明理由:
溶液的酸碱性,并结合适当的化学语言说明理由:___________ 。
(1)向1L 1
 的NaOH溶液中通入0.5mol二氧化碳气体,最终所得溶液中各离子浓度关系正确的选项有(假设溶液体积不发生变化):___________。
的NaOH溶液中通入0.5mol二氧化碳气体,最终所得溶液中各离子浓度关系正确的选项有(假设溶液体积不发生变化):___________。A.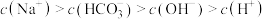 |
B.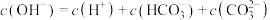 |
C.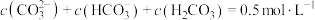 |
D. |
 的电离平衡常数
的电离平衡常数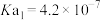 ,
,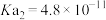 。
。②盐类水解常数
 可以表示盐溶液水解平衡的限度,书写方式与电离平衡常数一致。
可以表示盐溶液水解平衡的限度,书写方式与电离平衡常数一致。写出
 溶液中
溶液中 水解的平衡常数的表达式,并根据上述数据计算出
水解的平衡常数的表达式,并根据上述数据计算出 的数值:
的数值:
(3)根据
 的
的 数值和
数值和 电离平衡常数的数值,判断至下
电离平衡常数的数值,判断至下 溶液的酸碱性,并结合适当的化学语言说明理由:
溶液的酸碱性,并结合适当的化学语言说明理由:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】可逆反应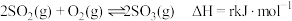 (其中
(其中 )是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
(1) 在高温下分解产生的
在高温下分解产生的 可作为硫酸工业中的催化剂,其倠化原理如下:
可作为硫酸工业中的催化剂,其倠化原理如下:
i: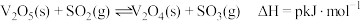
ii: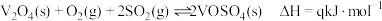
iii:
_______ (用含r,p,q的字母表达式表示)。
(2)①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是___________ (填标号)。
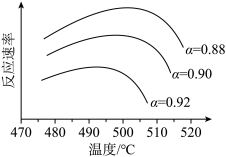
a.温度越高,反应速率越大
b. 的曲线代表平衡转化率
的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
②为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是___________ (填标号)。
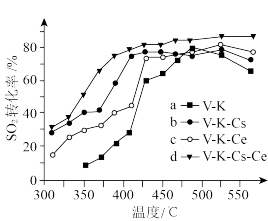
③设 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为 ,用含p和
,用含p和 的代数式表示上述催化氧化反应的
的代数式表示上述催化氧化反应的
___________ (用平衡分压代替平衡浓度计算)。
(3)硫酸工业尾气中的 可利用钠碱循环法(用
可利用钠碱循环法(用 溶液作为吸收液来吸收
溶液作为吸收液来吸收 )进行处理。若将尾气通入
)进行处理。若将尾气通入 的
的 溶液中:
溶液中:
①当溶液的pH约为6时, 溶液的吸收能力明显下降,此时溶液中
溶液的吸收能力明显下降,此时溶液中 的浓度是
的浓度是 ,则此时溶液中离子浓度由大到小的顺序为
,则此时溶液中离子浓度由大到小的顺序为___________ 。
②当溶液的pH降至约为6时,需送至电解槽再生,再生示意图如下:
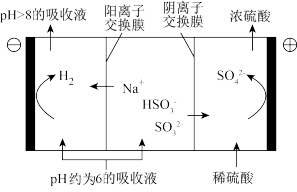
 在阳极放电的电极反应式是
在阳极放电的电极反应式是___________ ,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用,简述再生原理:___________ 。
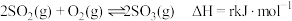 (其中
(其中 )是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。
)是硫酸工业中非常重要的一个反应,因该反应中使用催化剂而被命名为接触法制硫酸。(1)
 在高温下分解产生的
在高温下分解产生的 可作为硫酸工业中的催化剂,其倠化原理如下:
可作为硫酸工业中的催化剂,其倠化原理如下:i:
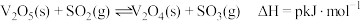
ii:
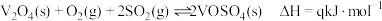
iii:

(2)①为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是

a.温度越高,反应速率越大
b.
 的曲线代表平衡转化率
的曲线代表平衡转化率c.α越大,反应速率最大值对应温度越低
d.可根据不同α下的最大速率,选择最佳生产温度
②为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是

③设
 的平衡分压为p,
的平衡分压为p, 的平衡转化率为
的平衡转化率为 ,用含p和
,用含p和 的代数式表示上述催化氧化反应的
的代数式表示上述催化氧化反应的
(3)硫酸工业尾气中的
 可利用钠碱循环法(用
可利用钠碱循环法(用 溶液作为吸收液来吸收
溶液作为吸收液来吸收 )进行处理。若将尾气通入
)进行处理。若将尾气通入 的
的 溶液中:
溶液中:①当溶液的pH约为6时,
 溶液的吸收能力明显下降,此时溶液中
溶液的吸收能力明显下降,此时溶液中 的浓度是
的浓度是 ,则此时溶液中离子浓度由大到小的顺序为
,则此时溶液中离子浓度由大到小的顺序为②当溶液的pH降至约为6时,需送至电解槽再生,再生示意图如下:

 在阳极放电的电极反应式是
在阳极放电的电极反应式是
您最近一年使用:0次



