名校
解题方法
1 . 金属锌和铝的单质及其化合物的化学性质相似。某混合物由A12O3、ZnO、Fe2O3组成,将其分离的工艺流程如下:

回答下列问题:
(1)小苏打的化学式为_______ ,"沉降池”中反应的离子方程式为CO2+OH-= 、
、_____ 、_____ 。
(2)“操作a”为___________ 。
(3)金属m可与“滤渣1”组成铝热试剂,则铝热反应的化学方程式为___________ 。
(4)测定“小苏打溶液”的物质的量浓度。
①稀盐酸配制:取6mol/L的盐酸配制80mL1.5mol/L的稀盐酸,需要用到的最合适的定量仪器及其规格为___________ 。
②物质的量浓度测定:量取25.0mL小苏打溶液置于试管中,逐滴滴加1.5mol/L的稀盐酸,边滴边振荡,直至无气泡产生,消耗稀盐酸10.0mL。“小苏打溶液"的物质的量浓度为___________ 。
③误差分析:用量筒量取6mol/L的盐酸时仰视观察,则测得的“小苏打溶液”的物质的量浓度___________ (填“偏高"“偏低”或“无影响”)。

回答下列问题:
(1)小苏打的化学式为
 、
、(2)“操作a”为
(3)金属m可与“滤渣1”组成铝热试剂,则铝热反应的化学方程式为
(4)测定“小苏打溶液”的物质的量浓度。
①稀盐酸配制:取6mol/L的盐酸配制80mL1.5mol/L的稀盐酸,需要用到的最合适的定量仪器及其规格为
②物质的量浓度测定:量取25.0mL小苏打溶液置于试管中,逐滴滴加1.5mol/L的稀盐酸,边滴边振荡,直至无气泡产生,消耗稀盐酸10.0mL。“小苏打溶液"的物质的量浓度为
③误差分析:用量筒量取6mol/L的盐酸时仰视观察,则测得的“小苏打溶液”的物质的量浓度
您最近一年使用:0次
名校
2 . 某学习小组设计了如下实验,探究浓度和温度对反应的影响。
实验探究Ⅰ:
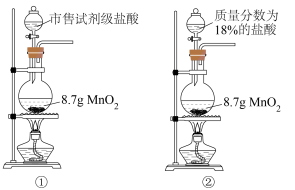
已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:___________ ;①中发生反应的离子方程式为___________ ;8.7gMnO2与33.1mL市售试剂级盐酸在加热条件下反应,生成氯气的物质的量是否为0.1mol?______ (填“是"或“否),并简述其原因:___________ 。
实验探究Ⅱ:
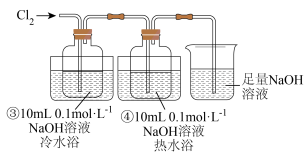
(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:___________ 。
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:___________ 。
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为___________ (用离子方程式解释)。
实验探究Ⅰ:

已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:
实验探究Ⅱ:

(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为
您最近一年使用:0次
名校
解题方法
3 . 聚合硫酸铁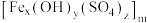 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
①称取一定质量的聚合硫酸铁,配成 溶液。
溶液。
②准确量取①中溶液 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。
③准确量取①中溶液 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。
该聚合硫酸铁组成中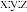 为
为
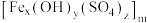 (铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:
(铁元素化合价为+3)是一种高效的混凝剂,常用于净水,它的组成可以通过以下实验测定:①称取一定质量的聚合硫酸铁,配成
 溶液。
溶液。②准确量取①中溶液
 于烧杯中,加入足量的盐酸酸化的
于烧杯中,加入足量的盐酸酸化的 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体 。
。③准确量取①中溶液
 于烧杯中,加入足量的
于烧杯中,加入足量的 溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体
溶液至沉淀完全,过滤、洗涤、干燥、灼烧,得到红棕色固体 。
。该聚合硫酸铁组成中
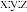 为
为A. | B. | C.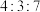 | D. |
您最近一年使用:0次
2023-12-30更新
|
178次组卷
|
3卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
4 . 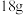 葡萄糖
葡萄糖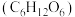 在足量的氧气中充分燃烧,将生成物全部通入到足量的过氧化钠中充分吸收,固体质量增加
在足量的氧气中充分燃烧,将生成物全部通入到足量的过氧化钠中充分吸收,固体质量增加 ,下列说法错误的是
,下列说法错误的是
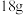 葡萄糖
葡萄糖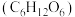 在足量的氧气中充分燃烧,将生成物全部通入到足量的过氧化钠中充分吸收,固体质量增加
在足量的氧气中充分燃烧,将生成物全部通入到足量的过氧化钠中充分吸收,固体质量增加 ,下列说法错误的是
,下列说法错误的是A. |
| B.反应后的固体是混合物 |
C.生成的 的质量为 的质量为 |
| D.上述生成物与过氧化钠反应的产物之一能使带火星的木条复燃 |
您最近一年使用:0次
2023-12-26更新
|
306次组卷
|
2卷引用:江西省鹰潭市2023-2024学年高一上学期11月期中化学试题
名校
解题方法
5 . 现有一份 和
和 固体混合物,某化学兴趣小组设计如图所示实验装置(夹持仪器省略),测定固体混合物中
固体混合物,某化学兴趣小组设计如图所示实验装置(夹持仪器省略),测定固体混合物中 的质量分数。实验步骤如下:
的质量分数。实验步骤如下:
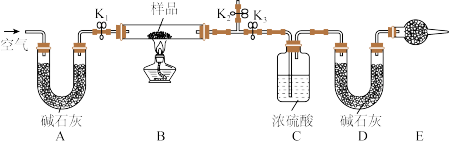
①组装好实验装置,并___________;
②加药品,称取mg样品放入硬质玻璃管中;称量装有碱石灰的U形管D的质量为 ;
;
③打开活塞 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟;
,缓缓鼓入空气数分钟;
④关闭活塞 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体;
,点燃酒精灯加热至不再产生气体;
⑤打开活塞 ,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为
,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为 。
。
请回答下列问题:
(1)补充实验步骤①的操作为___________ 。
(2)装置E中实验仪器的名称为___________ 。
(3)装置B中发生反应的化学方程式为___________ 。
(4)实验步骤③和⑤中“缓缓鼓入空气数分钟”的目的分别是___________ 。
(5)若缺少实验步骤③会导致测定结果___________ (填“偏大”“偏小”或“无影响”)。
(6)样品中 的质量分数为
的质量分数为___________ ×100%(用含m、 、
、 的式子表示)。
的式子表示)。
(7)除了该方法外,还可以用沉淀法测定 的质量分数。在选择沉淀剂时,甲同学选了过量的
的质量分数。在选择沉淀剂时,甲同学选了过量的 ,乙同学选了过量的
,乙同学选了过量的 ,从误差较小的角度选择,你认为
,从误差较小的角度选择,你认为___________ 同学更好,理由是___________ 。
 和
和 固体混合物,某化学兴趣小组设计如图所示实验装置(夹持仪器省略),测定固体混合物中
固体混合物,某化学兴趣小组设计如图所示实验装置(夹持仪器省略),测定固体混合物中 的质量分数。实验步骤如下:
的质量分数。实验步骤如下:
①组装好实验装置,并___________;
②加药品,称取mg样品放入硬质玻璃管中;称量装有碱石灰的U形管D的质量为
 ;
;③打开活塞
 、
、 ,关闭
,关闭 ,缓缓鼓入空气数分钟;
,缓缓鼓入空气数分钟;④关闭活塞
 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体;
,点燃酒精灯加热至不再产生气体;⑤打开活塞
 ,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为
,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为 。
。请回答下列问题:
(1)补充实验步骤①的操作为
(2)装置E中实验仪器的名称为
(3)装置B中发生反应的化学方程式为
(4)实验步骤③和⑤中“缓缓鼓入空气数分钟”的目的分别是
(5)若缺少实验步骤③会导致测定结果
(6)样品中
 的质量分数为
的质量分数为 、
、 的式子表示)。
的式子表示)。(7)除了该方法外,还可以用沉淀法测定
 的质量分数。在选择沉淀剂时,甲同学选了过量的
的质量分数。在选择沉淀剂时,甲同学选了过量的 ,乙同学选了过量的
,乙同学选了过量的 ,从误差较小的角度选择,你认为
,从误差较小的角度选择,你认为
您最近一年使用:0次
2023-11-21更新
|
149次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高一上学期11月期中化学试题
名校
6 . 某营养液中含有KAl(SO4)2、K2SO4、KCl三种溶质,实验测得部分离子的浓度如图甲表示。取200mL样品加水稀释,测得 Al3+的浓度(c)随溶液体积(V)的变化如图乙曲线表示。下列判断错误的是


A.图甲中X离子是SO |
| B.图乙中c1=8.0 |
| C.营养液中 KCl与K2SO4的物质的量之比为2: 1 |
| D.营养液中K2SO4的浓度是2mol/L |
您最近一年使用:0次
2023-11-08更新
|
628次组卷
|
6卷引用:江西省宜春市丰城中学2023-2024学年高一上学期1月期末化学试题
江西省宜春市丰城中学2023-2024学年高一上学期1月期末化学试题 四川省成都市树德中学2023-2024学年高一上学期11月期中考试化学试题(已下线)【精品卷】2.3.3 物质的量浓度课堂例题-人教版2023-2024学年必修第一册四川省绵阳市东辰学校2023-2024学年高一上学期期末模拟化学试卷黑龙江省实验中学2023-2024学年高一上学期第二次阶段测试化学试题四川省广安市华蓥中学2023-2024学年高一上学期12月月考化学试题
名校
7 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
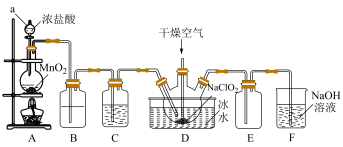
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近一年使用:0次
2023-11-06更新
|
632次组卷
|
2卷引用:江西省广信中学2023-2024学年高一上学期11月月考化学试题
名校
8 . 化学贯穿古今,下列对古诗词所涉及化学知识的解读不正确的是
| A.“错把陈醋当成墨,写尽半生纸上酸”,陈醋是混合物 |
| B.“松叶堪为酒,春来酿几多”,清香的美酒在酿制过程中发生的变化涉及电子转移 |
| C.“我昔庐山寻瀑布,香炉峰上披烟雾”,烟雾属于胶体 |
| D.“熬胆矾铁斧,久之亦化为铜”,其中能导电,所以铜是电解质 |
您最近一年使用:0次
名校
解题方法
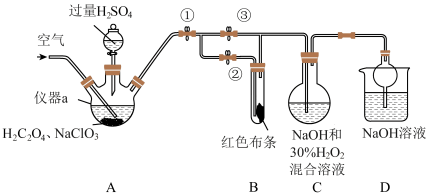
9 . ClO2又称百毒净,可用于水的净化和纸张、纺织品的漂白。用如图所示装置(夹持装置和加热装置省略)制备ClO2并探究ClO2的某些性质。
(1)仪器a的名称为_______ 。
(2)装置A用于制备ClO2且生成的ClO2中混有CO2,该反应的化学方程式为_______ 。
(3)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了NaClO2和气体,该反应体现了H2O2的_______ 性。若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______ 。
(4)D装置的作用是_______ 。
(5)城市饮用水处理,新技术用NaClO2替代Cl2,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂NaClO2的消毒效率是Cl2的_______ 倍(结果保留两位小数)。
(1)仪器a的名称为
(2)装置A用于制备ClO2且生成的ClO2中混有CO2,该反应的化学方程式为
(3)关闭止水夹②,打开止水夹①③,通空气一段时间后,装置C中生成了NaClO2和气体,该反应体现了H2O2的
(4)D装置的作用是
(5)城市饮用水处理,新技术用NaClO2替代Cl2,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂NaClO2的消毒效率是Cl2的
您最近一年使用:0次
2023-10-04更新
|
233次组卷
|
2卷引用:江西省宜春市宜丰中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
10 . Ⅰ.现有以下物质:①NaCl固体 ②盐酸 ③Ba(OH)2溶液 ④铜 ⑤CO2 ⑥硫酸氢钾固体 ⑦乙醇(C2H5OH) ⑧CuSO4·H2O晶体 ⑨熔融态BaSO4 ⑩液氨,请回答下列问题(用序号):
(1)能导电的是_______ ,属于电解质的是_______ ,属于非电解质的是_______ 。
Ⅱ.W、X、Y、Z都是中学化学中常见物质,其中W、X、Y中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)。根据题意回答下列问题:
①除X固体中混有的Y固体的方法为_______ (填除杂方法的名称),反应方程式为_______ 。
②反应Ⅲ的离子方程式为_______ 。
(3)若W为气体单质,Z为一种黑色金属单质。
①反应Ⅱ的离子方程式为_______ 。
②一定条件下,Z能与水发生反应,该反应的化学方程式为_______ 。
(1)能导电的是
Ⅱ.W、X、Y、Z都是中学化学中常见物质,其中W、X、Y中均含有同一种元素,在一定条件下的相互转化关系如图所示(部分反应中的水已略去)。根据题意回答下列问题:
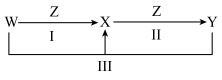
①除X固体中混有的Y固体的方法为
②反应Ⅲ的离子方程式为
(3)若W为气体单质,Z为一种黑色金属单质。
①反应Ⅱ的离子方程式为
②一定条件下,Z能与水发生反应,该反应的化学方程式为
您最近一年使用:0次
2023-10-04更新
|
309次组卷
|
2卷引用:江西省宜春市宜丰中学2022-2023学年高一上学期期末考试化学试题



