名校
解题方法
1 . 下列离子反应方程式正确的是
A.氯气通入冷的石灰乳: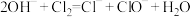 |
B.向NaHCO3溶液中滴入少量澄清石灰水: |
C.向明矾溶液中滴加Ba(OH)2溶液到 恰好完全沉淀时: 恰好完全沉淀时: |
| D.向FeI2溶液中通入少量氯气:Cl2 + 2I- = 2Cl- + I2 |
您最近一年使用:0次
名校
2 . 某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠溶液反应):
①向一粒研碎后的药片(0.50g)中加入20.00mL蒸馏水;
②配制0.50mol/L的稀盐酸250mL和0.50mol/L的NaOH溶液250mL;
③用0.50mol/L的NaOH溶液中和过量的稀盐酸,记录所消耗的NaOH溶液的体积;
④加入25.00mL、0.50mol/L的稀盐酸。
请按要求回答下列问题:
(1)正确的操作顺序是___________ (填序号)。
(2)测定过程中发生反应的离子方程式为:___________ 、___________ 。
(3)该测定实验共进行了4次。4次测定所消耗的NaOH溶液的体积如下表:
①配制上述的稀盐酸时,需要选取的主要玻璃仪器有酸式滴定管(可量取液体体积精确到0.01mL的仪器)、烧杯、玻璃棒、___________ 。
②配制上述的NaOH溶液时,需要用托盘天平称取NaOH固体的质量是___________ 。
③下列操作会导致配制的盐酸浓度偏低的是___________ 。
A.未洗涤玻璃棒和烧杯
B.定容时俯视刻度线
C.洗涤后的容量瓶有残留的蒸馏水
D.摇匀后发现液面低于刻度线,再滴加水至刻度线
④根据相关实验数据,计算这种药片中碳酸钙的质量分数为___________ 。
①向一粒研碎后的药片(0.50g)中加入20.00mL蒸馏水;
②配制0.50mol/L的稀盐酸250mL和0.50mol/L的NaOH溶液250mL;
③用0.50mol/L的NaOH溶液中和过量的稀盐酸,记录所消耗的NaOH溶液的体积;
④加入25.00mL、0.50mol/L的稀盐酸。
请按要求回答下列问题:
(1)正确的操作顺序是
(2)测定过程中发生反应的离子方程式为:
(3)该测定实验共进行了4次。4次测定所消耗的NaOH溶液的体积如下表:
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH(aq)]/mL | 13.02 | 13.22 | 12.98 | 13.00 |
②配制上述的NaOH溶液时,需要用托盘天平称取NaOH固体的质量是
③下列操作会导致配制的盐酸浓度偏低的是
A.未洗涤玻璃棒和烧杯
B.定容时俯视刻度线
C.洗涤后的容量瓶有残留的蒸馏水
D.摇匀后发现液面低于刻度线,再滴加水至刻度线
④根据相关实验数据,计算这种药片中碳酸钙的质量分数为
您最近一年使用:0次
名校
解题方法
3 . “价—类”二维图是研究物质性质的重要工具,如图是硫元素的“价—类”二维图。回答下列问题:_______ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为_______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性_______ (填“增强”或“减弱”)。
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液_______ (填褪色或不褪色),反应的化学方程式为 _______ 。
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出_______ (填“还原”或“漂白”)性。
(6)实验室产生c排放到大气中会引起酸雨,应用_______ 溶液吸收,发生的反应方程式为 _______ 。

(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)实验室产生c排放到大气中会引起酸雨,应用
您最近一年使用:0次
2024-02-22更新
|
227次组卷
|
2卷引用:广东省广州南方学院番禺附属中学2023-2024学年高一下学期3月教学质量监测化学试题
4 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域,实验室中利用如图装置(部分装置省略)制备 和NaClO,并探究其氧化还原性质。
和NaClO,并探究其氧化还原性质。
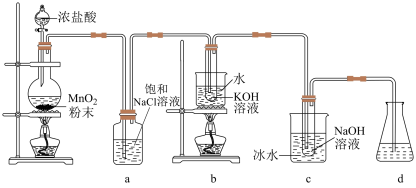
已知:温度会影响 与碱反应氧化产物的价态。
与碱反应氧化产物的价态。
回答下列问题:
(1)发生装置中添加浓盐酸的仪器名称是___________ ,装置a的作用是___________ 。
(2)写出b中试管内反应的化学方程式___________ 。
(3)装置c采用冰水浴冷却的目的是___________ 。
(4)反应结束后,取出b中试管,经蒸发浓缩,___________ ,___________ ,少量冷水洗涤,干燥,得到 晶体。
晶体。
(5)设计实验探究 和NaClO氧化性强弱。实验方案如下,完成下列表格。
和NaClO氧化性强弱。实验方案如下,完成下列表格。
因此, 的氧化能力
的氧化能力___________ (填“大于”或“小于”)NaClO的氧化能力。
(6) 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: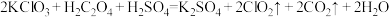 。
。
①请在答题卡上用单线桥表示该反应中电子转移的方向和数目:___________
②“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力(消毒过程中,物质所得电子数相等,认为氧化能力相等)。
的氧化能力(消毒过程中,物质所得电子数相等,认为氧化能力相等)。 的有效氯含量为
的有效氯含量为___________ 。(计算结果保留两位小数)
 和NaClO,并探究其氧化还原性质。
和NaClO,并探究其氧化还原性质。
已知:温度会影响
 与碱反应氧化产物的价态。
与碱反应氧化产物的价态。回答下列问题:
(1)发生装置中添加浓盐酸的仪器名称是
(2)写出b中试管内反应的化学方程式
(3)装置c采用冰水浴冷却的目的是
(4)反应结束后,取出b中试管,经蒸发浓缩,
 晶体。
晶体。(5)设计实验探究
 和NaClO氧化性强弱。实验方案如下,完成下列表格。
和NaClO氧化性强弱。实验方案如下,完成下列表格。| 实验操作 | 现象 | |
| Ⅰ | 取  溶液,振荡。 溶液,振荡。 | 无明显变化 |
| Ⅱ | 取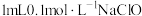 溶液于2号试管中, 溶液于2号试管中, | 出现红褐色沉淀 |
 的氧化能力
的氧化能力(6)
 是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得:
是一种新型含氯消毒剂,已经开始在自来水消毒领域使用。实验室可通过以下反应制得: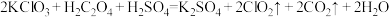 。
。①请在答题卡上用单线桥表示该反应中电子转移的方向和数目:
②“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力(消毒过程中,物质所得电子数相等,认为氧化能力相等)。
的氧化能力(消毒过程中,物质所得电子数相等,认为氧化能力相等)。 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
5 . “化肥也能爆炸”。阅读下面信息材料,回答相关问题。
硝酸铵可用作肥料;一定条件下会剧烈分解生成 、
、 和
和 ,从而发生爆炸因此也可用作军用炸药;易溶于水,且有明显吸热现象,又可作冷冻剂。工业上用
,从而发生爆炸因此也可用作军用炸药;易溶于水,且有明显吸热现象,又可作冷冻剂。工业上用 和
和 在中和器中完成硝酸铵的制备。
在中和器中完成硝酸铵的制备。
(1)上述材料涉及多种含氮的物质,其中有2种属于电解质的是___________ (填化学式)。
(2)根据上述材料写出工业制备硝酸铵的化学方程式___________ ,该反应___________ (填“是”或“否”)属于氧化还原反应。
(3)上述硝酸铵爆炸发生的反应为 ,该反应中被氧化和被还原的N原子数之比为
,该反应中被氧化和被还原的N原子数之比为___________ ,氧化产物为___________ 。
(4)某化学小组需要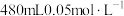 的
的 溶液作为盆栽植物营养液。
溶液作为盆栽植物营养液。
①配制溶液时,现有天平、药匙、烧杯、量筒、玻璃棒,还需要的仪器有___________ 和___________ 。
②根据计算需用天平称取___________ g硝酸铵固体。
③若溶解硝酸铵固体时未待溶液恢复室温就立刻转移到容量瓶进行定容,会导致配制 溶液的浓度
溶液的浓度___________ (填“偏低”、“偏高”或“无影响”)。
硝酸铵可用作肥料;一定条件下会剧烈分解生成
 、
、 和
和 ,从而发生爆炸因此也可用作军用炸药;易溶于水,且有明显吸热现象,又可作冷冻剂。工业上用
,从而发生爆炸因此也可用作军用炸药;易溶于水,且有明显吸热现象,又可作冷冻剂。工业上用 和
和 在中和器中完成硝酸铵的制备。
在中和器中完成硝酸铵的制备。(1)上述材料涉及多种含氮的物质,其中有2种属于电解质的是
(2)根据上述材料写出工业制备硝酸铵的化学方程式
(3)上述硝酸铵爆炸发生的反应为
 ,该反应中被氧化和被还原的N原子数之比为
,该反应中被氧化和被还原的N原子数之比为(4)某化学小组需要
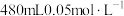 的
的 溶液作为盆栽植物营养液。
溶液作为盆栽植物营养液。①配制溶液时,现有天平、药匙、烧杯、量筒、玻璃棒,还需要的仪器有
②根据计算需用天平称取
③若溶解硝酸铵固体时未待溶液恢复室温就立刻转移到容量瓶进行定容,会导致配制
 溶液的浓度
溶液的浓度
您最近一年使用:0次
名校
6 . 某实验需要用1.0 mol·L-1 NaOH溶液450 mL。
(1)配制该溶液的实验操作步骤有:
a.在托盘天平上称量___________ g NaOH固体放入烧杯中,加适量蒸馏水溶解,冷却至室温。
b.把烧杯中的溶液小心地注入___________ 中。
c.将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2 cm处,改用___________ 加蒸馏水至液面与刻度线相切。
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转入容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
e.将瓶塞塞紧,充分摇匀。
(2)操作步骤的正确顺序为___________ 。
(3)该配制过程中两次用到玻璃棒,其作用分别是___________ 、___________ 。
(4)在进行b步操作时,不慎有液体溅出,下列处理措施正确的是___________(填序号)。
(5)现有硫酸和硫酸钠溶液200 mL,其中硫酸的浓度是1 mol·L-1,硫酸钠的浓度是0.5 mol·L-1.要使硫酸和硫酸钠的浓度分别为2 mol·L-1和0.2 mol·L-1,应加入98%的硫酸(密度为1.84 g·cm-3)的体积是___________ ,再加入水配制后溶液的体积是___________ 。
(1)配制该溶液的实验操作步骤有:
a.在托盘天平上称量
b.把烧杯中的溶液小心地注入
c.将蒸馏水注入容量瓶,液面离容量瓶颈刻度线下1~2 cm处,改用
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转入容量瓶中。轻轻摇动容量瓶,使溶液混合均匀。
e.将瓶塞塞紧,充分摇匀。
(2)操作步骤的正确顺序为
(3)该配制过程中两次用到玻璃棒,其作用分别是
(4)在进行b步操作时,不慎有液体溅出,下列处理措施正确的是___________(填序号)。
| A.继续进行实验 |
| B.添加部分NaOH溶液 |
| C.倒掉溶液,重新配制 |
| D.倒掉溶液,洗净容量瓶后重新配制 |
您最近一年使用:0次
名校
解题方法
7 . 铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
Ⅰ.某学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答下列问题:
(1)实验①中湿棉花、肥皂液作用分别是___________ 、___________ ;实验①中能观察到肥皂液中持续产生肥皂泡,当用燃烧着火柴靠近肥皂泡时,气泡破裂,气体燃烧,火焰呈黄色,并发出轻微的爆鸣声。解释火焰呈黄色的原因___________ ;实验①中反应的化学方程式是___________ 。
(2)实验②前,甲同学对其反应及现象进行预测:向反应后固体加入稀硫酸发生反应的离子方程式_______________ ;实验②中溶液B呈现______ 色,其中发生反应的离子方程式___________ 。
(3)实验②中,乙同学观察到溶液B未呈现红色,则溶液B未呈现红色的原因__________ (用离子方程式表示)。检验B溶液中金属离子的方法_______________ 。
Ⅱ.我国具有5000年文化,文物是活的历史。某博物馆修复出土铁器包括:检测锈蚀产物→分析腐蚀原理→脱氯→形成保护层等过程。
(4)锈蚀产物的主要成分为 、
、 、
、 、
、 、FeOCl。研究发现,出土文物
、FeOCl。研究发现,出土文物 保护层被
保护层被 氧化为
氧化为 而引起腐蚀的。
而引起腐蚀的。 中铁的化合价为
中铁的化合价为_______ 。
(5)利用在NaOH溶液中,溶解度FeOCl大于 ,对固体FeOCl进行脱氯,离子方程式为
,对固体FeOCl进行脱氯,离子方程式为_______________ 。
(6)用 把脱氯产物
把脱氯产物 还原为
还原为 ,生成1mol
,生成1mol  需要
需要___________ mol  。
。
Ⅰ.某学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验① | 实验② |
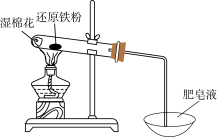 | 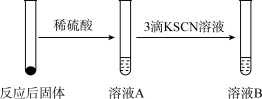 |
(1)实验①中湿棉花、肥皂液作用分别是
(2)实验②前,甲同学对其反应及现象进行预测:向反应后固体加入稀硫酸发生反应的离子方程式
(3)实验②中,乙同学观察到溶液B未呈现红色,则溶液B未呈现红色的原因
Ⅱ.我国具有5000年文化,文物是活的历史。某博物馆修复出土铁器包括:检测锈蚀产物→分析腐蚀原理→脱氯→形成保护层等过程。
(4)锈蚀产物的主要成分为
 、
、 、
、 、
、 、FeOCl。研究发现,出土文物
、FeOCl。研究发现,出土文物 保护层被
保护层被 氧化为
氧化为 而引起腐蚀的。
而引起腐蚀的。 中铁的化合价为
中铁的化合价为(5)利用在NaOH溶液中,溶解度FeOCl大于
 ,对固体FeOCl进行脱氯,离子方程式为
,对固体FeOCl进行脱氯,离子方程式为(6)用
 把脱氯产物
把脱氯产物 还原为
还原为 ,生成1mol
,生成1mol  需要
需要 。
。
您最近一年使用:0次
名校
解题方法
8 . 实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题:
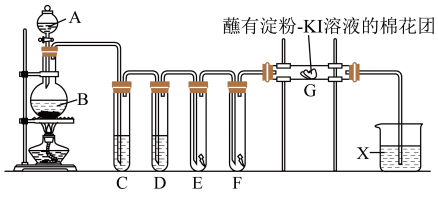
(1)仪器B的名称是______ 。
(2)A中盛有浓盐酸,B中盛有 ,写出反应的化学方程式:
,写出反应的化学方程式:______ 。
(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是______ 。
(4)试管C中试剂为______ 。
(5)用离子方程式表示试剂X的作用:______ 。
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:______ 。

(1)仪器B的名称是
(2)A中盛有浓盐酸,B中盛有
 ,写出反应的化学方程式:
,写出反应的化学方程式:(3)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(4)试管C中试剂为
(5)用离子方程式表示试剂X的作用:
(6)家庭中常用消毒液(主要成分为NaClO)与洁厕灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2.密封保存,请勿与洁厕灵同时使用。 3.保质期为一年。 |
您最近一年使用:0次
名校
解题方法
9 . 下列选项描述与对应图像相符的是
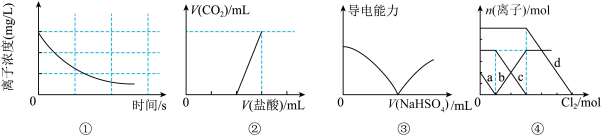

A.图①为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图②为往 与 与 的物质的量之比为 的物质的量之比为 的混合液中滴加盐酸的体积与产生 的混合液中滴加盐酸的体积与产生 体积变化的图像 体积变化的图像 |
C.图③为往 溶液中滴加 溶液中滴加 溶液的体积与导电性变化的图像 溶液的体积与导电性变化的图像 |
D.图④为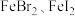 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 |
您最近一年使用:0次
2023-12-27更新
|
541次组卷
|
3卷引用:广东省汕头市金山中学2023-2024学年高一上学期期末考试 化学试题
名校
解题方法
10 . 为了验证氧化性 ,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。

已知:
实验过程:
I.打开弹簧夹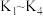 ,通入一段时间
,通入一段时间 ,再将T型导管插入B中,继续通入
,再将T型导管插入B中,继续通入 ,然后关闭
,然后关闭 、
、 、
、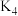 。
。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹 。
。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹 、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹
、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹 。
。
Ⅵ.更换新的试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹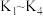 ,再通入一段时间
,再通入一段时间 ,然后拆卸,洗涤,整理仪器。
,然后拆卸,洗涤,整理仪器。
(1)A中反应的化学方程式为___________ 。
(2)棉花中浸润的溶液是___________ 。
(3)步骤Ⅲ中溶液变黄的离子方程式是___________ ,能说明氧化性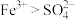 的离子方程式是
的离子方程式是___________ 。
(4)过程Ⅶ的目的是___________ 。
(5)甲、乙、丙三位同学分别完成上述实验,结论如下表所示。他们的检测结果一定能证明氧化性 的是
的是___________ (填“甲”、“乙”、“丙”)。
 ,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
已知:

实验过程:
I.打开弹簧夹
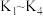 ,通入一段时间
,通入一段时间 ,再将T型导管插入B中,继续通入
,再将T型导管插入B中,继续通入 ,然后关闭
,然后关闭 、
、 、
、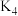 。
。Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹
 。
。Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹
 、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹
、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹 。
。Ⅵ.更换新的试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹
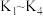 ,再通入一段时间
,再通入一段时间 ,然后拆卸,洗涤,整理仪器。
,然后拆卸,洗涤,整理仪器。(1)A中反应的化学方程式为
(2)棉花中浸润的溶液是
(3)步骤Ⅲ中溶液变黄的离子方程式是
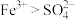 的离子方程式是
的离子方程式是(4)过程Ⅶ的目的是
(5)甲、乙、丙三位同学分别完成上述实验,结论如下表所示。他们的检测结果一定能证明氧化性
 的是
的是| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 既有 ,又有 ,又有 | 有 |
| 乙 | 有 ,无 ,无 | 有 |
| 丙 | 有 ,无 ,无 | 有 |
您最近一年使用:0次



