名校
解题方法
1 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4•7H2O)和氧化铝,其工艺流程如图:
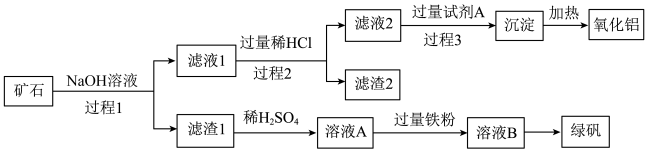
回答下列问题:
(1)滤渣1的成分是_______ ,举例说明滤渣2的用途 _______ 。
(2)用离子方程式表示溶液A加入过量铁粉的目的是_______ 。
(3)写出由滤液1生成滤液2的离子方程式_______ 。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有_______ 。
(5)过程3需要加入的试剂A是_______ ,写出此过程的离子方程式 _______ 。

回答下列问题:
(1)滤渣1的成分是
(2)用离子方程式表示溶液A加入过量铁粉的目的是
(3)写出由滤液1生成滤液2的离子方程式
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有
(5)过程3需要加入的试剂A是
您最近一年使用:0次
名校
解题方法
2 . “价—类”二维图是研究物质性质的重要工具,如图是硫元素的“价—类”二维图。回答下列问题:_______ 。
(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为_______ 。
(3)溶液e久置于空气中会生成f,该过程溶液的酸性_______ (填“增强”或“减弱”)。
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液_______ (填褪色或不褪色),反应的化学方程式为 _______ 。
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出_______ (填“还原”或“漂白”)性。
(6)实验室产生c排放到大气中会引起酸雨,应用_______ 溶液吸收,发生的反应方程式为 _______ 。

(2)反应a+c→b中,氧化产物与还原产物的物质的量之比为
(3)溶液e久置于空气中会生成f,该过程溶液的酸性
(4)Cl2和c都有漂白作用,先将二者以等物质的量混合后再通入到品红溶液中,品红溶液
(5)将c通入到酸性KMnO4溶液中,溶液颜色逐渐变浅,该反应中c表现出
(6)实验室产生c排放到大气中会引起酸雨,应用
您最近一年使用:0次
2024-02-22更新
|
227次组卷
|
2卷引用:新疆 乌鲁木齐市第十二中学2023-2024学年高一上学期1月期末化学试题
名校
3 .  具有强氧化性,
具有强氧化性, 具有还原性,某探究小组的同学学习氧化还原反应的知识后推测
具有还原性,某探究小组的同学学习氧化还原反应的知识后推测 与
与 可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。

Ⅰ.实验探究:
(1)装置A中盛装稀盐酸的仪器名称为___________ ,A装置发生的离子方程式为_____________________ ,B装置的作用是_____________________ ,里面盛放的试剂可以是___________ (填序号)。
A浓硫酸 B.碱石灰 C.无水硫酸铜
(2)下面是实验过程中的重要步骤,选出正确的操作顺序___________ 。
①用小试管收集气体,并检验其纯度
②停止加热,充分冷却后,关闭止水夹 和
和
③加热装有 的硬质玻璃管,使其逐渐熔化,反应一段时间
的硬质玻璃管,使其逐渐熔化,反应一段时间
④打开 和
和 ,滴加稀盐酸
,滴加稀盐酸
(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则 与
与 反应生成的产物为
反应生成的产物为___________ 。
Ⅱ.数据处理:
(4)实验结束以后,该小组的同学还想测定C装置内白色固体中未反应完的 含量。
含量。
操作流程如下:

①操作2的名称________________
②白色固体中 的质量分数为
的质量分数为________________ (用含 和
和 的式子表示)。
的式子表示)。
 具有强氧化性,
具有强氧化性, 具有还原性,某探究小组的同学学习氧化还原反应的知识后推测
具有还原性,某探究小组的同学学习氧化还原反应的知识后推测 与
与 可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
可以发生反应。为了验证他们的猜想,设计了如图所示的实验进行验证。
Ⅰ.实验探究:
(1)装置A中盛装稀盐酸的仪器名称为
A浓硫酸 B.碱石灰 C.无水硫酸铜
(2)下面是实验过程中的重要步骤,选出正确的操作顺序
①用小试管收集气体,并检验其纯度
②停止加热,充分冷却后,关闭止水夹
 和
和
③加热装有
 的硬质玻璃管,使其逐渐熔化,反应一段时间
的硬质玻璃管,使其逐渐熔化,反应一段时间④打开
 和
和 ,滴加稀盐酸
,滴加稀盐酸(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则
 与
与 反应生成的产物为
反应生成的产物为Ⅱ.数据处理:
(4)实验结束以后,该小组的同学还想测定C装置内白色固体中未反应完的
 含量。
含量。操作流程如下:

①操作2的名称
②白色固体中
 的质量分数为
的质量分数为 和
和 的式子表示)。
的式子表示)。
您最近一年使用:0次
名校
解题方法
4 . 某工厂的工业废水中含有大量的 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备
。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备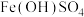 ,流程如下:
,流程如下:
 和较多的
和较多的 。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备
。为减少污染并变废为宝,工厂计划从该废水中回收金属铜,并制备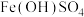 ,流程如下:
,流程如下: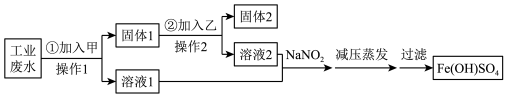
A.甲为铁粉,乙为 溶液 溶液 |
| B.操作1和操作2均用到漏斗、烧杯和玻璃棒,且固体2为铜 |
C.往溶液1与溶液2中加入 反应生成NO,欲制备1.5mol 反应生成NO,欲制备1.5mol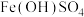 ,理论上至少需要2mol ,理论上至少需要2mol |
D.为检验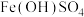 中是否含有 中是否含有 ,加入盐酸溶解,再加入过量NaOH溶液,观察沉淀颜色变化 ,加入盐酸溶解,再加入过量NaOH溶液,观察沉淀颜色变化 |
您最近一年使用:0次
2023-01-12更新
|
418次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
5 . 将 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体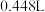 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是
 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体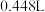 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是A.原混合物中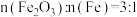 |
B.原混合物中氧化铁的质量为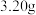 |
C.向所得溶液中滴加 溶液,溶液显红色 溶液,溶液显红色 |
D.向所得溶液中通入 ,可以将 ,可以将 完全转化为 完全转化为 |
您最近一年使用:0次
2023-01-01更新
|
590次组卷
|
6卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一下学期第一次质量检测(开学摸底)化学试题
新疆乌鲁木齐市第八中学2022-2023学年高一下学期第一次质量检测(开学摸底)化学试题辽宁省大连市2022-2023学年高一上学期期末考试化学试题河南省信阳市华中师大息县附中2022-2023学年高一下学期开学考试化学试题山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题江苏省扬州中学2022-2023学年高一下学期4月期中考试化学试题(已下线)综合突破01 期末压轴80题之选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
名校
解题方法
6 . 某同学进行有关 的性质实验。下列说法不正确的是
的性质实验。下列说法不正确的是

 的性质实验。下列说法不正确的是
的性质实验。下列说法不正确的是
| A.图I可以用来收集氯气 |
B.图III中若气球干瘪,证明 可与NaOH反应 可与NaOH反应 |
| C.图II中生成棕黄色的烟,加少量水溶解得到蓝色溶液 |
D.图I中发生反应的离子方程式为 |
您最近一年使用:0次
2022-12-28更新
|
211次组卷
|
2卷引用:新疆乌鲁木齐市第四中学2022-2023学年高一上学期期末考试化学试题
解题方法
7 . 已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
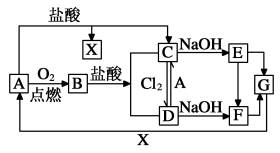
(1)写出A、C、F、G的化学式:A_____ ,C_____ ,F____ ,G_____ 。
(2)写出B与盐酸反应的离子方程式_____ 。
(3)检验D中阳离子的试剂常用_____ 。
(4)①写出下列转化的离子方程式C→D:_____ 。
②写出的化学方程式E→F:____ ,由E转化为F的现象是____ 。

(1)写出A、C、F、G的化学式:A
(2)写出B与盐酸反应的离子方程式
(3)检验D中阳离子的试剂常用
(4)①写出下列转化的离子方程式C→D:
②写出的化学方程式E→F:
您最近一年使用:0次
名校
解题方法
8 . 已知:将Cl2通入适量NaOH溶液中,反应会放热,当温度升高后会发生如下反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O。则Cl2通入NaOH溶液的产物中可能有NaCl、NaClO、NaClO3中的两种或三种,且 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是| A.与碱的反应中,Cl2既是氧化剂又是还原剂 |
| B.参加反应的Cl2物质的量为0.5a mol |
C.若某温度下,反应后 =6,则溶液中 =6,则溶液中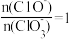 |
D.改变温度,反应中转移电子的物质的量可能为 mol mol |
您最近一年使用:0次
2022-10-24更新
|
2092次组卷
|
12卷引用:新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题
新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题江苏省无锡市锡山高级中学2021-2022学年高一上学期期中考试化学试题山东省实验中学2022-2023学年高一上学期11月期中考试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高一上学期期中考试化学(A卷)试题北京市第八中学2022-2023学年高一上学期12月月考化学试题陕西省榆林中学2022-2023学年高一上学期期末考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题江苏省苏州中学2022-2023学年高一下学期开学考试化学试题陕西省安康市2022-2023学年高一下学期开学摸底考试化学试题辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
11-12高二上·浙江嘉兴·期中
9 . 已知在酸性溶液中,下列物质氧化 时,自身发生如下变化:
时,自身发生如下变化: ,
, ,
, ,
,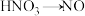 ,如果分别用相同数目的这些微粒氧化足量的
,如果分别用相同数目的这些微粒氧化足量的 ,得到
,得到 最多的是
最多的是
 时,自身发生如下变化:
时,自身发生如下变化: ,
, ,
, ,
,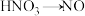 ,如果分别用相同数目的这些微粒氧化足量的
,如果分别用相同数目的这些微粒氧化足量的 ,得到
,得到 最多的是
最多的是A. | B. | C. | D. |
您最近一年使用:0次
2022-01-21更新
|
317次组卷
|
24卷引用:【全国百强校】新疆维吾尔自治区生产建设兵团第二中学2018-2019学年高一上学期期中检测化学试题
【全国百强校】新疆维吾尔自治区生产建设兵团第二中学2018-2019学年高一上学期期中检测化学试题新疆昌吉教育共同体2020-2021学年高一下学期期末质量检测化学试题(已下线)2011-2012学年北京市师大附中高一上学期期中考试化学试卷(已下线)2012-2013学年河北枣强县中学高一上学期期末考试化学试卷(已下线)2014—2015学年甘肃兰州一中高一上学期期中考试化学卷上海交通大学附属中学2016-2017学年高一下学期质量检测一(3月)化学试题山东省曲阜师范大学附属中学2017-2018学年高一上学期期中考试化学试题北京师范大学附属中学2017-2018学年高一上学期期中考试化学试题【全国百强校】内蒙古鄂尔多斯市第一中学2018-2019学年高一上学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第三中学校2018-2019学年高一上学期第二次月考化学试题安徽省阜阳市第三中学2019-2020学年高一上学期第二次调研考试化学试题山西省祁县第二中学校2019-2020学年高一上学期期中考试化学试题四川省三台中学2019-2020学年高一上学期第三次月考化学试题河北省辛集市第一中学2021-2022学年高一上学期第一次月考化学试题河北省石家庄市第一中学2021-2022学年高一上学期期中考试化学试卷吉林省洮南市第一中学2021-2022学年高一上学期期中考试化学试题内蒙古呼和浩特市2021-2022学年高一上学期期末考试化学试题内蒙古赤峰二中2021-2022学年高一上学期第二次月考化学试题北京市北京师范大学附属中学2022-2023学年高一上学期期中考试化学试题北京市清华大学附属中学2023-2024学年高一上学期12月统练二化学试题 河北省石家庄市第二中学西校区2023-2024学年高一上学期12月月考化学试题北京师范大学附属中学2023-2024学年高一上学期期中考试化学试题北京市陈经纶中学2023-2024学年高一上学期12月月考化学试卷 (已下线)2011-2012学年浙江省嘉兴一中高二上学期期中考试化学试卷
10 . 根据下面实验过程得出的结论,不正确的是
| 选项 | 实验过程 | 实验结论 |
| A | 红热的木炭放入盛有氧气的集气瓶中,剧烈燃烧发出白光 | 氧气浓度大,木炭燃烧剧烈 |
| B | 湿润的蓝色石蕊试纸放入盛有二氧化碳气体的集气瓶中,蓝色 石蕊试纸变为红色 | 二氧化碳能与水反应生成碳酸 |
| C | 氢氧化钠固体置于空气中,表面很快变得潮湿并逐渐溶解 | 氢氧化钠固体有吸水性 |
| D | 向未知溶液中滴加氯化钡试液,有白色沉淀生成,再滴加稀硝 酸,沉淀不消失 | 溶液中一定含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-22更新
|
150次组卷
|
2卷引用:新疆叶城县第八中学2021-2022学年高一上学期期中考试化学试题



