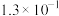解题方法
1 . 电化学原理在工业生产中有重要的应用,根据电化学原理完成下列问题。
(1)用 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)

①图中a极要连接电源的(填“正”或“负”)___________ 极,C口流出的物质是___________ 。
② 放电的电极反应式为
放电的电极反应式为___________ 。
(2)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①生成锂单质的电极反应式是___________ 。
②理论分析,阳极电解产物可能有 。生成
。生成 的电极反应式是
的电极反应式是___________ 。
(1)用
 溶液吸收烟气中的
溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生
溶液进行电解,可循环再生 ,同时得到
,同时得到 ,其原理如下图所示。(电极材料为石墨)
,其原理如下图所示。(电极材料为石墨)
①图中a极要连接电源的(填“正”或“负”)
②
 放电的电极反应式为
放电的电极反应式为(2)我国科学家通过电解,从海水中提取到锂单质,其工作原理如图所示。

①生成锂单质的电极反应式是
②理论分析,阳极电解产物可能有
 。生成
。生成 的电极反应式是
的电极反应式是
您最近一年使用:0次
解题方法
2 . 回答下列问题
(1)已知 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为___________ 。
(2)常温下,用 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡___________ (填“向左”、“向右”或“不”)移动。试计算该溶液中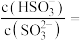
___________ (常温下 的电离平衡常数
的电离平衡常数 ,
, )。
)。
(3)保险粉样品中 的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为
的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为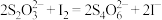 。准确称取
。准确称取 样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用
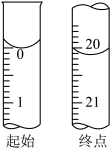
样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用 碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是
碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是___________ 。滴定起始和终点的液面位置如图所示。则样品的纯度为___________ 。(设 的摩尔质量为
的摩尔质量为 )
)
(4)化工生产中常用 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为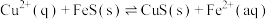 。下列有关叙述正确的是
。下列有关叙述正确的是___________ 。
a、
b、达到平衡时
c、该反应平衡常数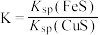
(1)已知
 (次磷酸)的水溶液中存在
(次磷酸)的水溶液中存在 分子。
分子。 与足量
与足量 溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为(2)常温下,用
 溶液吸收
溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡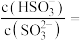
 的电离平衡常数
的电离平衡常数 ,
, )。
)。(3)保险粉样品中
 的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为
的纯度(质量分数)可通过氧化还原滴定法来测定,反应的离子方程式为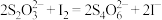 。准确称取
。准确称取 样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用
样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用 碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是
碘的标准溶液进行滴定,判断达到滴定终点的操作和现象是 的摩尔质量为
的摩尔质量为 )
)
(4)化工生产中常用
 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的 ,其反应原理为
,其反应原理为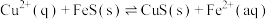 。下列有关叙述正确的是
。下列有关叙述正确的是a、

b、达到平衡时

c、该反应平衡常数
您最近一年使用:0次
3 . 回答下列问题。
(1)现有常温下 的盐酸(甲)、
的盐酸(甲)、 的醋酸溶液(乙)和
的醋酸溶液(乙)和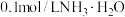 (丙),请根据下列操作回答:
(丙),请根据下列操作回答:
①常温下,将丙溶液加水稀释,下列数值变大的是___________ (填字母)。
A. B.
B. C.
C. D.
D.
②已知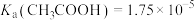 ,则醋酸溶液(乙)的浓度为
,则醋酸溶液(乙)的浓度为_______  (结果保留三位有效数字)。
(结果保留三位有效数字)。
③常温下,取甲、乙各1mL分别稀释至100mL,稀释后,溶液的pH:甲______ 乙(填“>”“<”或“=”)。
(2)①相同条件下,取相同体积、相同pH的 、
、 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为________ 。
②某温度下,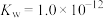 ,将
,将 的
的 溶液和
溶液和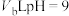 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
___________ 。
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表:
①将 通入氨水中,当
通入氨水中,当 降至
降至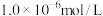 时,溶液中的
时,溶液中的
___________ 。
②下列微粒在溶液中不能大量共存的是___________ 。
A. 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
(1)现有常温下
 的盐酸(甲)、
的盐酸(甲)、 的醋酸溶液(乙)和
的醋酸溶液(乙)和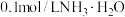 (丙),请根据下列操作回答:
(丙),请根据下列操作回答:①常温下,将丙溶液加水稀释,下列数值变大的是
A.
 B.
B. C.
C. D.
D.
②已知
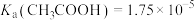 ,则醋酸溶液(乙)的浓度为
,则醋酸溶液(乙)的浓度为 (结果保留三位有效数字)。
(结果保留三位有效数字)。③常温下,取甲、乙各1mL分别稀释至100mL,稀释后,溶液的pH:甲
(2)①相同条件下,取相同体积、相同pH的
 、
、 和
和 三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为
三种碱溶液,分别滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为 、
、 、
、 ,则三者的大小关系为
,则三者的大小关系为②某温度下,
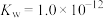 ,将
,将 的
的 溶液和
溶液和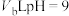 的
的 溶液混合均匀,测得溶液的
溶液混合均匀,测得溶液的 ,则
,则
(3)已知:在25℃,有关弱电解质的电离平衡常数如下表:
| 弱电解质 |  |  |  |  |
| 电离平衡常数 |   |   |  |  |
 通入氨水中,当
通入氨水中,当 降至
降至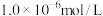 时,溶液中的
时,溶液中的
②下列微粒在溶液中不能大量共存的是
A.
 、
、 B.
B. 、
、 C.
C. 、
、 D.
D. 、
、
您最近一年使用:0次
2024-02-04更新
|
95次组卷
|
2卷引用:湖北省应城市2023-2024学年高二上学期1月期末考试化学试题
4 . 已知25℃时,部分弱电解质的电离常数如下表所示:
(1)四种酸 、
、 、
、 、
、 的酸性从强到弱的顺序
的酸性从强到弱的顺序______ 。
(2) 时,将
时,将 溶液和
溶液和
 氨水混合,所得溶液呈
氨水混合,所得溶液呈______ (填“酸”“中”或“碱”)性。
(3) 时,向
时,向 的
的 溶液中逐滴加入
溶液中逐滴加入 溶液,所得混合溶液呈酸性。
溶液,所得混合溶液呈酸性。
①混合溶液中的粒子浓度由大到小的顺序( 除外):
除外):______ 。
②针对该混合溶液,下列说法正确的是______ 。
A.混合溶液存在
B.向混合溶液中继续滴加蒸馏水,溶液酸性减弱, 数值会增大
数值会增大
C.继续向溶液中滴加 溶液至
溶液至 值为6,
值为6,
D.继续滴加 溶液至大于
溶液至大于 时,可能有水电离出
时,可能有水电离出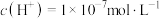
(4)若向 溶液中通入少量
溶液中通入少量 气体,写出发生反应的离子方程式:
气体,写出发生反应的离子方程式:______ 。
弱酸 |
|
|
|
|
|
电离常数 |
|
|
|
|
|
(1)四种酸
 、
、 、
、 、
、 的酸性从强到弱的顺序
的酸性从强到弱的顺序(2)
 时,将
时,将 溶液和
溶液和
 氨水混合,所得溶液呈
氨水混合,所得溶液呈(3)
 时,向
时,向 的
的 溶液中逐滴加入
溶液中逐滴加入 溶液,所得混合溶液呈酸性。
溶液,所得混合溶液呈酸性。①混合溶液中的粒子浓度由大到小的顺序(
 除外):
除外):②针对该混合溶液,下列说法正确的是
A.混合溶液存在

B.向混合溶液中继续滴加蒸馏水,溶液酸性减弱,
 数值会增大
数值会增大C.继续向溶液中滴加
 溶液至
溶液至 值为6,
值为6,
D.继续滴加
 溶液至大于
溶液至大于 时,可能有水电离出
时,可能有水电离出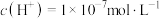
(4)若向
 溶液中通入少量
溶液中通入少量 气体,写出发生反应的离子方程式:
气体,写出发生反应的离子方程式:
您最近一年使用:0次
5 . 常温下,根据表中的几种物质的电离平衡常数回答下列问题:
(1)下列四种离子结合质子能力由大到小的顺序是_____ (填序号)。
a. b.
b. c.
c. d.
d.
(2)下列反应不能发生的是___________ (填序号)。
a.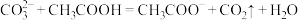
b.
C.
d.
(3)反应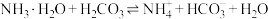 的平衡常数
的平衡常数
________ 。
| 弱酸 |  |  |  | HClO |
| 电离平衡常数 |  | 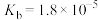 | 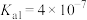 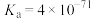 | 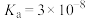 |
a.
 b.
b. c.
c. d.
d.
(2)下列反应不能发生的是
a.
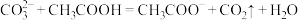
b.

C.

d.

(3)反应
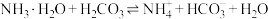 的平衡常数
的平衡常数
您最近一年使用:0次
名校
6 . 新能源汽车所用蓄电池分为铅酸蓄电池、二次锂电池、空气电池等。铅酸蓄电池是常见的二次电池,应用非常广泛。电池反应式为:Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l)。
2PbSO4(s)+2H2O(l)。
(1)电池工作时负极的电极反应式为________ ,放电过程中电解质溶液的pH_____ (填“增大”、“减小”或“不变”),充电时与外接电源的正极极相接的是_______ (填“Pb”或“PbO2”)。
(2)若用该电池作电源,用石墨作电极电解饱和氯化钠溶液,其示意图如下:

①Na+向_____ (填“c”或“d”)极移动,溶液A的溶质为________ 。(填化学式)
②电解总反应的离子方程式为________ 。
③当阳极收集到33.6 L(标准状况)气体时,铅蓄电池的负极将增重_____ g,若要使电解质溶液复原,可向电解后的溶液中加入或通入的物质___________ 。(填化学式)
 2PbSO4(s)+2H2O(l)。
2PbSO4(s)+2H2O(l)。(1)电池工作时负极的电极反应式为
(2)若用该电池作电源,用石墨作电极电解饱和氯化钠溶液,其示意图如下:

①Na+向
②电解总反应的离子方程式为
③当阳极收集到33.6 L(标准状况)气体时,铅蓄电池的负极将增重
您最近一年使用:0次
名校
7 . 氢能是发展中的新能源,它的利用包括氢的制备和储存。回答下列问题:
(1)如图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为_____ (用a、b表示)。
②正极反应式为_____ 。
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此储氢是关键技术之一、某些金属氢化物可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g) MHx+2y(s)达到化学平衡。下列有关叙述正确的是
MHx+2y(s)达到化学平衡。下列有关叙述正确的是_____ 。
a.v(放氢)=v(吸氢)
b.若通入惰性气体Ar,压强增大,反应速率增大
c.容器内气体压强保持不变
d.吸收ymolH2只需1molMHx
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_____ 。
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取Na2FeO4的同时还能获得氢气:Fe+2H2O+2OH- FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
①电解一段时间后,c(OH−)降低的区域在_____ (填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_____ 。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c(Na2FeO4)低于最高值的原因:_____ 。
(1)如图为碱性氢氧燃料电池的示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①在导线中电子流动方向为
②正极反应式为
(2)氢氧燃料电池工作时,H2和O2连续由外部供给,因此储氢是关键技术之一、某些金属氢化物可做储氢材料,在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)
 MHx+2y(s)达到化学平衡。下列有关叙述正确的是
MHx+2y(s)达到化学平衡。下列有关叙述正确的是a.v(放氢)=v(吸氢)
b.若通入惰性气体Ar,压强增大,反应速率增大
c.容器内气体压强保持不变
d.吸收ymolH2只需1molMHx
(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
(4)化工生产的副产品氢气,也是氢气的一种来源。电解法制取Na2FeO4的同时还能获得氢气:Fe+2H2O+2OH-
 FeO
FeO +3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO ,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
①电解一段时间后,c(OH−)降低的区域在
②电解过程中,须将阴极产生的气体及时排出,其原因是
③c(Na2FeO4)随初始c(NaOH)的变化如图2,分析N点c(Na2FeO4)低于最高值的原因:
您最近一年使用:0次
名校
8 . 甲、乙两池电极材料都是铁棒与碳棒(如图)。请回答下列问题:

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的___________ 棒;乙池中的___________ 棒。
②在乙池中阳极的电极反应式是___________ 。
(2)若两池中均盛放饱和NaCl溶液。
①写出甲池中正极的电极反应式___________ 。
②写出乙池中的总反应的离子方程式___________ 。
③据资料显示电解氯化钠稀溶液可制备“84消毒液”(主要成分为NaClO),通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出该电解的化学方程式___________ 。

(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的
②在乙池中阳极的电极反应式是
(2)若两池中均盛放饱和NaCl溶液。
①写出甲池中正极的电极反应式
②写出乙池中的总反应的离子方程式
③据资料显示电解氯化钠稀溶液可制备“84消毒液”(主要成分为NaClO),通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出该电解的化学方程式
您最近一年使用:0次
名校
9 . 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程式为___________ 。
(2)常温下,某化学兴趣小组在实验室中用石墨电极以如图所示装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下的氢气2.24L。(设电解前后溶液的体积均为1L,不考虑水的蒸发或气体的溶解)

①理论上,电解后溶液的pH≈___________ 。
②若实际测得反应后溶液的pH=13.00,则造成这种误差的原因可能是:
a.氯气和氢氧化钠溶液反应;
b.还可能为___________ (用化学方程式表示)。
(1)电解饱和食盐水的化学方程式为
(2)常温下,某化学兴趣小组在实验室中用石墨电极以如图所示装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下的氢气2.24L。(设电解前后溶液的体积均为1L,不考虑水的蒸发或气体的溶解)

①理论上,电解后溶液的pH≈
②若实际测得反应后溶液的pH=13.00,则造成这种误差的原因可能是:
a.氯气和氢氧化钠溶液反应;
b.还可能为
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)“84”消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈___________ 性(填“酸”“碱”或“中”),用离子方程式表示其原因___________ 。
(2)25℃时,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为___________ 。该温度下,若pH=a的100体积某强酸溶液与pH=b的1体积某强碱溶液混合后溶液呈中性,则a+b=___________ 。
(3)向浓度均为0.1mol•L-1的CdCl2和ZnCl2混合液中滴加碳酸铵溶液至生成两种沉淀,则溶液中c(Zn2+):c(Cd2+)=___________ 。[已知:Ksp(CdCO3)=1.0×10-12、Ksp(ZnCO3)=1.5×10-10]
(4)相同条件下,0.1mol•L-1下列溶液中,c( )最大的是
)最大的是_______ ,c( )最小的是
)最小的是_______ (填序号)。
A.(NH4)2SO4 B.(NH4)2CO3 C.NH4Cl D.NH4HSO4 E.NH3∙H2O
(1)“84”消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈
(2)25℃时,pH均为3的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为
(3)向浓度均为0.1mol•L-1的CdCl2和ZnCl2混合液中滴加碳酸铵溶液至生成两种沉淀,则溶液中c(Zn2+):c(Cd2+)=
(4)相同条件下,0.1mol•L-1下列溶液中,c(
 )最大的是
)最大的是 )最小的是
)最小的是A.(NH4)2SO4 B.(NH4)2CO3 C.NH4Cl D.NH4HSO4 E.NH3∙H2O
您最近一年使用:0次