名校
解题方法
1 . 化学用语是学习化学的重要工具,下列化学用语表述错误的是
A. 的空间填充模型为 的空间填充模型为 | B.2-甲基-2-戊烯的键线式为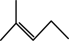 |
C.基态 的价电子排布式为 的价电子排布式为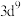 | D. 的电子式为 的电子式为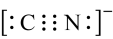 |
您最近一年使用:0次
7日内更新
|
374次组卷
|
2卷引用:吉林省长春市东北师范大学附属实验学校2023-2024学年高三下学期七模化学试题
2 . 下列实验操作或处理方法错误的是
A.点燃 前,先检验其纯度 前,先检验其纯度 | B.金属K着火,用湿抹布盖灭 |
| C.温度计中水银洒落地面,用硫粉处理 | D.苯酚沾到皮肤上,先后用乙醇、水冲洗 |
您最近一年使用:0次
7日内更新
|
1903次组卷
|
4卷引用:2024年吉林省高考化学试题
名校
3 . 按要求回答下列问题:
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
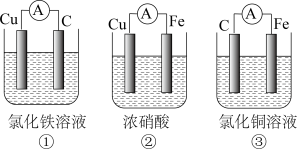
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是_______ (填序号)。_______ 。
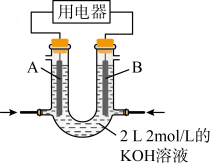
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。_______ (填“A”或“B”)处电极入口通甲烷,其电极反应式为_______ 。当消耗甲烷的体积为33.6 L(标准状况)时,假设电池的能量转化率为80%,导线中转移电子的物质的量为_______ 。
(1)反应A+B→C(放热)分两步进行①A+B→X(吸热);②X→C(放热)。下列示意图中,能正确表示总反应过程中能量变化的是_______。
A.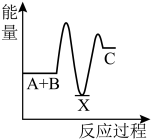 | B.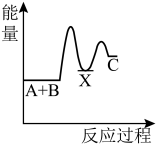 | C.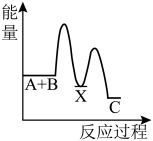 | D.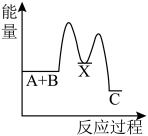 |
(2)下图是一氧化碳和氧在钌催化剂的表面形成化学键的过程。下列说法正确的是_______。
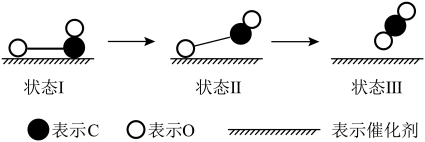
A. 和 和 均为酸性氧化物 均为酸性氧化物 | B.该过程中, 先断键成C和O 先断键成C和O |
| C.状态I到状态Ⅲ为放热过程 | D.图示表示 和 和 反应生成 反应生成 的过程 的过程 |
(3)为了验证Fe2+与Cu2+氧化性强弱,下列装置能达到实验目的的是
(4)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
您最近一年使用:0次
真题
4 . 如下图所示的自催化反应,Y作催化剂。下列说法正确的是
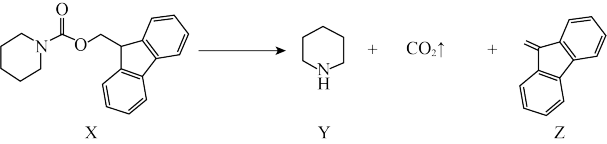
| A.X不能发生水解反应 | B.Y与盐酸反应的产物不溶于水 |
C.Z中碳原子均采用 杂化 杂化 | D.随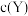 增大,该反应速率不断增大 增大,该反应速率不断增大 |
您最近一年使用:0次
7日内更新
|
2347次组卷
|
4卷引用:2024年吉林省高考化学试题
真题
5 . 硫及其化合物部分转化关系如图。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是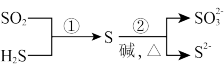
A.标准状况下,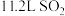 中原子总数为 中原子总数为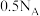 |
B.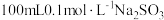 溶液中, 溶液中, 数目为 数目为 |
C.反应①每消耗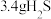 ,生成物中硫原子数目为 ,生成物中硫原子数目为 |
D.反应②每生成 还原产物,转移电子数目为 还原产物,转移电子数目为 |
您最近一年使用:0次
7日内更新
|
2022次组卷
|
4卷引用:2024年吉林省高考化学试题
真题
6 . 下列化学用语或表述正确的是
A.中子数为1的氦核素: | B. 的晶体类型:分子晶体 的晶体类型:分子晶体 |
C. 的共价键类型: 的共价键类型: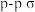 键 键 | D. 的空间结构:平面三角形 的空间结构:平面三角形 |
您最近一年使用:0次
7日内更新
|
1983次组卷
|
4卷引用:2024年吉林省高考化学试题
名校
7 . 回答下列问题。
(1)维生素C是重要的营养素,其分子结构如图所示:_______ 。
(2)有机物的结构为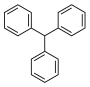 一氯代物有
一氯代物有_______ 种。
(3)C4H8ClBr的同分异构体有_______ 种(不考虑立体异构)。
(4)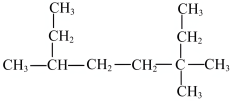 系统命名为
系统命名为_______ ;若该物质是某烯烃(只含1个双键)与 加成后的产物,则该烯烃可能的结构简式有
加成后的产物,则该烯烃可能的结构简式有_______ 种(不考虑顺反异构)。
(5)分子式为C5H12O的醇,能被催化氧化成醛的同分异构体有_______ 种。
(1)维生素C是重要的营养素,其分子结构如图所示:
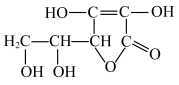
(2)有机物的结构为
 一氯代物有
一氯代物有(3)C4H8ClBr的同分异构体有
(4)
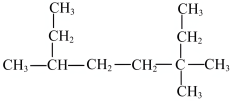 系统命名为
系统命名为 加成后的产物,则该烯烃可能的结构简式有
加成后的产物,则该烯烃可能的结构简式有(5)分子式为C5H12O的醇,能被催化氧化成醛的同分异构体有
您最近一年使用:0次
8 . 2-溴戊二酸二甲酯(相对分子质量为239)是某抗癌药物的重要中间体,其制备的反应原理如图所示:
步骤一:制备
将10.0g戊二酸(固态,相对分子质量为132)加入到三颈烧瓶中,再向其中加入三氯甲烷25mL,搅拌均匀,保持78℃条件下,依次缓慢滴加12mL氯化亚砜、3滴催化剂、10ml液溴,随后回流;回流完毕后,将三颈烧瓶置于冰盐浴中,将溶液温度降到-10℃后,缓慢滴加25mL甲醇(沸点64.7℃)保持滴加过程中温度不超过0℃。
步骤二:除杂
向三颈烧瓶中加入25mL饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用25mL饱和氯化钠溶液洗涤3次,洗涤完毕,“用无水硫酸镁干燥,过滤。
步骤三:提纯
过滤后的液体置于热浴容器中(外温170℃),接上精馏装置,进行减压蒸馏。
步骤四:收集
收集100—110℃的馏分,得到10.86g无色透明油状液体。
回答下列问题:
(1)使用装置A的优点是_____________ ,三颈烧瓶宜选择的规格是__________ (填标号)。
A.50mL B.150mL C.200mL D.500mL
(2)步骤一中采取“温度降到-10℃”“缓慢滴加”这些措施的可能原因有_____________ 。
a.减缓反应速率
b.防止高温下发生复杂的有机副反应
c.避免原料挥发,使反应物充分反应
(3)步骤二中用饱和氯化钠溶液洗涤的目的是_______________ 。
(4)步骤三中使用减压蒸馏的目的是______________ 。
(5)中间产物Ⅰ比戊二酸的沸点低很多的原因是_______________ ,反应中生成中间产物1(戊二酰氯)的同时得到两种有刺激性气味的气体,该反应的化学方程式为________________ 。
(6)从环保角度分析,该实验装置存在明显不足之处,解决的办法是_____________ 。
(7)本实验的产率约是 。

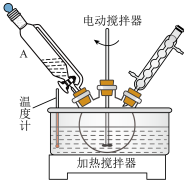
步骤一:制备
将10.0g戊二酸(固态,相对分子质量为132)加入到三颈烧瓶中,再向其中加入三氯甲烷25mL,搅拌均匀,保持78℃条件下,依次缓慢滴加12mL氯化亚砜、3滴催化剂、10ml液溴,随后回流;回流完毕后,将三颈烧瓶置于冰盐浴中,将溶液温度降到-10℃后,缓慢滴加25mL甲醇(沸点64.7℃)保持滴加过程中温度不超过0℃。
步骤二:除杂
向三颈烧瓶中加入25mL饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用25mL饱和氯化钠溶液洗涤3次,洗涤完毕,“用无水硫酸镁干燥,过滤。
步骤三:提纯
过滤后的液体置于热浴容器中(外温170℃),接上精馏装置,进行减压蒸馏。
步骤四:收集
收集100—110℃的馏分,得到10.86g无色透明油状液体。
回答下列问题:
(1)使用装置A的优点是
A.50mL B.150mL C.200mL D.500mL
(2)步骤一中采取“温度降到-10℃”“缓慢滴加”这些措施的可能原因有
a.减缓反应速率
b.防止高温下发生复杂的有机副反应
c.避免原料挥发,使反应物充分反应
(3)步骤二中用饱和氯化钠溶液洗涤的目的是
(4)步骤三中使用减压蒸馏的目的是
(5)中间产物Ⅰ比戊二酸的沸点低很多的原因是
(6)从环保角度分析,该实验装置存在明显不足之处,解决的办法是
(7)本实验的产率约是 。
| A.30% | B.50% | C.60% | D.80% |
您最近一年使用:0次
名校
9 . 铁(Fe)、钴(Co)、镍(Ni)是第四周期第VⅢ族的元素,在化学上称为铁系元素,其合金和化合物在生产生活中应用广泛。
(1)基态Ni原子的价层电子排布图为_____________ 。
(2) 的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是
的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是_____________ ,氮有_____________ 种不同空间运动状态的电子。
(3) 在水溶液中以
在水溶液中以 的形式存在。向含
的形式存在。向含 的溶液中加入过量氨水可生成更稳定的
的溶液中加入过量氨水可生成更稳定的 ,试分析
,试分析 更稳定的原因是
更稳定的原因是________________ 。
(4)硫酸镍溶于氨水形成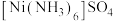 蓝色溶液。
蓝色溶液。
① 的空间构型为
的空间构型为_____________ 。
②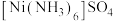 含有的化学键类型包括
含有的化学键类型包括_____________ (填字母)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.非极性共价键
(5)一种Al-Fe合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。若此合金中Al、Fe原子核中心之间最近的距离为a pm,则此合金的密度
__________  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,列出计算式即可)。
,列出计算式即可)。
(1)基态Ni原子的价层电子排布图为
(2)
 的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是
的检验试剂常用硫氰化钾(KSCN),K、S、C、N四种元素中电负性最大的是(3)
 在水溶液中以
在水溶液中以 的形式存在。向含
的形式存在。向含 的溶液中加入过量氨水可生成更稳定的
的溶液中加入过量氨水可生成更稳定的 ,试分析
,试分析 更稳定的原因是
更稳定的原因是(4)硫酸镍溶于氨水形成
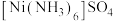 蓝色溶液。
蓝色溶液。①
 的空间构型为
的空间构型为②
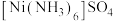 含有的化学键类型包括
含有的化学键类型包括A.极性共价键 B.离子键 C.配位键 D.金属键 E.非极性共价键
(5)一种Al-Fe合金的立方晶胞如图所示,其沿x轴、y轴、z轴的投影完全相同。若此合金中Al、Fe原子核中心之间最近的距离为a pm,则此合金的密度

 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,列出计算式即可)。
,列出计算式即可)。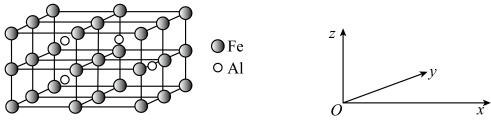
您最近一年使用:0次
10 . 有关晶体的结构如下图所示。下列说法错误的是
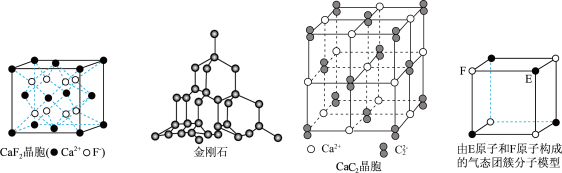
A.在 晶体中,每个晶胞平均占有4个 晶体中,每个晶胞平均占有4个 |
| B.在金刚石晶体中,碳原子与碳碳键个数之比为1∶2 |
C.在 晶体中,1个 晶体中,1个 周围等距离且最近的 周围等距离且最近的 有6个 有6个 |
| D.由E原子和F原子构成的气态团簇分子的分子式为EF或FE |
您最近一年使用:0次



