1 . 用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。
已知:
ⅰ.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ.2中曲线Ⅰ的离子浓度关系符合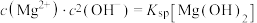 ;
;
曲线Ⅱ的离子浓度关系符合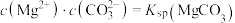 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。
 在不同pH的
在不同pH的 体系中的可能产物。
体系中的可能产物。已知:
ⅰ.图1中曲线表示
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ⅱ.2中曲线Ⅰ的离子浓度关系符合
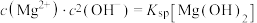 ;
;曲线Ⅱ的离子浓度关系符合
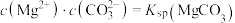 [注:起始
[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图1得到]。
由图1得到]。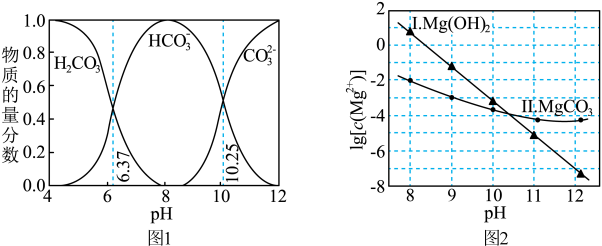
A.由图1可知,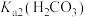 的数量级是 的数量级是 |
B.由图2,若初始状态 , , ,无沉淀生成 ,无沉淀生成 |
C.由图2,若初始状态 , ,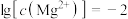 ,平衡后溶液中存在 ,平衡后溶液中存在 mol/L mol/L |
D.由图1和图2,若初始状态 , ,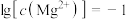 ,发生反应: ,发生反应: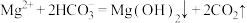 |
您最近一年使用:0次
7日内更新
|
44次组卷
|
2卷引用:安徽省江南十校2023-2024学年高二下学期5月阶段联考化学B试题
解题方法
2 . 下列有关“类比”合理的是
| A.碳酸钠固体溶于水放热,则碳酸氢钠固体溶于水也放热 |
| B.Mg、Al与稀盐酸构成的原电池中较活泼的Mg作负极,故Mg、Al与氢氧化钠溶液构成的原电池中也是Mg作负极 |
C.铜与硫黄加热反应生成 ,则铁粉与硫黄加热反应生成FeS ,则铁粉与硫黄加热反应生成FeS |
D. 中Cl的化合价为+1,则 中Cl的化合价为+1,则 中F的化合价为+1 中F的化合价为+1 |
您最近一年使用:0次
名校
解题方法
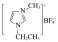
3 . 2019年诺贝尔化学奖颁给研究锂电池的科学家,一种用作锂电池电解液的锂盐的结构如图所示,其中X位于第三周期,X原子的电子数为Z原子电子数的两倍,W、Z、Y位于同一周期,下列叙述正确的是

| A.W、X、Y、Z四种元素对应的简单氢化物的稳定性依次减弱 |
B.Z、W的非金属性强弱可以通过比较 和 和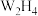 的热稳定性进行判断 的热稳定性进行判断 |
| C.X的氧化物对应的水化物均为强酸 |
D. 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
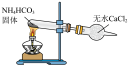
4 . 下列实验装置(部分夹持装置已略去)可以达到对应实验目的的是
| 实验目的 | A.加热熔融NaOH固体 | B.除去 中的少量HCl 中的少量HCl |
| 实验装置 |
|
|
| 实验目的 | C.实验室制取干燥的氨气 | D.灼烧海带 |
| 实验装置 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列叙述正确的个数是
①常温常压下,17g甲基(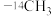 )所含的中子数为
)所含的中子数为
②1molBrCl与 完全反应生成氯化氢和次溴酸,转移的电子的物质的量为1mol
完全反应生成氯化氢和次溴酸,转移的电子的物质的量为1mol
③0℃,101kPa含有1mol硫原子的 与
与 的混合物,其体积小于22.4L
的混合物,其体积小于22.4L
④用 检验
检验 的现象为产生大量白烟
的现象为产生大量白烟
⑤可用石灰乳吸收反应产生的 制备漂白粉
制备漂白粉
⑥加入铝粉能放出 的溶液中,
的溶液中, 、
、 、
、 、
、 一定能够大量共存
一定能够大量共存
⑦常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
⑧向 固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明
固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明 是两性氧化物
是两性氧化物
①常温常压下,17g甲基(
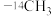 )所含的中子数为
)所含的中子数为
②1molBrCl与
 完全反应生成氯化氢和次溴酸,转移的电子的物质的量为1mol
完全反应生成氯化氢和次溴酸,转移的电子的物质的量为1mol③0℃,101kPa含有1mol硫原子的
 与
与 的混合物,其体积小于22.4L
的混合物,其体积小于22.4L④用
 检验
检验 的现象为产生大量白烟
的现象为产生大量白烟⑤可用石灰乳吸收反应产生的
 制备漂白粉
制备漂白粉⑥加入铝粉能放出
 的溶液中,
的溶液中, 、
、 、
、 、
、 一定能够大量共存
一定能够大量共存⑦常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
⑧向
 固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明
固体中滴加NaOH溶液或氢氟酸,固体均溶解,说明 是两性氧化物
是两性氧化物| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
6 . 海洋生物参与氮循环过程如图所示(其他含氮物质不参与反应)。下列说法错误的是
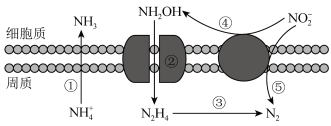
A.1 mol  与1 mol 与1 mol  所含电子数相等 所含电子数相等 |
B.反应③中,若 与 与 反应,则 反应,则 作还原剂 作还原剂 |
| C.以上六种含氮微粒,一共呈现了氮的四种价态 |
D.工业上用铵盐来处理含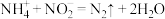 |
您最近一年使用:0次
名校
解题方法
7 . 恒温下,将16 mol  与24 mol
与24 mol  的混合气体通入一个固定容积的密闭容器中,发生如下反应:
的混合气体通入一个固定容积的密闭容器中,发生如下反应: 。回答下列问题:
。回答下列问题:
(1)合成氨反应中的能量变化如图所示,该反应中反应物化学键断裂吸收的总能量_______ (填“大于”或“小于”)生成物化学键形成放出的总能量。_______ (填选项字母)。
a. 的物质的量保持不变
的物质的量保持不变
b.三种气体的浓度相等
c.密闭容器内气体压强不再发生变化
d.反应后混合气体的密度不再发生变化
e.单位时间内消耗1 mol ,同时生成2 mol
,同时生成2 mol 
(3)①若反应进行到某时刻时,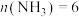 mol,此时
mol,此时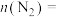
_______ mol;
②反应达到平衡时,混合气体的体积为716.8L(标准状况下), 和
和 的转化率之比
的转化率之比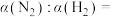
_______ ;原混合气体与平衡时混合气体的压强之比p(始)∶p(平)=_______ 。
(4)若改变下列一个条件,推测该反应的速率发生的变化。
①升温,化学反应速率_______ ;(填“加快”、“减慢”或“不变”,下同)
②恒温恒容下,充入一定量的稀有气体使容器中的压强增大,化学反应速率_______ 。
 与24 mol
与24 mol  的混合气体通入一个固定容积的密闭容器中,发生如下反应:
的混合气体通入一个固定容积的密闭容器中,发生如下反应: 。回答下列问题:
。回答下列问题:(1)合成氨反应中的能量变化如图所示,该反应中反应物化学键断裂吸收的总能量

a.
 的物质的量保持不变
的物质的量保持不变b.三种气体的浓度相等
c.密闭容器内气体压强不再发生变化
d.反应后混合气体的密度不再发生变化
e.单位时间内消耗1 mol
 ,同时生成2 mol
,同时生成2 mol 
(3)①若反应进行到某时刻时,
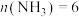 mol,此时
mol,此时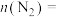
②反应达到平衡时,混合气体的体积为716.8L(标准状况下),
 和
和 的转化率之比
的转化率之比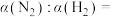
(4)若改变下列一个条件,推测该反应的速率发生的变化。
①升温,化学反应速率
②恒温恒容下,充入一定量的稀有气体使容器中的压强增大,化学反应速率
您最近一年使用:0次
名校
解题方法
8 . 氟是化学性质最为活泼的元素,氟可与除He、Ne和Ar外的所有元素形成化合物。几种氟化物的熔、沸点如下表所示,下列说法不正确的是
| 氟化物 | LiF |
|  |  |
| 熔点/℃ | 845 | a | -207 | c |
| 沸点/℃ | 1681 | b | -129 | d |
A.键角: | B.1 mol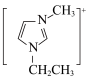 中共含有15 mol σ键 中共含有15 mol σ键 |
| C.a<845、b<1681、c>-207、d>-129 | D. 中含有配位键 中含有配位键 |
您最近一年使用:0次
名校
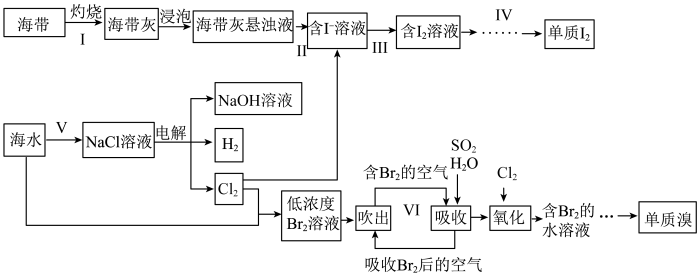
9 . 海洋是一座资源的宝库,下图是利用海洋资源生产卤素单质的工艺流程。
(1)实验室灼烧海带时使用的仪器有_______ 、泥三角、三脚架、酒精灯等,步骤Ⅱ的操作名称为_______ 。
(2)步骤Ⅲ中需要严格控制Cl2的用量,原因是_______ 。
(3)若步骤Ⅲ加H2O2的酸性溶液氧化I-,则其离子方程式为_______ 。
(4)步骤Ⅴ中,从海水提取的粗盐中主要含 、
、 、
、 等杂质离子,除去这些离子可加入的试剂有①盐酸②BaCl2溶液③Na2CO3溶液④NaOH溶液,加入试剂的正确顺序为
等杂质离子,除去这些离子可加入的试剂有①盐酸②BaCl2溶液③Na2CO3溶液④NaOH溶液,加入试剂的正确顺序为_______ (填标号)。
a.①②③④ b.②③④① c.③②④① d.②④③①
(5)步骤Ⅵ中,用SO2吸收Br2的离子方程式为_______ 。
(6)提取Br2的流程中,两次通入Cl2的目的是富集浓缩溴。若最终获得240gBr2,理论上需消耗标准状况下Cl2的体积为_______ 。

(1)实验室灼烧海带时使用的仪器有
(2)步骤Ⅲ中需要严格控制Cl2的用量,原因是
(3)若步骤Ⅲ加H2O2的酸性溶液氧化I-,则其离子方程式为
(4)步骤Ⅴ中,从海水提取的粗盐中主要含
 、
、 、
、 等杂质离子,除去这些离子可加入的试剂有①盐酸②BaCl2溶液③Na2CO3溶液④NaOH溶液,加入试剂的正确顺序为
等杂质离子,除去这些离子可加入的试剂有①盐酸②BaCl2溶液③Na2CO3溶液④NaOH溶液,加入试剂的正确顺序为a.①②③④ b.②③④① c.③②④① d.②④③①
(5)步骤Ⅵ中,用SO2吸收Br2的离子方程式为
(6)提取Br2的流程中,两次通入Cl2的目的是富集浓缩溴。若最终获得240gBr2,理论上需消耗标准状况下Cl2的体积为
您最近一年使用:0次
名校
解题方法
10 . 桂皮中的肉桂醛( )是一种食用香料,一种合成路线如图:
)是一种食用香料,一种合成路线如图:
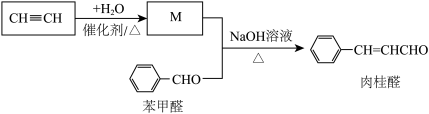
| A.与肉桂醛具有相同官能团的芳香化合物的同分异构体有4种 |
B.M能与新制 反应: 反应: |
| C.等物质的量的乙炔和M完全燃烧消耗氧气体积(标准状况)一致 |
| D.乙炔及肉桂醛都能发生加聚反应,且得到聚合物均不能导电 |
您最近一年使用:0次