1 . 回答下列问题:
(1)根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,计算在一定条件下,氮气与氧气反应生成1mol一氧化氮气体的过程中_______ (填“吸收”或“放出”)的能量为_______ kJ。 ,n(NO)随时间变化如下表:
,n(NO)随时间变化如下表:
①0~2s内,用O2表示该反应的反应速率为_______ mol·L-1·s-1。
②下列措施能够使该反应的反应速率加快的是_______ (填字母)。
a.降低温度 b.使用合适的催化剂 c.减小容器容积
(3)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成可循环使用的N2O5。_______ (填“石墨Ⅰ”或“石墨Ⅱ”)。
②若电路中有2mol电子转移,则理论上石墨Ⅱ处需消耗标准状况下的O2为_______ L。
在恒容密闭容器中,用H2还原SO2,生成S的反应分两步完成(如图甲所示),该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:_______ (填化学式)。
(5)0~t1时间段的温度为_______ 。
(1)根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,计算在一定条件下,氮气与氧气反应生成1mol一氧化氮气体的过程中

 ,n(NO)随时间变化如下表:
,n(NO)随时间变化如下表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
②下列措施能够使该反应的反应速率加快的是
a.降低温度 b.使用合适的催化剂 c.减小容器容积
(3)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成可循环使用的N2O5。

②若电路中有2mol电子转移,则理论上石墨Ⅱ处需消耗标准状况下的O2为
在恒容密闭容器中,用H2还原SO2,生成S的反应分两步完成(如图甲所示),该过程中相关物质的物质的量浓度随时间的变化关系如图乙所示,请分析并回答如下问题:
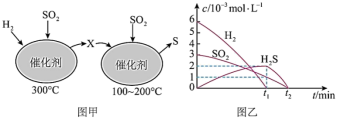
(5)0~t1时间段的温度为
您最近一年使用:0次
名校
2 . 下列生产或实验事实引出的相应结论正确的是
| 选项 | 事实 | 结论 |
| A | 在容积可变的密闭容器中发生反应:2NH3(g) N2H4 (g)+H2 (g),把容器体积缩小一半 N2H4 (g)+H2 (g),把容器体积缩小一半 | 正反应速率加快,逆反应速率也加快 |
| B | 将少量Na2S2O3样品溶于水,滴入过量的稀硝酸后,再滴入BaCl2溶液,有白色沉淀产生 | 说明Na2S2O3已变质 |
| C | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 与氨溶液中无铵根离子 |
| D | 向鸡蛋清溶液中滴加饱和硫酸铵溶液,振荡,有固体析出 | 硫酸铵溶液能使蛋白质变性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.现有乙烯、丙烯、丁烯的混合气体共14g,其原子数一定为3NA |
| B.标准状况下,11.2L己烷所含的分子数为0.5NA |
| C.含2mol H2SO4的浓硫酸与足量的铜在加热条件下反应,生成SO2的体积在标准状况下为22.4L |
| D.3mol NO2溶于水,转移的电子数为NA |
您最近一年使用:0次
4 . N、S元素化合物知识在高中化学体系中占有重要地位,请根据题意回答下列问题。
(1)工业制硝酸中NH3的催化氧化化学方程式_______ 。
(2)检验溶液中含有NH4+的离子方程式_______ ,实验室一般使用_______ 检验该反应有氨气生成。
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有_______ 和_______ 。(填浓硫酸的性质)
(4)铜与浓硫酸的化学反应方程式为_______ 。
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因_______ 。
(1)工业制硝酸中NH3的催化氧化化学方程式
(2)检验溶液中含有NH4+的离子方程式
(3)向蔗糖中滴加浓硫酸,蔗糖变黑并膨胀,散发刺激性气味,说明浓硫酸具有
(4)铜与浓硫酸的化学反应方程式为
(5)请用方程式解释实验室盛放碱液的试剂瓶不用玻璃塞的原因
您最近一年使用:0次
名校
解题方法
5 . 含有下列各组离子或分子的溶液中,通入过量SO2气体后能大量共存的是
A.H+、Ca2+、Fe3+、 |
| B.Ba2+、Cl-、Al3+、H+ |
C.Na+、 、I-、HS- 、I-、HS- |
| D.Na+、NH3·H2O、K+、Cl- |
您最近一年使用:0次
名校
解题方法
6 . 下列反应的离子方程式正确的是
A.过量铁粉与稀硝酸反应,产生无色气体:Fe+4H++ =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
B.向硫化钠溶液通入足量二氧化硫:S2-+2SO2+2H2O=H2S+2 |
| C.用Ca(ClO)2溶液吸收SO2:Ca2++2ClO-+SO2+H2O = 2HClO+CaSO3↓ |
D.用稀硝酸除去试管内壁银镜:3Ag+4H++ =3Ag++NO↑+2H2O =3Ag++NO↑+2H2O |
您最近一年使用:0次
名校
7 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐,利用离子液体[EMIM]可电沉积还原金属Ge,其中 的结构如图所示。下列说法错误的是
的结构如图所示。下列说法错误的是
 的结构如图所示。下列说法错误的是
的结构如图所示。下列说法错误的是
| A.该离子液体能导电 |
B.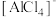 的空间构型为正四面体形 的空间构型为正四面体形 |
| C.离子晶体的熔点都很高 |
| D.电解沉积金属时,金属在阴极析出 |
您最近一年使用:0次
名校
解题方法
8 . 下列现象不能用氢键解释的是
A.可燃冰( )中甲烷分子与水分子间形成了氢键,所以可燃冰能稳定存在 )中甲烷分子与水分子间形成了氢键,所以可燃冰能稳定存在 |
| B.氨易液化,用作制冷剂 |
| C.氢键使蛋白质成为具有生物活性的高级结构 |
D.分子间氢键使得接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出来的相对分子质量大一些 计算出来的相对分子质量大一些 |
您最近一年使用:0次
名校
解题方法
9 . 下列分离或提纯有机物的方法错误的是
| 选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
| A | 乙醇 | 水 | 加氧化钙固体,蒸馏 |
| B | 苯甲酸 | NaCl | 水,重结晶 |
| C | 乙烷 | 乙烯 | 通入一定量的氢气 |
| D | 苯 | 溴苯 | 蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 .  与ICl的反应分两步完成,其能量曲线如图所示。下列说法错误的是
与ICl的反应分两步完成,其能量曲线如图所示。下列说法错误的是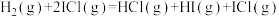
反应②: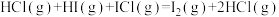
 与ICl的反应分两步完成,其能量曲线如图所示。下列说法错误的是
与ICl的反应分两步完成,其能量曲线如图所示。下列说法错误的是
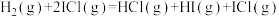
反应②:
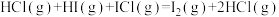
| A.反应①、②均是反应物总能量高于生成物总能量 |
| B.使用催化剂可以改变反应历程,从而改变总反应的反应热 |
C. 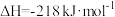 |
| D.基元反应①为该反应的决速步骤 |
您最近一年使用:0次



