名校
解题方法
1 . 化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去)。___________ 种, 所涉及的操作方法中,包含过滤的是
所涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)根据上述流程图,将化学方程式补充完整:__________ 。

(3)煅烧 固体的化学方程式是
固体的化学方程式是___________ 。
(4)下列联合制碱法流程说法正确的是___________ (填字母)。
a.两种气体的先后顺序为先通入 ,再通入
,再通入
b. 可以循环使用
可以循环使用
c.副产物 可用作肥料
可用作肥料
d.溶液B中一定含有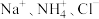
e.①中 析出是因为一定条件下
析出是因为一定条件下 的溶解度最小
的溶解度最小
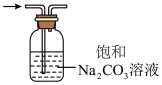
(5)某小组利用下列装置对 和
和 的性质进行探究,(气密性已检验)。
的性质进行探究,(气密性已检验)。 溶液,请将该洗气装置补充完整
溶液,请将该洗气装置补充完整___________ 。
②实验持续一段时间后,观察到饱和 溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因___________ 。
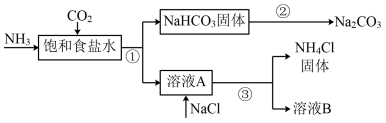
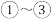 所涉及的操作方法中,包含过滤的是
所涉及的操作方法中,包含过滤的是(2)根据上述流程图,将化学方程式补充完整:

(3)煅烧
 固体的化学方程式是
固体的化学方程式是(4)下列联合制碱法流程说法正确的是
a.两种气体的先后顺序为先通入
 ,再通入
,再通入
b.
 可以循环使用
可以循环使用c.副产物
 可用作肥料
可用作肥料d.溶液B中一定含有
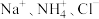
e.①中
 析出是因为一定条件下
析出是因为一定条件下 的溶解度最小
的溶解度最小(5)某小组利用下列装置对
 和
和 的性质进行探究,(气密性已检验)。
的性质进行探究,(气密性已检验)。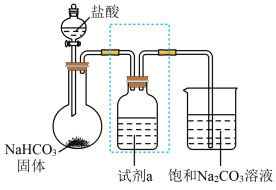
 溶液,请将该洗气装置补充完整
溶液,请将该洗气装置补充完整②实验持续一段时间后,观察到饱和
 溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
您最近一年使用:0次
名校
解题方法
2 . 1.下列实验装置能达到实验目的的是
| 选项 | A | B |
| 实验装置 |
|
|
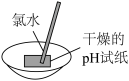
| 实验目的 | 测定氯水的pH | 铝热反应 |
| 选项 | C | D |
| 实验装置 |
|
|
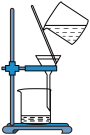
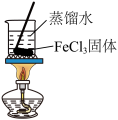
| 实验目的 | 除去粗盐溶液中的不溶物 | 制备氢氧化铁胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列实验操作正确的是
|
|
|
|
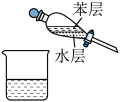
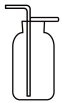
A.除去 | B.分离苯和水 | C.收集 | D.溶液滴加 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 十二烷基磺酸钠( )常用作轻纺工业的乳化剂。下列说法正确的是
)常用作轻纺工业的乳化剂。下列说法正确的是
 )常用作轻纺工业的乳化剂。下列说法正确的是
)常用作轻纺工业的乳化剂。下列说法正确的是| A.非金属性:C>H | B.离子半径: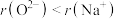 |
C.电离能: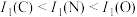 | D.热稳定性: |
您最近一年使用:0次
名校
5 . 设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.22.4L 中含有C﹣H的数目为 中含有C﹣H的数目为 |
B.1mol 中σ键的个数为 中σ键的个数为 |
C.0.1mol/LNaCl的溶液中 数为 数为 |
D.16g 所含有的电子数为 所含有的电子数为 |
您最近一年使用:0次
6 . 氢燃料电池汽车是未来汽车发展的重要方向之一。二甲醚重整制氢技术是一种理想制氢方案。
(1)1mol二甲醚CH3OCH3(g)与水蒸气发生可逆反应,生成CO2(g)和H2(g)的化学方程式为________________ 。
(2)根据下列两个热化学方程式,计算上述反应的反应热∆H=__________ kJ·mol-1。
反应I:CH3OCH3(g)+H2O(g)⇌2CH3OH(g) ∆H1=+37 kJ·mol-1
反应Ⅱ:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ∆H2=+49 kJ·mol-1
升高温度,反应速率_______ (填“变大”、“变小”或“不变”);根据以上反应判断,可采取_____________ (合理措施)来提高二甲醚的转化率(写一条)。
(3)在一个恒压 (起始体积为3 L)的密闭容器中充入2 mol CH3OH(g)和1 mol H2O(g),仅研究反应Ⅱ。CH3OH的平衡含量随温度、压强的变化如图所示。_______ P2(填“>”、“<”);B、C两点平衡常数KB_______ KC(填“>”、“<”或“=”);A点体积变为______ L,此时平衡常数KA的计算表达式为____________ (列式即可)。
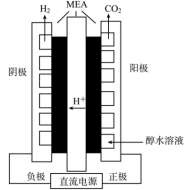
(4)我国科学家开发了一种运用质子交换膜的电解甲醇制氢装置(见图),甲醇的电解电压相对于水可降低近2/3,降低了制氢的能耗。写出阳极电极反应式______________ 。
(1)1mol二甲醚CH3OCH3(g)与水蒸气发生可逆反应,生成CO2(g)和H2(g)的化学方程式为
(2)根据下列两个热化学方程式,计算上述反应的反应热∆H=
反应I:CH3OCH3(g)+H2O(g)⇌2CH3OH(g) ∆H1=+37 kJ·mol-1
反应Ⅱ:CH3OH(g)+H2O(g)⇌CO2(g)+3H2(g) ∆H2=+49 kJ·mol-1
升高温度,反应速率
(3)在一个

(4)我国科学家开发了一种运用质子交换膜的电解甲醇制氢装置(见图),甲醇的电解电压相对于水可降低近2/3,降低了制氢的能耗。写出阳极电极反应式
您最近一年使用:0次
7 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,2.24L  含有的分子数为0.1 含有的分子数为0.1 |
B.2.8g由乙烯和丙烯组成的混合物中,所含的原子总数为0.6 |
C.0.3mol 2-甲基丁烷中含有的碳碳单键数为1.5 |
D.常温常压下,60g  中含有的分子数为 中含有的分子数为 |
您最近一年使用:0次
名校
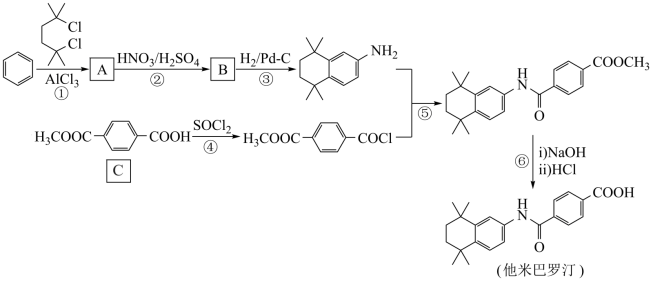
8 . 他米巴罗汀是一种对白血病、阿尔茨海默症等疾病具有较好治疗效果的药物,其一种合成路线:
(1)A的结构简式是___________ ,C中含氧官能团的名称是___________ 。
(2)①和③的反应类型分别是___________ ,___________ 。
(3)草酰氯(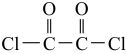 )与乙二胺(
)与乙二胺(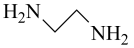 )反应可得到一种六元环状化合物,该反应的化学方程式为
)反应可得到一种六元环状化合物,该反应的化学方程式为___________ 。
(4)化合物W与C互为同分异构体,且满足下列条件:
①属于芳香族化合物且能与NaHCO3反应;
②能发生银镜反应;
③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应。
则W共有___________ 种,其中一种核磁共振氢谱为1:2:2:2:1,其结构简式为___________ 。
(5)参照上述合成路线,设计由苯和1,3-丁二烯合成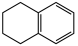 的路线(其它无机试剂任选)。
的路线(其它无机试剂任选)。___________
(1)A的结构简式是
(2)①和③的反应类型分别是
(3)草酰氯(
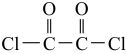 )与乙二胺(
)与乙二胺( )反应可得到一种六元环状化合物,该反应的化学方程式为
)反应可得到一种六元环状化合物,该反应的化学方程式为(4)化合物W与C互为同分异构体,且满足下列条件:
①属于芳香族化合物且能与NaHCO3反应;
②能发生银镜反应;
③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应。
则W共有
(5)参照上述合成路线,设计由苯和1,3-丁二烯合成
 的路线(其它无机试剂任选)。
的路线(其它无机试剂任选)。
您最近一年使用:0次
名校
解题方法
9 . 有机物的种类多,在日常生活中有重要的用途。请回答下列问题:_____ 。
(2)请用系统命名法命名有机物②_____ 。
(3)⑤与⑦发生共聚反应的化学方程式_____ 。
(4)属于非极性分子的是_____ (填序号)。
(5)⑥中基态氧原子的核外电子的空间运动状态有_____ 种。
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:_____ ,该过程形成的原子光谱为_____ (填“吸收”或“发射”)光谱。
①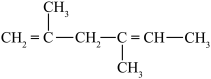 ;②
;②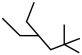 ;③
;③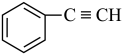 ;④
;④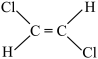 ;⑤
;⑤ ;⑥
;⑥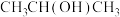 ;⑦
;⑦
(2)请用系统命名法命名有机物②
(3)⑤与⑦发生共聚反应的化学方程式
(4)属于非极性分子的是
(5)⑥中基态氧原子的核外电子的空间运动状态有
(6)硼在成键时能将一个2s电子激发进入2p能级参与形成化学键,请写出该激发态原子价电子轨道表示式:
您最近一年使用:0次
名校
10 . 锑(Sb)是银白色金属,广泛应用于电气、医药等领域。某科研小组从精炼铋烟尘(主要成分为 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: 、
、 、
、 。
。
② 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、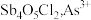 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。
③ “还原熔炼”的主要反应为 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。
回答下列问题:
(1)基态 的价电子排布式为
的价电子排布式为_______ 。
(2)“水解”步骤发生的反应为 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以_______  填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有_______ (任写一种)。
(3)“转化”步骤中 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(4)“还原熔炼”时碳的用量对锑回收率的影响如图 所示。碳用量超过
所示。碳用量超过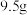 时,锑的回收率降低的原因可能是
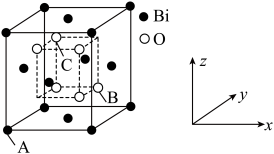
时,锑的回收率降低的原因可能是_______ 。 的立方晶胞结构如图所示
的立方晶胞结构如图所示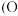 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为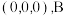 点坐标为
点坐标为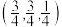 ,则
,则 点坐标为
点坐标为_______ 。晶胞边长为 ,则密度为
,则密度为_______ g cm-3(
cm-3( 的摩尔质量为
的摩尔质量为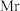 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
 、
、 、
、 等)中提炼金属锑的流程如图所示:
等)中提炼金属锑的流程如图所示: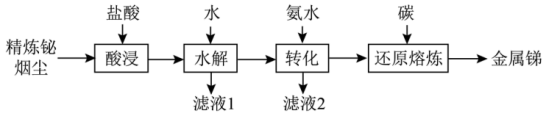
 、
、 、
、 。
。②
 易水解生成两种氯氧锑沉淀
易水解生成两种氯氧锑沉淀 、
、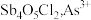 、
、 在上述情况下水解非常微弱。
在上述情况下水解非常微弱。③ “还原熔炼”的主要反应为
 ,熔炼过程中原料之间可能会形成泡渣而结块。
,熔炼过程中原料之间可能会形成泡渣而结块。回答下列问题:
(1)基态
 的价电子排布式为
的价电子排布式为(2)“水解”步骤发生的反应为
 、
、 ,加入少量水时,
,加入少量水时, 的水解产物以
的水解产物以 填化学式
填化学式 为主;促进
为主;促进 转化为
转化为 的措施有
的措施有(3)“转化”步骤中
 转化为
转化为 的化学方程式为
的化学方程式为(4)“还原熔炼”时碳的用量对锑回收率的影响如图
 所示。碳用量超过
所示。碳用量超过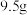 时,锑的回收率降低的原因可能是
时,锑的回收率降低的原因可能是
 的立方晶胞结构如图所示
的立方晶胞结构如图所示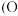 占据部分
占据部分 的四面体空隙
的四面体空隙 ,以
,以 点为原点建立分数坐标,已知
点为原点建立分数坐标,已知 点坐标为
点坐标为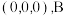 点坐标为
点坐标为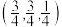 ,则
,则 点坐标为
点坐标为 ,则密度为
,则密度为 cm-3(
cm-3( 的摩尔质量为
的摩尔质量为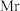 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
您最近一年使用:0次
7日内更新
|
86次组卷
|
2卷引用:广东省深圳市龙岗区龙城高级中学、深圳大学附属中学2023-2024学年高二下学期5月月考化学试题