名校
解题方法
1 . 2011年中国研制的第四代隐形战机歼-20在成都首次公开试飞成功。隐形战机的核心材料是金属钛,我国探明储量世界第一、下列有关22Ti的说法不正确的是
| A.钛的原子序数为22 |
| B.钛位于元素周期表第四周期第IVB族 |
| C.基态钛原子核外电子排布式为1s22s22p63s23p63d4 |
| D.钛是d区元素 |
您最近一年使用:0次
名校
2 . 用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应。下列有关叙述不正确的是
| A.①和②电子转移数之比为1∶3 | B.三种途径所消耗的铜的质量相等 |
| C.所消耗的硝酸的量:①>②>③ | D.对环境造成的危害,③最小 |
您最近一年使用:0次
3 . 某同学为研究浓硝酸与KSCN溶液的反应,进行如下实验:
资料: 能被氧化为
能被氧化为 ,
, 迅速聚合为红色的
迅速聚合为红色的 。
。
(1)KSCN中,C、N元素的化合价分别为+4价和-3价,则S元素的化合价为___________ 。
(2)Ⅰ中溶液立即变红是因为生成了___________ (填化学式)。
(3)研究 的最终转化产物。
的最终转化产物。
①取少量Ⅱ中试管内的溶液,___________ (填操作和现象),证明 中S元素的转化产物是
中S元素的转化产物是 。
。
②经检验Ⅱ中“红棕色气体”含有 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是___________ 。
③Ⅲ中, 转化为
转化为 、
、 ,离子方程式是
,离子方程式是___________ 。
④将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。
综合上述实验, 的最终转化产物中一定有
的最终转化产物中一定有___________ 。
| 实验操作 | 实验现象 |
Ⅰ.取1支试管,加入2mL浓硝酸,滴加5滴1 KSCN溶液 KSCN溶液 | 溶液立即变红 |
| Ⅱ.将试管静置一段时间 | 突然剧烈反应,红色迅速褪去,放出大量红棕色气体 |
Ⅲ.将Ⅱ中的气体通入 和NaOH的混合溶液中 和NaOH的混合溶液中 | 有白色沉淀生成 |
 能被氧化为
能被氧化为 ,
, 迅速聚合为红色的
迅速聚合为红色的 。
。(1)KSCN中,C、N元素的化合价分别为+4价和-3价,则S元素的化合价为
(2)Ⅰ中溶液立即变红是因为生成了
(3)研究
 的最终转化产物。
的最终转化产物。①取少量Ⅱ中试管内的溶液,
 中S元素的转化产物是
中S元素的转化产物是 。
。②经检验Ⅱ中“红棕色气体”含有
 ,但不能说明
,但不能说明 一定是
一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是③Ⅲ中,
 转化为
转化为 、
、 ,离子方程式是
,离子方程式是④将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。证明了红棕色气体中不含
溶液,不褪色。证明了红棕色气体中不含 。
。综合上述实验,
 的最终转化产物中一定有
的最终转化产物中一定有
您最近一年使用:0次
4 . 下列关于金属冶炼方法叙述不正确的是
A.在高温下C、CO、Al等还原剂可以将 还原为Fe 还原为Fe |
B.用电解熔融 的方法来冶炼铝 的方法来冶炼铝 |
| C.Hg和Ag都可以用加热分解它们氧化物的方法来冶炼 |
D.火法炼铜( )中,得到1mol Cu转移3mol电子 )中,得到1mol Cu转移3mol电子 |
您最近一年使用:0次
名校
5 . 关于 、
、 、
、 的完全燃烧,下列说法不正确的是
的完全燃烧,下列说法不正确的是
 、
、 、
、 的完全燃烧,下列说法不正确的是
的完全燃烧,下列说法不正确的是A.等物质的量完全燃烧时消耗 最多的是 最多的是 |
B.等质量完全燃烧时消耗 最多的是 最多的是 |
C.等质量完全燃烧生成 最多的是 最多的是 |
D.等质量完全燃烧生成 最多的是 最多的是 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.羊毛、蚕丝、塑料、橡胶都属于天然有机高分子材料 |
B.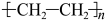 单体是 单体是 |
| C.乙烯分子中所有原子都在同一平面上 |
| D.乙烯和聚乙烯性质相似,均能使溴水和酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
7 . 下列说法正确的是
| A.光导纤维的主要成分是硅 |
| B.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液 |
| C.硅是人类将太阳能转换为电能的常用材料 |
| D.二氧化硅能与氢氟酸反应,则二氧化硅可以与盐酸反应 |
您最近一年使用:0次
8 . 下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 溶液中加入少量 固体,促进 固体,促进 分解 分解 |
B.密闭烧瓶内的 和 和 的混合气体,受热后颜色加深 的混合气体,受热后颜色加深 |
C.铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体 中,待不再变化后,加热能产生大量红棕色气体 |
| D.工业合成氨(放热反应),选择高温 |
您最近一年使用:0次
9 . 某同学为研究浓硝酸与KSCN溶液的反应,进行如下实验:
资料: 能被氧化为
能被氧化为 ,
, 迅速聚合为红色的
迅速聚合为红色的 。
。
(1)KSCN中, 的结构式是:
的结构式是: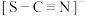 ,其中C元素的化合价为
,其中C元素的化合价为 价,则S元素的化合价为
价,则S元素的化合价为___________ 。
(2)Ⅰ中溶液立即变红是因为生成了___________ (填化学式)。
(3)研究 的最终转化产物。
的最终转化产物。
①取少量Ⅱ中试管内的溶液,___________ (填操作和现象),证明 中S元素的转化产物是
中S元素的转化产物是 。
。
②经检验Ⅱ中“红棕色气体”含有NO2,但不能说明NO2一定是 中N元素的转化产物,原因是
中N元素的转化产物,原因是___________ 。
③Ⅲ中,NO2转化为 、
、 ,离子方程式是
,离子方程式是___________ 。
④将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。
综合上述实验, 的最终转化产物中一定有
的最终转化产物中一定有___________ 。
(4)Ⅱ中,“静置一段时间后,突然剧烈反应”的可能原因是___________ (写出一条即可)。
| 实验操作 | 实验现象 |
Ⅰ.取1支试管,加入2mL浓硝酸,滴加5滴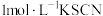 溶液 溶液 | 溶液立即变红 |
| Ⅱ.将试管静置一段时间 | 突然剧烈反应,红色迅速褪去,放出大量红棕色气体 |
Ⅲ.将Ⅱ中的气体通入 和NaOH的混合溶液中 和NaOH的混合溶液中 | 有白色沉淀生成 |
 能被氧化为
能被氧化为 ,
, 迅速聚合为红色的
迅速聚合为红色的 。
。(1)KSCN中,
 的结构式是:
的结构式是: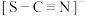 ,其中C元素的化合价为
,其中C元素的化合价为 价,则S元素的化合价为
价,则S元素的化合价为(2)Ⅰ中溶液立即变红是因为生成了
(3)研究
 的最终转化产物。
的最终转化产物。①取少量Ⅱ中试管内的溶液,
 中S元素的转化产物是
中S元素的转化产物是 。
。②经检验Ⅱ中“红棕色气体”含有NO2,但不能说明NO2一定是
 中N元素的转化产物,原因是
中N元素的转化产物,原因是③Ⅲ中,NO2转化为
 、
、 ,离子方程式是
,离子方程式是④将Ⅲ中沉淀过滤、洗涤,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量KMnO4溶液,不褪色。证明了红棕色气体中不含SO2。
综合上述实验,
 的最终转化产物中一定有
的最终转化产物中一定有(4)Ⅱ中,“静置一段时间后,突然剧烈反应”的可能原因是
您最近一年使用:0次
名校
解题方法
10 . 结合元素周期律,根据下列事实所得推测不合理 的是
| 事实 | 推测 | |
| A | Na、Al通常用电解法冶炼 | Mg可用电解法冶炼 |
| B | H3PO4是中强酸,H2SO4是强酸 | HClO4是强酸 |
| C | ⅣA族Si和Ge的单质是半导体材料 | 同族Pb的单质是半导体材料 |
| D | HI在230℃时分解,HCl在1500℃时分解 | HF分解温度大于1500℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



