名校
解题方法
1 . Ⅰ.某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,为b g
④从分液漏斗滴入 的稀硫酸,直到不再产生气体时为止
的稀硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明______ 。
(2)装置中干燥管B的作用是______ 。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果______ (填“偏高”“偏低”或“不变”)。
(4)步骤⑤的目的是______ 。
(5)步骤⑦的目的是______ 。
(6)该试样中纯碱的质量分数的计算式为______ (用含a、b、d的代数式表示)。
Ⅱ.现需要0.1mol/L的 溶液980mL,用98%、密度为
溶液980mL,用98%、密度为 的浓硫酸配制。
的浓硫酸配制。
(7)需要的玻璃仪器除了量筒、烧杯、玻璃棒外还需要______
(8)应用量取的浓硫酸体积为______ mL。
(9)试分析下列操作对所配溶液的浓度有何影响(填:偏高、偏低、无影响)
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会______ ;
②未冷却到室温就移液、定容______ 。
③移液前容量瓶中有水______ 。

主要实验步骤如下:
①按图组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量,为b g
④从分液漏斗滴入
 的稀硫酸,直到不再产生气体时为止
的稀硫酸,直到不再产生气体时为止⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量,为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
Ⅱ.现需要0.1mol/L的
 溶液980mL,用98%、密度为
溶液980mL,用98%、密度为 的浓硫酸配制。
的浓硫酸配制。(7)需要的玻璃仪器除了量筒、烧杯、玻璃棒外还需要
(8)应用量取的浓硫酸体积为
(9)试分析下列操作对所配溶液的浓度有何影响(填:偏高、偏低、无影响)
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会
②未冷却到室温就移液、定容
③移液前容量瓶中有水
您最近一年使用:0次
名校
2 . 下列物质用途或操作正确且与盐类水解有关的一组是
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用 水溶液制备
水溶液制备
③用氯化铁溶液和氨水制备氢氧化铁胶体
④实验室通常使用热的纯碱溶液去除油污
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制 溶液时将
溶液时将 晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火
①用热饱和硫酸铵溶液清洗铁器表面的铁锈
②用
 水溶液制备
水溶液制备
③用氯化铁溶液和氨水制备氢氧化铁胶体
④实验室通常使用热的纯碱溶液去除油污
⑤在氯化氢氛围中灼烧氯化镁晶体制备无水氯化镁
⑥配制
 溶液时将
溶液时将 晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度
晶体溶于浓硝酸中并加蒸馏水稀释至指定浓度⑦刻蚀印刷电路板用氯化铁作腐蚀液
⑧用泡沫灭火器灭火
| A.①②④⑤⑧ | B.③④⑤⑦⑧ | C.①②④⑤⑥ | D.②③④⑤⑥ |
您最近一年使用:0次
名校
3 . 根据下图回答下列问题
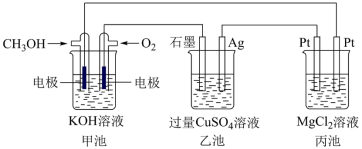
(1)图中甲池属于燃料电池,写出通入 一端的电极反应式为
一端的电极反应式为___________ 。从能量转换的角度分析比起直接燃烧燃料产生电能,使用燃料电池主要优点是___________ 。
(2)乙池发生反应的化学方程式为___________ ,反应一段时间后,向乙池中加入一定量___________ 固体,能使 溶液恢复到原浓度。
溶液恢复到原浓度。
(3)丙池左端Pt电极上产生的现象为___________ ,甲池中消耗448mL(标准状况下) ,此时丙池中理论上产生
,此时丙池中理论上产生___________ g固体。
(4)欲降低废水中重金属元素铬的毒性,可将 转化为
转化为 沉淀除去。在常温下,已知:
沉淀除去。在常温下,已知: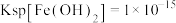 、
、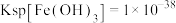 、
、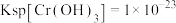 ,当离子浓度在
,当离子浓度在 以下时认为该离子已经完全沉淀,请回答:
以下时认为该离子已经完全沉淀,请回答:
①相同温度下 的溶解度
的溶解度___________  的溶解度(填“>”、“<”或“=”)
的溶解度(填“>”、“<”或“=”)
②浓度为0.1mol/L的 与10.0mol/L
与10.0mol/L 同时生成沉淀的pH范围是
同时生成沉淀的pH范围是___________ 。

(1)图中甲池属于燃料电池,写出通入
 一端的电极反应式为
一端的电极反应式为(2)乙池发生反应的化学方程式为
 溶液恢复到原浓度。
溶液恢复到原浓度。(3)丙池左端Pt电极上产生的现象为
 ,此时丙池中理论上产生
,此时丙池中理论上产生(4)欲降低废水中重金属元素铬的毒性,可将
 转化为
转化为 沉淀除去。在常温下,已知:
沉淀除去。在常温下,已知: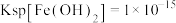 、
、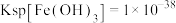 、
、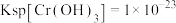 ,当离子浓度在
,当离子浓度在 以下时认为该离子已经完全沉淀,请回答:
以下时认为该离子已经完全沉淀,请回答:①相同温度下
 的溶解度
的溶解度 的溶解度(填“>”、“<”或“=”)
的溶解度(填“>”、“<”或“=”)②浓度为0.1mol/L的
 与10.0mol/L
与10.0mol/L 同时生成沉淀的pH范围是
同时生成沉淀的pH范围是
您最近一年使用:0次
解题方法
4 . 化合物X由4种元素组成。某兴趣小组按如图流程进行实验:

请回答:
(1)白色沉淀B的化学式为___________ ,B的物质的量为___________ 。
(2)根据C→D→E的现象,溶液C中溶质的成分一定有___________ (用化学式表示);
(3)根据溶液G后续的操作可知,溶液G中没有___________ 离子;经检测固体纯净物H为单质铁,则组成X的元素有____ 、____ 、____ 、____ ,X的化学式为________ 。
(4)设计实验确定溶液G中阴离子:用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明___________ ;取少量溶液G,加入足量 ,用盐酸酸化,再加入
,用盐酸酸化,再加入 溶液,若有白色沉淀,说明
溶液,若有白色沉淀,说明___________ 。
(5)X与足量 反应生成固体F的化学方程式是
反应生成固体F的化学方程式是___________ 。

请回答:
(1)白色沉淀B的化学式为
(2)根据C→D→E的现象,溶液C中溶质的成分一定有
(3)根据溶液G后续的操作可知,溶液G中没有
(4)设计实验确定溶液G中阴离子:用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明
 ,用盐酸酸化,再加入
,用盐酸酸化,再加入 溶液,若有白色沉淀,说明
溶液,若有白色沉淀,说明(5)X与足量
 反应生成固体F的化学方程式是
反应生成固体F的化学方程式是
您最近一年使用:0次
名校
5 . 在恒容密闭容器中采用下列反应合成甲醇: 。
。
(1)判断反应达到平衡状态的依据是___________。
(2)表中数据是反应在不同温度下的化学平衡常数(K)。
①由表中数据判断该反应的
___________ 0(填“>”、“=”或“<”);
②某温度下,将 和
和 充入1L的密闭容器中,充分反应后,达到平衡时测得
充入1L的密闭容器中,充分反应后,达到平衡时测得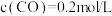 ,则
,则 的转化率为
的转化率为___________ ,此时的温度为___________  。
。
(3)要提高 的转化率,可以采取的措施是
的转化率,可以采取的措施是___________ 。
a.增加H2浓度 b.加入催化剂 c.增加CO的浓度 d.升温 e.加入惰性气体 f.降温
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示,在 、
、 时改变了一种条件,且不是浓度改变,则改变的条件为t2
时改变了一种条件,且不是浓度改变,则改变的条件为t2___________ ,
___________ 。

(5)一定条件下, 与
与 在催化剂的作用下生成
在催化剂的作用下生成 的能量变化为
的能量变化为 。在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
。在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是___________
 。
。(1)判断反应达到平衡状态的依据是___________。
A.生成 的速率与消耗 的速率与消耗 的速率相等 的速率相等 |
B. 、 、 、 、 的浓度都不再发生变化 的浓度都不再发生变化 |
| C.混合气体的相对平均分子质量不变 |
| D.混合气体的密度不变 |
(2)表中数据是反应在不同温度下的化学平衡常数(K)。
①由表中数据判断该反应的

| 温度 |  |  |  |
 | 2.041 | 0.270 | 0.012 |
 和
和 充入1L的密闭容器中,充分反应后,达到平衡时测得
充入1L的密闭容器中,充分反应后,达到平衡时测得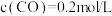 ,则
,则 的转化率为
的转化率为 。
。(3)要提高
 的转化率,可以采取的措施是
的转化率,可以采取的措施是a.增加H2浓度 b.加入催化剂 c.增加CO的浓度 d.升温 e.加入惰性气体 f.降温
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示,在
 、
、 时改变了一种条件,且不是浓度改变,则改变的条件为t2
时改变了一种条件,且不是浓度改变,则改变的条件为t2

(5)一定条件下,
 与
与 在催化剂的作用下生成
在催化剂的作用下生成 的能量变化为
的能量变化为 。在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
。在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO、2molH2 |  | 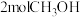 | |
| 平衡时 | CH3OH的浓度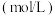 |  |  |  |
| 反应的能量变化 |  | 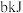 | 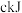 | |
体系压强 |  |  |  | |
| 反应物转化率 | 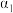 | 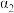 | 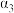 | |
A.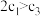 | B.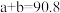 | C.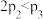 | D.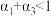 |
您最近一年使用:0次
名校
6 . 化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的种合成路线如下:
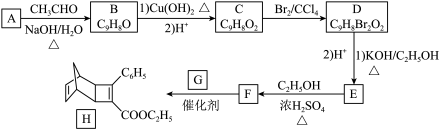
已知:①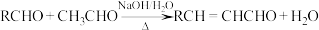 ②
②
(1)A物质的名称为
_______ 。
(2)B物质中官能团的名称为
_______ 。
(3)由C生成D和E生成F的反应类型分别为
_______ 、
_______ 。
(4)E的结构简式为
_______ 。
(5)G为甲苯的同分异构体由F生成H的化学方程式为
_______ 。
(6)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,满足上述条件的X有
_______ 种,写出其中任意一种符合要求的X的结构简式
_______ 。
(7)写出用环戊烷和2—丁炔为原料制备化合物
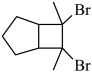 的合成路线(其他试剂任选):
的合成路线(其他试剂任选):
_______ 。

已知:①
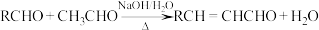 ②
②
(1)A物质的名称为
(2)B物质中官能团的名称为
(3)由C生成D和E生成F的反应类型分别为
(4)E的结构简式为
(5)G为甲苯的同分异构体由F生成H的化学方程式为
(6)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,满足上述条件的X有
(7)写出用环戊烷和2—丁炔为原料制备化合物
 的合成路线(其他试剂任选):
的合成路线(其他试剂任选):
您最近一年使用:0次
7 . 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是
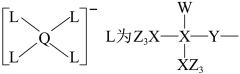
| A.W与X的化合物为极性分子 | B.第一电离能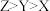 |
| C.Q的氧化物是两性氧化物 | D.该阴离子中含有配位键 |
您最近一年使用:0次
2023-06-13更新
|
11985次组卷
|
26卷引用:天津市第四十七中学2023-2024学年高三上学期期中考试化学试题
天津市第四十七中学2023-2024学年高三上学期期中考试化学试题2023年高考辽宁卷化学真题(已下线)T9-元素周期律及周期表(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第19讲元素周期律与元素周期表江西省九江市彭泽县第二高级中学2022-2023学年高一下学期7月期末化学试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)海南省海南中学2023-2024学年高三上学期第0次月考化学试题(已下线)第7讲 配合物与超分子黑龙江省哈尔滨市第九中学校2023-2024学年高三上学期开学考试化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省石家庄市第十七中学2023-2024高二上学期期末考试化学试题湖北省沙市中学2023-2024学年高三下学期3月月考化学试题2024届河北省实验中学高三年级上学期第一次月考化学试题安徽师范大学附属中学2023-2024学年高二下学期4月测试化学试题广东省广州市天河外国语学校2024届高三1月校考化学试题福建省宁化市第一中学2023-2024学年高三下学期3月质量检测化学试题(已下线)测试辽宁化学 请勿下载
8 . I.氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:_______ 。
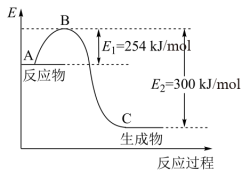
(2)若已知下列数据:
试根据表中及图中数据计算N-H的键能_______ kJ·mol-1。
(3)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1= nkJ·mol-1
N2(g)+O2(g)=2NO(g) △H2= mkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=_______ kJ/mol。(用含a、b的式子表示)。
II.氨的合成是最重要的化工生产之一。已知:N2+3H2⇌2NH3,在3个体积均为2L的密闭容器中,在相同的温度下,使用相同的催化剂合成氨,实验测得反应在起始、达到平衡时的有关数据如下表所示:
试回答:
(4)下列各项能说明该反应已达到平衡状态的是_______ (填写序号字母)。
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.3v(N2)正=v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(5)分析上表数据,下列关系正确的是_______(填写序号字母)。
(6)容器乙中反应从开始到达平衡平均速率为v(H2)=_______ mol/(L·min)。
III.直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液。
(7)负极电极反应式是_______ 。
(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:

(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
(3)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1= nkJ·mol-1
N2(g)+O2(g)=2NO(g) △H2= mkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=
II.氨的合成是最重要的化工生产之一。已知:N2+3H2⇌2NH3,在3个体积均为2L的密闭容器中,在相同的温度下,使用相同的催化剂合成氨,实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2molNH3 |
| 达平衡时间(min) | 5 | 8 | |
| N2浓度(mol/L) | C1 | 1.5 | |
| NH3的体积分数 | W1 | W3 | |
| 混合气体密度(g/L) | ρ1 | ρ2 |
(4)下列各项能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.3v(N2)正=v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(5)分析上表数据,下列关系正确的是_______(填写序号字母)。
| A.2c1<1.5mol·L-1 | B.2ρ1=ρ2 | C.w3=w1 | D.K甲= K乙= K丙 |
III.直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液。
(7)负极电极反应式是
您最近一年使用:0次
2023-02-01更新
|
382次组卷
|
2卷引用:天津市第四十七中学2022-2023学年高二上学期期末检测化学试题
9 . 亚硝酰硫酸(NOSO4H)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品中杂质硝酸的含量。
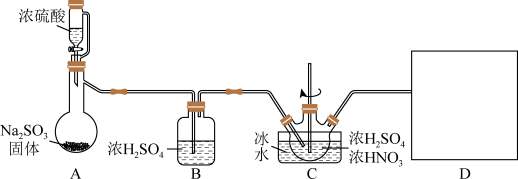
回答下列问题:
(1)装置A中盛装Na2SO3固体的仪器名称是_______ ,装置D最好选用_______ (填序号)。
a. b.
b.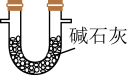 c.
c.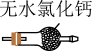 d.
d.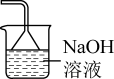
(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①C中“冷水”的温度一般控制在20℃,装置C中温度过高产率降低的原因是_______ 。
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是_______ 。
③请写出亚硝酰硫酸(NOSO4H)与水分解时发生的化学方程式_______ (已知亚硝酸不稳定,易分解,亚硝酸发生分解反应的方程式为2HNO2=NO2↑+NO↑+H2O)。
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400 g产品放入250mL锥形瓶中,加80mL浓硫酸,用0.1000mol/L (NH4)2Fe(SO4)2标准溶液滴定,消耗标准溶液20.00mL。
已知:(NH4)2Fe(SO4)2可与NO生成粉红色的FeSO4·NO。
①滴定过程中锥形瓶内发生的离子方程式为_______ 。
②锥形瓶中加入浓硫酸除了可以作溶剂外,另一个作用是_______ 。
③下列操作造成测定结果偏高的是_______ (填字母)。
A.滴定终点滴定管读数时俯视读数
B.用容量瓶配制(NH4)2Fe(SO4)2标准溶液时俯视
C.酸式滴定管用蒸馏水洗净后,未用标准液润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
④判断滴定达到终点的现象是_______ 。
⑤亚硝酰硫酸中硝酸的含量为_______ 。

回答下列问题:
(1)装置A中盛装Na2SO3固体的仪器名称是
a.
 b.
b. c.
c. d.
d.
(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①C中“冷水”的温度一般控制在20℃,装置C中温度过高产率降低的原因是
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
③请写出亚硝酰硫酸(NOSO4H)与水分解时发生的化学方程式
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400 g产品放入250mL锥形瓶中,加80mL浓硫酸,用0.1000mol/L (NH4)2Fe(SO4)2标准溶液滴定,消耗标准溶液20.00mL。
已知:(NH4)2Fe(SO4)2可与NO生成粉红色的FeSO4·NO。
①滴定过程中锥形瓶内发生的离子方程式为
②锥形瓶中加入浓硫酸除了可以作溶剂外,另一个作用是
③下列操作造成测定结果偏高的是
A.滴定终点滴定管读数时俯视读数
B.用容量瓶配制(NH4)2Fe(SO4)2标准溶液时俯视
C.酸式滴定管用蒸馏水洗净后,未用标准液润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
④判断滴定达到终点的现象是
⑤亚硝酰硫酸中硝酸的含量为
您最近一年使用:0次
2023-01-11更新
|
348次组卷
|
3卷引用:天津市第四十七中学2022—2023学年高三上学期期末 阶段性学习检测化学试题
名校
解题方法
10 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
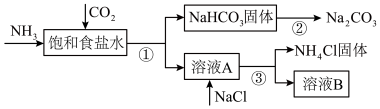
(1)饱和食盐水中通二氧化碳和氨气的化学方程式是_______
(2)下列说法中合理的是_______(填标号)。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是日常生活常用的消毒剂,二氧化氯 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。
①某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是_______ (填序号)
②某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
_______  (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
③ 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式_______ ,将 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式_______ 。

(1)饱和食盐水中通二氧化碳和氨气的化学方程式是
(2)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是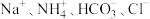 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。①某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色裉去;b.有大量气泡产生 |
| 2 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为③
 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
492次组卷
|
3卷引用:天津市第四十七中学2023-2024学年高三上学期第一次阶段性检测化学试题



