名校
1 . 硫酸亚铁是重要的化工原料
Ⅰ.
(1)由 溶液制备硫酸亚铁晶体的方法是
溶液制备硫酸亚铁晶体的方法是___________ 。检验晶体中 是否完全变质,将晶体溶于水,加
是否完全变质,将晶体溶于水,加___________ (填试剂)。
(2) 溶液与过量的
溶液与过量的 溶液混合,可以得到含
溶液混合,可以得到含 的浊液,离子方程式是
的浊液,离子方程式是___________ 。
Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以 为原料制备FeOOH的流程如下:
为原料制备FeOOH的流程如下:
(3)若在实验室完成上述制备,不需要使用的仪器是___________ 。 时段,pH快速下降的原因是反应生成了FeOOH和
时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
② 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是___________ 。
(5)判断流程中产品洗涤干净的方法是___________ 。
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。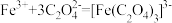 ,
,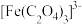 不与稀碱液反应。
不与稀碱液反应。
①在溶液c中滴加NaOH标准溶液,使用的指示剂为___________ 。
②若实验时加入了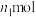 的
的 ,消耗
,消耗 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为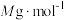 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为___________ (用含w、 、
、 、M的代数式表示)。
、M的代数式表示)。
③测定时,若滴入 不足量,会使实验结果
不足量,会使实验结果___________ (选填“偏大”“偏小”或“无影响”)。
Ⅰ.
(1)由
 溶液制备硫酸亚铁晶体的方法是
溶液制备硫酸亚铁晶体的方法是 是否完全变质,将晶体溶于水,加
是否完全变质,将晶体溶于水,加(2)
 溶液与过量的
溶液与过量的 溶液混合,可以得到含
溶液混合,可以得到含 的浊液,离子方程式是
的浊液,离子方程式是Ⅱ.氧化铁黄(FeOOH)是一种黄色颜料,具有非常好的耐光性和耐碱性,是氧化铁的一水合物。以
 为原料制备FeOOH的流程如下:
为原料制备FeOOH的流程如下: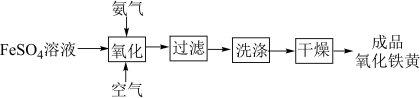
(3)若在实验室完成上述制备,不需要使用的仪器是
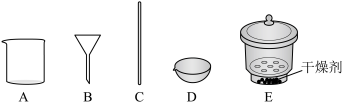
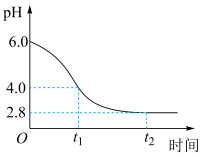
 时段,pH快速下降的原因是反应生成了FeOOH和
时段,pH快速下降的原因是反应生成了FeOOH和 ,该反应的化学方程式为
,该反应的化学方程式为②
 时段,经历的反应为
时段,经历的反应为 ,该过程pH继续平缓下降的原因可能是
,该过程pH继续平缓下降的原因可能是(5)判断流程中产品洗涤干净的方法是
(6)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。
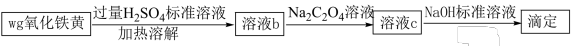
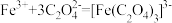 ,
,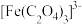 不与稀碱液反应。
不与稀碱液反应。①在溶液c中滴加NaOH标准溶液,使用的指示剂为
②若实验时加入了
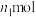 的
的 ,消耗
,消耗 ,设氧化铁黄的摩尔质量为
,设氧化铁黄的摩尔质量为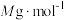 ,则氧化铁黄样品纯度为
,则氧化铁黄样品纯度为 、
、 、M的代数式表示)。
、M的代数式表示)。③测定时,若滴入
 不足量,会使实验结果
不足量,会使实验结果
您最近一年使用:0次
名校
解题方法
2 . 铁元素在人体健康和新材料研发中有重要的应用。
I.在血液中,以 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 。图为载氧后的血红蛋白分子示意图。
。图为载氧后的血红蛋白分子示意图。___________ 。
(2)载氧时,血红蛋白分子中 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是___________ (填字母)。
a. b.
b. c.CO
c.CO
(3)一种最简单的卟啉环结构如图。___________ 。
②比较C和N的电负性大小,并从原子结构角度说明理由:___________ 。
③该卟啉分子在酸性环境中配位能力会减弱,原因是___________ 。
Ⅱ. 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为apm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为apm。 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 。
。
(4)该晶体的密度是___________  。
。
(5)距离F最近的Cs的个数为___________ 。
Ⅲ.磷酸铁锂-石墨电池的总反应: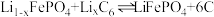 (
(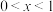 )。
)。
(6)放电时负极的电极反应式是___________ 。
I.在血液中,以
 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 。图为载氧后的血红蛋白分子示意图。
。图为载氧后的血红蛋白分子示意图。
(2)载氧时,血红蛋白分子中
 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是a.
 b.
b. c.CO
c.CO(3)一种最简单的卟啉环结构如图。
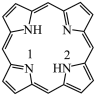
②比较C和N的电负性大小,并从原子结构角度说明理由:
③该卟啉分子在酸性环境中配位能力会减弱,原因是
Ⅱ.
 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为apm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为apm。
 ,阿伏伽德罗常数的值为
,阿伏伽德罗常数的值为 。
。(4)该晶体的密度是
 。
。(5)距离F最近的Cs的个数为
Ⅲ.磷酸铁锂-石墨电池的总反应:
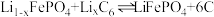 (
(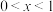 )。
)。(6)放电时负极的电极反应式是
您最近一年使用:0次
名校
3 . L是一种治疗自主神经功能障碍药物的活性成分,以A为原料合成L的流程如图所示。
(1)下列说法正确的是___________。
(2)E的结构简式为___________ 。
(3)H→I第一步反应的化学方程式为___________ 。
(4)设计F→G,H→I步骤的目的是___________ 。
(5)G→H中 可以用吡啶(
可以用吡啶(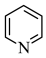 )替代,吡啶的作用是
)替代,吡啶的作用是___________ 。
(6)在E的芳香族同分异构体中,同时具备下列条件的结构有___________ 种。
①既能发生水解反应,又能发生银镜反应;
②1mol有机物最多能与3molNaOH反应;
③1mol有机物与足量的Na反应能生成 (标准状况)。
(标准状况)。
(7)设计以苯乙醛为原料制备吸湿性高分子材料(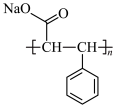 )的合成路线
)的合成路线___________ (无机试剂任选)。

(1)下列说法正确的是___________。
| A.A的名称是3-甲基苯酚 | B.B、C中均无手性碳原子 |
| C.H中官能团有酯基、醚键 | D.J→L为取代反应 |
(2)E的结构简式为
(3)H→I第一步反应的化学方程式为
(4)设计F→G,H→I步骤的目的是
(5)G→H中
 可以用吡啶(
可以用吡啶( )替代,吡啶的作用是
)替代,吡啶的作用是(6)在E的芳香族同分异构体中,同时具备下列条件的结构有
①既能发生水解反应,又能发生银镜反应;
②1mol有机物最多能与3molNaOH反应;
③1mol有机物与足量的Na反应能生成
 (标准状况)。
(标准状况)。(7)设计以苯乙醛为原料制备吸湿性高分子材料(
 )的合成路线
)的合成路线
您最近一年使用:0次
2024-06-10更新
|
379次组卷
|
4卷引用:2024届天津市天津市河西区天津市第四中学模拟预测化学试题
名校
4 . 某小组同学利用如下实验探究平衡移动原理。
ⅰ.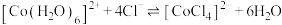 。
。
ⅱ. 溶液为无色。
溶液为无色。
下列说法正确的是
实验1: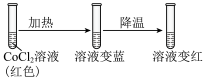
实验2: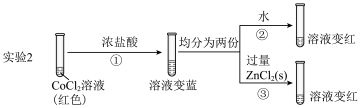
ⅰ.
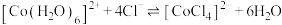 。
。ⅱ.
 溶液为无色。
溶液为无色。下列说法正确的是
| A.结合实验1和2,推测ⅰ中反应是放热反应 |
B.①中滴加浓盐酸,增大了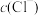 ,导致Q>K,ⅰ中平衡正向移动 ,导致Q>K,ⅰ中平衡正向移动 |
C.②中加水,溶液变红,说明平衡逆向移动, 的浓度增大 的浓度增大 |
D.③中加入 ,溶液变红,推测 ,溶液变红,推测 与 与 形成了配合物 形成了配合物 |
您最近一年使用:0次
2024-04-10更新
|
848次组卷
|
5卷引用:2024届天津市天津市河西区天津市第四中学模拟预测化学试题
名校
5 . 烟气脱硝技术是环境科学研究的热点。实验室模拟 将烟气中的
将烟气中的 深度氧化为
深度氧化为 ,并进一步将
,并进一步将 转化获得含氮产品,流程示意图如下。
转化获得含氮产品,流程示意图如下。
i.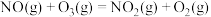
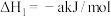
ii.

iii.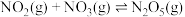

(1) 被
被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:


___________ 
(2)一定条件下,不同温度时, 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。
___________  (填“>”或“<”)。
(填“>”或“<”)。
②8s时, 的浓度不同的原因是
的浓度不同的原因是___________ 。
(3)一定条件下,NO的初始浓度为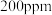 时,不同反应时间,深度氧化器中
时,不同反应时间,深度氧化器中 的浓度随
的浓度随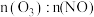 的变化如图所示。反应过程中
的变化如图所示。反应过程中 的浓度极低。
的浓度极低。 时,深度氧化器中发生的反应主要是
时,深度氧化器中发生的反应主要是___________ (填“i”“ii”或“iii”)。
② 时,
时, 的浓度随
的浓度随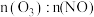 变化的原因是
变化的原因是___________ 。
(4) 且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是
且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是___________ 。
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。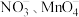 的还原产物分别是
的还原产物分别是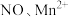 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为___________  。
。
 将烟气中的
将烟气中的 深度氧化为
深度氧化为 ,并进一步将
,并进一步将 转化获得含氮产品,流程示意图如下。
转化获得含氮产品,流程示意图如下。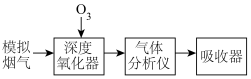
i.
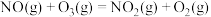
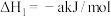
ii.


iii.
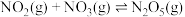

(1)
 被
被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:


(2)一定条件下,不同温度时,
 的浓度随时间的变化如图所示。
的浓度随时间的变化如图所示。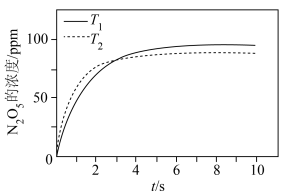

 (填“>”或“<”)。
(填“>”或“<”)。②8s时,
 的浓度不同的原因是
的浓度不同的原因是(3)一定条件下,NO的初始浓度为
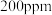 时,不同反应时间,深度氧化器中
时,不同反应时间,深度氧化器中 的浓度随
的浓度随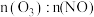 的变化如图所示。反应过程中
的变化如图所示。反应过程中 的浓度极低。
的浓度极低。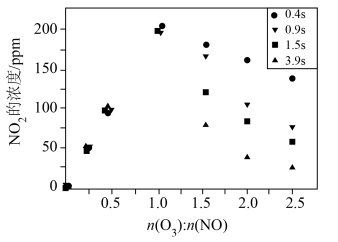
 时,深度氧化器中发生的反应主要是
时,深度氧化器中发生的反应主要是②
 时,
时, 的浓度随
的浓度随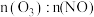 变化的原因是
变化的原因是(4)
 且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是
且恒压的条件下进行烟气处理,烟气达到排放标准所需深度氧化的时间仍较长。结合(3),保持上述条件不变,解决这一问题可采取的措施及目的分别是(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。
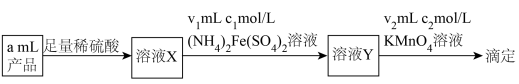
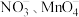 的还原产物分别是
的还原产物分别是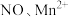 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
2024-04-10更新
|
645次组卷
|
4卷引用:2024届天津市天津市河西区天津市第四中学模拟预测化学试题
2024届天津市天津市河西区天津市第四中学模拟预测化学试题北京市西城区2024届高三统一测试(一模)化学试题(已下线)题型11 反应原理综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)提升练09 化学反应原理综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
6 .  和
和 在工农业。科研等方面应用广泛。按要求回答下列问题。
在工农业。科研等方面应用广泛。按要求回答下列问题。
(1)工业合成 时用到含铁催化剂。
时用到含铁催化剂。
①基态Fe原子的简化电子排布式为___________ 。
②我国科学家研发得Fe-LiH等双中心催化剂,在合成 中显示出高催化活性。Li、H元素的第一电离能(
中显示出高催化活性。Li、H元素的第一电离能( )较小的是
)较小的是___________ (填元素符号)。
(2) (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是___________ 。
② 的沸点高于
的沸点高于 的可能原因是
的可能原因是___________ 。
(3)在侯德榜制碱流程中两处用到 。
。
①其一先将 通入饱和食盐水,再通入
通入饱和食盐水,再通入 ,得到小苏打沉淀。写出该反应的离子方程式:
,得到小苏打沉淀。写出该反应的离子方程式:___________ 。
②其二为提高食盐利用率,向析出大量小苏打后的母液中加入NaCl细粉,通入 ,析出X晶体。
,析出X晶体。 参与此反应的离子方程式为
参与此反应的离子方程式为___________ ;X晶体中阳离子的空间结构为___________ 。
(4)Fe-Mg合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,H₂分子在晶胞的体心和棱的中心位置。___________ 个。
②要储存1 kg ,至少需要
,至少需要___________ kg Fe-Mg合金。
 和
和 在工农业。科研等方面应用广泛。按要求回答下列问题。
在工农业。科研等方面应用广泛。按要求回答下列问题。(1)工业合成
 时用到含铁催化剂。
时用到含铁催化剂。①基态Fe原子的简化电子排布式为
②我国科学家研发得Fe-LiH等双中心催化剂,在合成
 中显示出高催化活性。Li、H元素的第一电离能(
中显示出高催化活性。Li、H元素的第一电离能( )较小的是
)较小的是(2)
 (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②
 的沸点高于
的沸点高于 的可能原因是
的可能原因是(3)在侯德榜制碱流程中两处用到
 。
。①其一先将
 通入饱和食盐水,再通入
通入饱和食盐水,再通入 ,得到小苏打沉淀。写出该反应的离子方程式:
,得到小苏打沉淀。写出该反应的离子方程式:②其二为提高食盐利用率,向析出大量小苏打后的母液中加入NaCl细粉,通入
 ,析出X晶体。
,析出X晶体。 参与此反应的离子方程式为
参与此反应的离子方程式为(4)Fe-Mg合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,H₂分子在晶胞的体心和棱的中心位置。
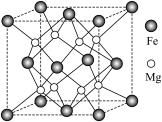
②要储存1 kg
 ,至少需要
,至少需要
您最近一年使用:0次
名校
7 . 高电压水系锌——有机混合液流电池的装置及其充放电原理示意图如下。
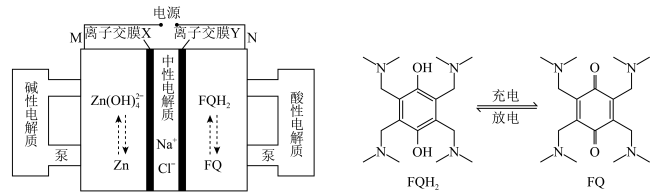
A.放电时,负极反应式: | B.放电时,1 mol FQ反应需转移4 mol  |
C.充电时, 可通过离子交换膜Y 可通过离子交换膜Y | D.充电时,M电极接电源负极 |
您最近一年使用:0次
2024-03-28更新
|
360次组卷
|
3卷引用:天津市河西区2023-2024学年高三下学期一模化学试题
8 . 氯及其化合物在生活生产中有着重要的应用。按要求回答下列问题。
Ⅰ.氯气的制备
(1)实验室中用 与浓盐酸反应制取并收集纯净的
与浓盐酸反应制取并收集纯净的 ,从下面装置中选出合理装置并连接组装,达成该实验目的的连接顺序为
,从下面装置中选出合理装置并连接组装,达成该实验目的的连接顺序为___________ 。
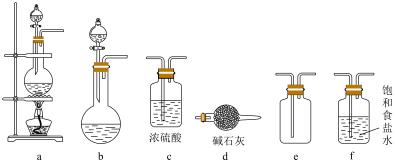
(2)忽略溶液中水蒸气的影响,在方框内画出上述实验中装置的可替代装置,并标注所需试剂的名称。______
(3)写出 在该替代装置中发生反应的离子方程式:
在该替代装置中发生反应的离子方程式:___________ 。
(4)工业上电解饱和食盐水方法制备 反应的离子方程式为
反应的离子方程式为___________ 。
Ⅱ.探究光照条件下氯水体系中粒子的变化
用强光照射盛有氯水的广口瓶,利用传感器采集到氯水的pH、 、广口瓶中
、广口瓶中 的体积分数随时间(t)变化的数据,如下图所示:
的体积分数随时间(t)变化的数据,如下图所示:
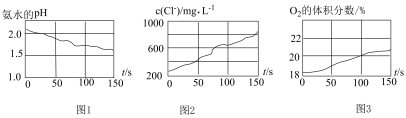
(5)由图1可得结论:___________ 。
(6)分析上述三个图示数据信息,用离子方程式表示得出的结论:___________ 、___________ 。
Ⅲ.探究“84”消毒液(主要成分NaClO)的使用方法
(7)“84”消毒液呈碱性的原因(用化学用语解释):___________ 。
(8)“84”消毒液不能与洁厕灵(含盐酸)混用,否则会产生气体为___________ 。
(9)“84”消毒液与消毒酒精混用会产生乙醛,写出反应的离子方程式___________ 。
Ⅰ.氯气的制备
(1)实验室中用
 与浓盐酸反应制取并收集纯净的
与浓盐酸反应制取并收集纯净的 ,从下面装置中选出合理装置并连接组装,达成该实验目的的连接顺序为
,从下面装置中选出合理装置并连接组装,达成该实验目的的连接顺序为
(2)忽略溶液中水蒸气的影响,在方框内画出上述实验中装置的可替代装置,并标注所需试剂的名称。
(3)写出
 在该替代装置中发生反应的离子方程式:
在该替代装置中发生反应的离子方程式:(4)工业上电解饱和食盐水方法制备
 反应的离子方程式为
反应的离子方程式为Ⅱ.探究光照条件下氯水体系中粒子的变化
用强光照射盛有氯水的广口瓶,利用传感器采集到氯水的pH、
 、广口瓶中
、广口瓶中 的体积分数随时间(t)变化的数据,如下图所示:
的体积分数随时间(t)变化的数据,如下图所示:
(5)由图1可得结论:
(6)分析上述三个图示数据信息,用离子方程式表示得出的结论:
Ⅲ.探究“84”消毒液(主要成分NaClO)的使用方法
(7)“84”消毒液呈碱性的原因(用化学用语解释):
(8)“84”消毒液不能与洁厕灵(含盐酸)混用,否则会产生气体为
(9)“84”消毒液与消毒酒精混用会产生乙醛,写出反应的离子方程式
您最近一年使用:0次
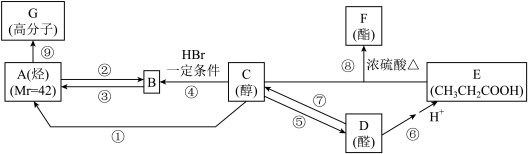
9 . 有机物A~G在一定条件下的转化关系如下图所示(部分条件已略):
(1)A是乙烯的同系物,A的电子式为_______ ;高分子G的结构简式为_______ 。
(2)C的名称为_______ 。反应①~⑧中属于取代反应的有_______ (填编号)。
(3)写出下列反应的化学方程式:
反应③:_______ ;
反应⑤:_______ 。
(4)D所含官能团的名称为_______ ,官能团中碳原子的杂化方式为_______ ;检验D中所含官能团的实验,可选用的试剂和仪器:2%氨水、 2%
2%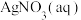 、热水:试管、烧杯。
、热水:试管、烧杯。
ⅰ.写出该实验D参与反应的化学方程式:_______ ;
ⅱ.补充该实验步骤:在洁净的试管中加入 2%
2%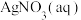 后边振荡边滴加2%氨水至
后边振荡边滴加2%氨水至_______ ,再向其中滴加几滴D,振荡后将试管放在热水中温热。
ⅲ.可观察到试管中的现象为_______ 。
(5)写出B的同分异构体的结构简式:_______ 。
(1)A是乙烯的同系物,A的电子式为
(2)C的名称为
(3)写出下列反应的化学方程式:
反应③:
反应⑤:
(4)D所含官能团的名称为
 2%
2%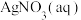 、热水:试管、烧杯。
、热水:试管、烧杯。ⅰ.写出该实验D参与反应的化学方程式:
ⅱ.补充该实验步骤:在洁净的试管中加入
 2%
2%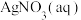 后边振荡边滴加2%氨水至
后边振荡边滴加2%氨水至ⅲ.可观察到试管中的现象为
(5)写出B的同分异构体的结构简式:
您最近一年使用:0次
名校
解题方法
10 . 除去废水中的含氮化合物一直是环保领域的热点问题。短程硝化-厌氧氨氧化工艺的目的是将氨氮( )废水中的氮元素转变为 N2脱除,其机理如下:
)废水中的氮元素转变为 N2脱除,其机理如下: 会被氧化成
会被氧化成 。
。
(1)该工艺中被氧化的微粒是___________ 。
(2)参与Ⅰ中反应的 n( ):n(O2) =
):n(O2) =_____ 。
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当 DO > 2mg/L 时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被抑制,II 中反应无法发生;还有可能是___________ 。 /
/ 采用微生物电解工艺也可有效除去
采用微生物电解工艺也可有效除去 /
/ ,其原理如下图所示。A 是电源
,其原理如下图所示。A 是电源___________ 极。结合电极反应式解释该工艺能提高氮的脱除率的原因:___________ 。________ 。
 )废水中的氮元素转变为 N2脱除,其机理如下:
)废水中的氮元素转变为 N2脱除,其机理如下:
 会被氧化成
会被氧化成 。
。(1)该工艺中被氧化的微粒是
(2)参与Ⅰ中反应的 n(
 ):n(O2) =
):n(O2) =(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当 DO > 2mg/L 时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被抑制,II 中反应无法发生;还有可能是

 /
/ 采用微生物电解工艺也可有效除去
采用微生物电解工艺也可有效除去 /
/ ,其原理如下图所示。A 是电源
,其原理如下图所示。A 是电源
您最近一年使用:0次



