解题方法
1 . 钙钛矿是指通式为 的一类化合物,钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等功能材料。
的一类化合物,钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等功能材料。
Ⅰ.最早发现的钙钛矿石中含 的立方晶胞如图1所示。
的立方晶胞如图1所示。
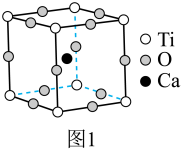
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ , 中组成元素的电负性大小顺序是
中组成元素的电负性大小顺序是___________ 。
(2)金属离子与氧离子之间的化学键为___________ 。
(3)晶胞中与 距离最近且相等的
距离最近且相等的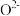 数目为
数目为___________ 。
Ⅱ.一种立方钙钛矿结构的金属卤化物光电材料的组成为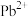 、
、 和有机碱离子
和有机碱离子 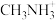 ,其晶胞如图2所示。
,其晶胞如图2所示。
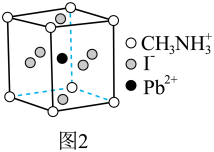
(4)图1中与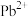 具有相同的空间位置的微粒是
具有相同的空间位置的微粒是
(5)有机碱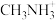 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是___________ 。
(6)若晶胞参数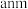 ,则晶体密度为
,则晶体密度为___________ 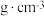 (用
(用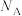 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕 盐,提升了太阳能电池的效率和使用寿命,其作用原理如图所示。
盐,提升了太阳能电池的效率和使用寿命,其作用原理如图所示。
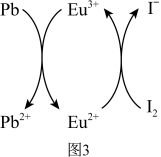
(7)用离子方程式表示该原理___________ 、___________ 。
 的一类化合物,钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等功能材料。
的一类化合物,钙钛矿型化合物可用于生产太阳能电池、传感器、固体电阻器等功能材料。Ⅰ.最早发现的钙钛矿石中含
 的立方晶胞如图1所示。
的立方晶胞如图1所示。
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 中组成元素的电负性大小顺序是
中组成元素的电负性大小顺序是(2)金属离子与氧离子之间的化学键为
(3)晶胞中与
 距离最近且相等的
距离最近且相等的 数目为
数目为Ⅱ.一种立方钙钛矿结构的金属卤化物光电材料的组成为
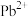 、
、 和有机碱离子
和有机碱离子 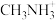 ,其晶胞如图2所示。
,其晶胞如图2所示。
(4)图1中与
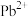 具有相同的空间位置的微粒是
具有相同的空间位置的微粒是A. | B.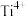 | C. | D.无 |
(5)有机碱
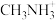 中,
中, 原子的杂化轨道类型是
原子的杂化轨道类型是(6)若晶胞参数
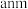 ,则晶体密度为
,则晶体密度为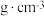 (用
(用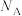 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕
 盐,提升了太阳能电池的效率和使用寿命,其作用原理如图所示。
盐,提升了太阳能电池的效率和使用寿命,其作用原理如图所示。
(7)用离子方程式表示该原理
您最近一年使用:0次
解题方法
2 . 含氯消毒剂在生产、生活中被广泛用于杀菌、消毒和漂白。常见的含氯消毒剂有84消毒液、漂白粉、二氯异氰尿酸钠、三氯异氰尿酸等。
(1)84消毒液的有效成分为___________ (填编号)。
A. B.
B. C.
C.
实验原理为:
二氯异氟尿酸钠为白色固体,难溶于冷水,是一种高效、安全的氧化性消毒剂。实验室可用如图所示装置制备(夹持装置已略去)。

(2)①仪器 中侧管的作用为
中侧管的作用为___________ 。
②装置A中的药品可以选择___________ 。(填编号)
A.浓硫酸 B. C.
C. D.漂白粉
D.漂白粉
(3)①实验后发现装置B中 溶液的利用率较低,改进的方法是
溶液的利用率较低,改进的方法是___________ 。
②当从装置B中观察到___________ 时,加入 的吡啶溶液。实验过程中B的温度必须保持在
的吡啶溶液。实验过程中B的温度必须保持在 控制在
控制在 ,则该实验的受热方式是
,则该实验的受热方式是___________ 。
③反应结束后,装置B中的悬浊液,经过滤、___________ 、干燥,得粗产品二氯异氰尿酸钠。
有效氯是二氯异氰尿酸钠产品质量的重要指标。通过下列步骤可检测二氯异氰尿酸钠样品的有效氯。
(a)准确称取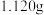 样品,用容量瓶配成
样品,用容量瓶配成 溶液;
溶液;
(b)取 上述溶液于碘量瓶中,加入适量稀硫酸和过量
上述溶液于碘量瓶中,加入适量稀硫酸和过量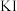 溶液,密封,在暗处静置
溶液,密封,在暗处静置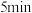 ;
;
(c)用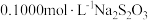 标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗 溶液的体积为
溶液的体积为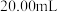 。
。
已知:
ⅰ.部分反应: 、
、
ⅱ.
(4)①步骤(1)中使用的容量瓶是否需要进行干燥___________ 。(填“是”或“否”)
②该样品的有效氯测定值
___________ 。(结果保留两位小数)
③滴定至溶液蓝色刚好褪去,振荡后又恢复,此时停止滴定可能会导致样品的有效氯测定值___________ 。(填“偏高”或“偏低”或“无影响”)
(1)84消毒液的有效成分为
A.
 B.
B. C.
C.
实验原理为:

二氯异氟尿酸钠为白色固体,难溶于冷水,是一种高效、安全的氧化性消毒剂。实验室可用如图所示装置制备(夹持装置已略去)。

(2)①仪器
 中侧管的作用为
中侧管的作用为②装置A中的药品可以选择
A.浓硫酸 B.
 C.
C. D.漂白粉
D.漂白粉(3)①实验后发现装置B中
 溶液的利用率较低,改进的方法是
溶液的利用率较低,改进的方法是②当从装置B中观察到
 的吡啶溶液。实验过程中B的温度必须保持在
的吡啶溶液。实验过程中B的温度必须保持在 控制在
控制在 ,则该实验的受热方式是
,则该实验的受热方式是③反应结束后,装置B中的悬浊液,经过滤、
有效氯是二氯异氰尿酸钠产品质量的重要指标。通过下列步骤可检测二氯异氰尿酸钠样品的有效氯。
(a)准确称取
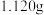 样品,用容量瓶配成
样品,用容量瓶配成 溶液;
溶液;(b)取
 上述溶液于碘量瓶中,加入适量稀硫酸和过量
上述溶液于碘量瓶中,加入适量稀硫酸和过量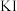 溶液,密封,在暗处静置
溶液,密封,在暗处静置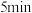 ;
;(c)用
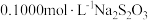 标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗
标准溶液滴定至溶液呈微黄色,加入淀粉,继续滴定至终点,平均消耗 溶液的体积为
溶液的体积为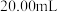 。
。已知:
ⅰ.部分反应:
 、
、
ⅱ.

(4)①步骤(1)中使用的容量瓶是否需要进行干燥
②该样品的有效氯测定值

③滴定至溶液蓝色刚好褪去,振荡后又恢复,此时停止滴定可能会导致样品的有效氯测定值
您最近一年使用:0次
3 . 四氧化三铁( )磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
(1) 能和稀硫酸反应,生成的两种盐是
能和稀硫酸反应,生成的两种盐是___________ 。验证反应后溶液中含有 的最恰当的试剂是
的最恰当的试剂是___________ 。
A.氯水 B.酸性 溶液 C.KSCN溶液 D.NaOH溶液
溶液 C.KSCN溶液 D.NaOH溶液
(2)铁粉在氧气中燃烧是制取 最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。
最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。___________ 。(从下图①、②、③中选择)
②在加入试剂之前,需对装置进行气密性检查。写出检查①的气密性的操作,___________ ,向分液漏斗中加足量水,塞紧玻璃塞,打开玻璃旋塞,过一会儿,水不再下滴,说明装置①的气密性良好。如果把分液漏斗改成恒压滴液漏斗,___________ (填“是”或“否”)可以用上述步骤检验装置的气密性?
③写出B装置中反应的化学方程式___________ 。
(3)氧化沉淀法也是制取 的一种常见方法,其制取流程如下图所示,
的一种常见方法,其制取流程如下图所示,___________ (填写化学式),由溶液N获得该副产品的操作是:加热浓缩→___________ →过滤洗涤→晶体加热至完全失去结晶水。
(4)某兴趣小组模仿上述流程制取 并测定其产率、具体操作如下:
并测定其产率、具体操作如下:
I.测定绿矾的含量:称取3.0g工业绿矾,配制成250.00mL溶液。量取25.00mL溶液于锥形瓶中,用0.01000 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为20.00mL。写出滴定时发生反应的离子方程式为
溶液的平均体积为20.00mL。写出滴定时发生反应的离子方程式为___________ 。
Ⅱ.称取300g工业绿矾,通过上述流程最终制得:50g 计算产品
计算产品 的产率为
的产率为___________ 。(保留4位有效数字)
 )磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。
)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。(1)
 能和稀硫酸反应,生成的两种盐是
能和稀硫酸反应,生成的两种盐是 的最恰当的试剂是
的最恰当的试剂是A.氯水 B.酸性
 溶液 C.KSCN溶液 D.NaOH溶液
溶液 C.KSCN溶液 D.NaOH溶液(2)铁粉在氧气中燃烧是制取
 最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。
最为快捷的方法。A~D是制取四氧化三铁的系列装置,A装置用于制取二氧化碳气体,并要求气流稳定,流速可控。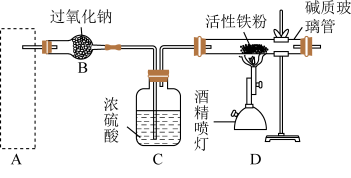
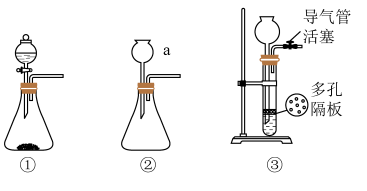
②在加入试剂之前,需对装置进行气密性检查。写出检查①的气密性的操作,
③写出B装置中反应的化学方程式
(3)氧化沉淀法也是制取
 的一种常见方法,其制取流程如下图所示,
的一种常见方法,其制取流程如下图所示,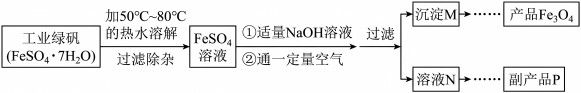
(4)某兴趣小组模仿上述流程制取
 并测定其产率、具体操作如下:
并测定其产率、具体操作如下:I.测定绿矾的含量:称取3.0g工业绿矾,配制成250.00mL溶液。量取25.00mL溶液于锥形瓶中,用0.01000
 酸性
酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的平均体积为20.00mL。写出滴定时发生反应的离子方程式为
溶液的平均体积为20.00mL。写出滴定时发生反应的离子方程式为Ⅱ.称取300g工业绿矾,通过上述流程最终制得:50g
 计算产品
计算产品 的产率为
的产率为
您最近一年使用:0次
4 . 基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。利用木质纤维素为起始原料结合 生产聚碳酸对二甲苯酚可以实现碳减排,路线如下,回答下列问题:
生产聚碳酸对二甲苯酚可以实现碳减排,路线如下,回答下列问题:___________ 。
(2)分析化合物Ⅱ的结构,预测反应后形成的新物质,参考①的示例,完成下表。
(3)化合物Ⅲ到化合物Ⅳ的反应是原子利用率100%的反应,且1mol Ⅲ与1mol化合物a反应得到1mol Ⅳ。则化合物a为___________ 。反应类型为___________ 。
(4)已知化合物Ⅴ的核磁共振氢谱有2组峰。且峰面积之比为2∶3,写出化合物Ⅴ的结构简式:___________ 。
(5)化合物Ⅶ的芳香族同分异构体中符合下列条件的有___________ 种(不含立体异构)。
①最多能与相同物质的量的 反应 ②能与2倍物质的量的Na发生放出
反应 ②能与2倍物质的量的Na发生放出 的反应
的反应
(6)关于Ⅶ生成Ⅷ的反应的说法中,不正确的有___________。
(7)结合上述信息,写出以丙烯为起始有机原料合成 的路线
的路线___________ (无机试剂任选)。
 生产聚碳酸对二甲苯酚可以实现碳减排,路线如下,回答下列问题:
生产聚碳酸对二甲苯酚可以实现碳减排,路线如下,回答下列问题:
(2)分析化合物Ⅱ的结构,预测反应后形成的新物质,参考①的示例,完成下表。
| 序号 | 变化的言能团的名称 | 可反应的试剂(物质) | 反应后形成的新物质 | 反应类型 |
| ① |  |
| 氧化反应 | |
| ② | 加成反应 |
(3)化合物Ⅲ到化合物Ⅳ的反应是原子利用率100%的反应,且1mol Ⅲ与1mol化合物a反应得到1mol Ⅳ。则化合物a为
(4)已知化合物Ⅴ的核磁共振氢谱有2组峰。且峰面积之比为2∶3,写出化合物Ⅴ的结构简式:
(5)化合物Ⅶ的芳香族同分异构体中符合下列条件的有
①最多能与相同物质的量的
 反应 ②能与2倍物质的量的Na发生放出
反应 ②能与2倍物质的量的Na发生放出 的反应
的反应(6)关于Ⅶ生成Ⅷ的反应的说法中,不正确的有___________。
| A.反应过程中,有H-O键断裂 | B.反应过程中,有C=O双键和C-O单键形成 |
| C.该反应为缩聚反应 | D. 属于极性分子,分子中存在 属于极性分子,分子中存在 键 键 |
(7)结合上述信息,写出以丙烯为起始有机原料合成
 的路线
的路线
您最近一年使用:0次
解题方法
5 . 常温下,二元弱酸 在溶液中各组分百分含量
在溶液中各组分百分含量 随溶液pH的变化如图所示。下列说法错误的是
随溶液pH的变化如图所示。下列说法错误的是
 在溶液中各组分百分含量
在溶液中各组分百分含量 随溶液pH的变化如图所示。下列说法错误的是
随溶液pH的变化如图所示。下列说法错误的是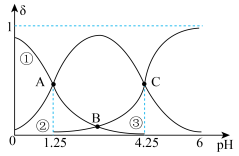
A.曲线②表示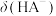 随溶液pH的变化 随溶液pH的变化 |
B. 的一级电离常数 的一级电离常数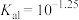 |
C.NaHA溶液中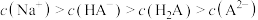 |
D.常温下,若向 溶液中滴加 溶液中滴加 溶液使溶液pH=7,则一定存在: 溶液使溶液pH=7,则一定存在: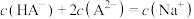 |
您最近一年使用:0次
2024-02-25更新
|
728次组卷
|
7卷引用:天津市红桥区2024届高三下学期二模化学试题
天津市红桥区2024届高三下学期二模化学试题2024届陕西省安康市高三下学期一模考试理科综合试题-高中化学甘肃省白银市名校2023-2024学年高三下学期联合调研化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)甘肃省天水市麦积区2024届高三下学期2月第二次模拟检测化学试题2024届陕西省西安博爱国际学校高三下学期第一次模拟考试理科综合试卷-高中化学四川省成都市崇州市怀远中学2023-2024学年高三上学期期末理综试题-高中化学
6 . 为达到碳中和的目标,工业燃烧煤的废气要进行脱碳处理。
(1)向2L密闭容器中加入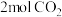 和
和 ,在适当的催化剂作用下,发生反应:
,在适当的催化剂作用下,发生反应: 。
。
①该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)。
②下列叙述能说明此反应达到平衡状态的是___________ (填字母)。
A.混合气体的平均相对分子质量保持不变
B. 和H2的体积分数保持不变
和H2的体积分数保持不变
C. 和H2的转化率相等
和H2的转化率相等
D.混合气体的密度保持不变
E.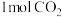 生成的同时有
生成的同时有 键断裂
键断裂
(2)改变温度,使反应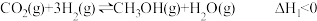 中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应I、II对比:平衡常数K(I)___________ K(II)(填“>”“<”或“=”,下同);平衡时 的浓度c(I)
的浓度c(I)___________ c(II)。
②对反应I,前10min内的平均反应速率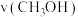 =
=_______ ;在其他条件不变的情况下,若30min时只改变温度至T2℃,此时 的物质的量为3.2mol,则T1
的物质的量为3.2mol,则T1_______ (填“>”<”或“=”)T2。若30min时只向容器中再充入 和
和 ,则平衡
,则平衡_______ (填“正向”“逆向”或“不”)移动。
(1)向2L密闭容器中加入
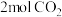 和
和 ,在适当的催化剂作用下,发生反应:
,在适当的催化剂作用下,发生反应: 。
。①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变
B.
 和H2的体积分数保持不变
和H2的体积分数保持不变C.
 和H2的转化率相等
和H2的转化率相等D.混合气体的密度保持不变
E.
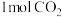 生成的同时有
生成的同时有 键断裂
键断裂(2)改变温度,使反应
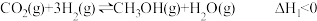 中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间(min) |  (mol) (mol) |  (mol) (mol) |  (mol) (mol) |  (mol) (mol) | |
| 反应I:恒温恒容 | 0 | 2 | 6 | 0 | 0 |
| 10 | 4.5 | ||||
| 20 | 1 | ||||
| 30 | 1 | ||||
| 反应II:绝热恒容 | 0 | 0 | 0 | 2 | 2 |
 的浓度c(I)
的浓度c(I)②对反应I,前10min内的平均反应速率
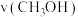 =
= 的物质的量为3.2mol,则T1
的物质的量为3.2mol,则T1 和
和 ,则平衡
,则平衡
您最近一年使用:0次
解题方法
7 . I.含氯物质在生产生活中有重要应用。
(1)实验室沿用舍勒的方法制取 的化学方程式为
的化学方程式为___________ 。
(2)实验室制取干燥 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为___________ 。

其中NaOH溶液的作用是___________ ,其原理是___________ (用离子方程式表示)。
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中___________ 已分解。检验此久置氯水中 存在的操作及现象是
存在的操作及现象是___________ 。
II.某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。

试回答下列问题:
(4)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成NO气体。该同学的推断不合理 的理由是___________ (用化学方程式表示)。
(5)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,加入过量稀硝酸;②待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观察到大试管中气体始终为无色,收集反应产生的气体。其中步骤①的作用是___________ 。
(6)当过量的铜与稀硝酸完全反应后,再加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是___________ (填选项编号),反应的离子方程式为___________ 。
a.还原剂 b.氧化剂 c.提供氢离子 d.提供热能
(1)实验室沿用舍勒的方法制取
 的化学方程式为
的化学方程式为(2)实验室制取干燥
 时,净化与收集
时,净化与收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为
其中NaOH溶液的作用是
(3)某氯水久置后不能使品红溶液褪色,可推测氯水中
 存在的操作及现象是
存在的操作及现象是II.某研究性学习小组的同学为了制取NO并探究其性质,进行了如下实验。

试回答下列问题:
(4)某同学用图甲装置进行实验,收集到无色气体,由此确定铜和稀硝酸反应生成NO气体。该同学的推断
(5)另一名同学设计了图乙装置进行实验,步骤如下:①在大试管中放入适量石灰石,加入过量稀硝酸;②待石灰石反应完全,将铜丝浸入过量的稀硝酸中;③一段时间后,观察到大试管中气体始终为无色,收集反应产生的气体。其中步骤①的作用是
(6)当过量的铜与稀硝酸完全反应后,再加入20%的稀硫酸,铜片上又有气泡产生,稀硫酸的作用是
a.还原剂 b.氧化剂 c.提供氢离子 d.提供热能
您最近一年使用:0次
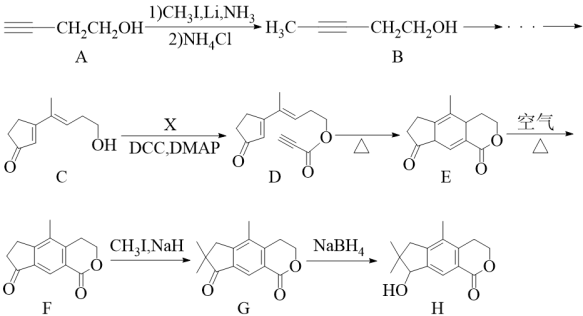
8 . 天然产物H具有抗肿瘤、镇痉等生物活性,可通过以下路线合成。 (
(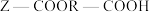 等)
等)
(1)在核磁共振氢谱中,化合物B有___________ 组吸收峰。
(2)化合物X的结构简式为___________ 。
(3)D→E的反应类型为___________ 。
(4)F的分子式为___________ ,G所含官能团的名称为___________ 。
(5)下列物质不能与H发生反应的是___________ (填序号)。
a. b.
b. 溶液 c.酸性
溶液 c.酸性 溶液 d.金属
溶液 d.金属
(6)A的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:___________ 。
(7)以 和
和 ,为原料,合成
,为原料,合成 ,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)
,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选) ___________ 。
 (
(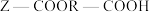 等)
等)(1)在核磁共振氢谱中,化合物B有
(2)化合物X的结构简式为
(3)D→E的反应类型为
(4)F的分子式为
(5)下列物质不能与H发生反应的是
a.
 b.
b. 溶液 c.酸性
溶液 c.酸性 溶液 d.金属
溶液 d.金属
(6)A的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:
(7)以
 和
和 ,为原料,合成
,为原料,合成 ,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)
,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)
您最近一年使用:0次
名校
9 . 常温下,向新制氯水中滴加 溶液,溶液中水电离出的
溶液,溶液中水电离出的 浓度与
浓度与 溶液体积之间的关系如图所示。下列推断
溶液体积之间的关系如图所示。下列推断正确 的是。
 溶液,溶液中水电离出的
溶液,溶液中水电离出的 浓度与
浓度与 溶液体积之间的关系如图所示。下列推断
溶液体积之间的关系如图所示。下列推断
A.E、H点溶液的 分别为3和7 分别为3和7 |
B.F点对应的溶液中: |
C.G点对应的溶液中: |
D.E~H点对应的溶液中, 为定值 为定值 |
您最近一年使用:0次
2023-04-06更新
|
807次组卷
|
8卷引用:天津市红桥区2023届高三第二次模拟考试化学试题
10 . 色满结构单元(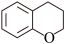 )广泛存在于许多具有生物活性分子的结构中。一种含色满结构单元的药物中间体G的合成路线如图:
)广泛存在于许多具有生物活性分子的结构中。一种含色满结构单元的药物中间体G的合成路线如图:

(1)色满结构单元(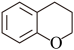 )的分子式是
)的分子式是_____ 。
(2)乙酸酐的结构简式是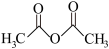 ,A→B反应类型是
,A→B反应类型是_____ 。
(3)检验A中的含氧官能团的化学试剂是_____ ;写出G中含氧官能团的名称为_____ 。
(4)E→F的化学方程式是_____ 。
(5)乙二酸二乙酯由乙二酸和乙醇反应制得,乙二酸二乙酯的结构简式是_____ 。M是乙二酸二乙酯的同分异构体,写出两种满足下列条件的M的结构简式_____ 、_____ 。
①1molM能与足量NaHCO3反应放出2molCO2
②核磁共振氢谱有三组峰
(6)设计以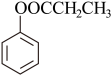 为原料制备
为原料制备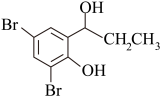 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)_____ 。
 )广泛存在于许多具有生物活性分子的结构中。一种含色满结构单元的药物中间体G的合成路线如图:
)广泛存在于许多具有生物活性分子的结构中。一种含色满结构单元的药物中间体G的合成路线如图:
(1)色满结构单元(
 )的分子式是
)的分子式是(2)乙酸酐的结构简式是
 ,A→B反应类型是
,A→B反应类型是(3)检验A中的含氧官能团的化学试剂是
(4)E→F的化学方程式是
(5)乙二酸二乙酯由乙二酸和乙醇反应制得,乙二酸二乙酯的结构简式是
①1molM能与足量NaHCO3反应放出2molCO2
②核磁共振氢谱有三组峰
(6)设计以
 为原料制备
为原料制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
2023-03-29更新
|
663次组卷
|
3卷引用:天津市红桥区2023届高三下学期一模考试化学试题
天津市红桥区2023届高三下学期一模考试化学试题(已下线)回归教材重难点13 熟悉有机化学“模型”-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)湖南省衡阳县第四中学2022-2023学年高三下学期4月月考化学试题




