1 . 次氯酸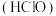 是极强氧化剂,在医疗、餐饮、家居清洁等方面有着重要应用,当前中国次氯酸产业规模庞大,位居全球前列。
是极强氧化剂,在医疗、餐饮、家居清洁等方面有着重要应用,当前中国次氯酸产业规模庞大,位居全球前列。
I.某学习小组设计下列装置制备 并验证其氧化性(夹持仪器及降温装置已省略)。
并验证其氧化性(夹持仪器及降温装置已省略)。
已知:①次氯酸的浓溶液呈黄色
② 为棕黄色气体,极易溶于水并迅速反应生成
为棕黄色气体,极易溶于水并迅速反应生成

回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ , 的结构式为
的结构式为___________ , 俗称
俗称___________ (写出一个即可)。
(2)制备 时要打开
时要打开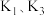 ,关闭
,关闭 ,待装置
,待装置 中反应结束时再通入一段时间
中反应结束时再通入一段时间 。
。
①仪器 中制备
中制备 时,发生反应为
时,发生反应为 ,该反应的氧化剂为
,该反应的氧化剂为___________ (填化学式)。
②仪器B、D中的试剂分别为___________ (填字母)。
a.浓 b.饱和食盐水、
b.饱和食盐水、 c.饱和食盐水、浓
c.饱和食盐水、浓
③搅拌器的作用主要是___________ 。
(3)验证 的氧化性时要向
的氧化性时要向 中加入过量
中加入过量 并充分搅拌,待溶液变澄清时停止搅拌。反应结束时,
并充分搅拌,待溶液变澄清时停止搅拌。反应结束时, 的溶液中含有的离子主要有
的溶液中含有的离子主要有 ,写出反应的离子方程式
,写出反应的离子方程式___________ 。
II. 是次氯酸工业重要的衍生产品,某实验小组的同学测定
是次氯酸工业重要的衍生产品,某实验小组的同学测定 晶体的纯度过程如下:取样品
晶体的纯度过程如下:取样品 配制成
配制成 溶液,从中取出
溶液,从中取出 ,加入足量
,加入足量 固体和适量稀
固体和适量稀 ,再滴加几滴淀粉溶液,(已知:
,再滴加几滴淀粉溶液,(已知: ),然后用
),然后用 标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为
标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为 (已知:
(已知: )。
)。
(4)下列滴定操作会导致测量结果偏低的是___________ (填字母)。
a.锥形瓶洗涤后没有干燥 b.滴定时锥形瓶中有液体浅出
c.滴定终点时俯视读数 d.滴定管滴定前有气泡,滴定后气泡消失
(5)样品中 的纯度为
的纯度为___________ (用含 的代数式表示)。
的代数式表示)。
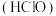 是极强氧化剂,在医疗、餐饮、家居清洁等方面有着重要应用,当前中国次氯酸产业规模庞大,位居全球前列。
是极强氧化剂,在医疗、餐饮、家居清洁等方面有着重要应用,当前中国次氯酸产业规模庞大,位居全球前列。I.某学习小组设计下列装置制备
 并验证其氧化性(夹持仪器及降温装置已省略)。
并验证其氧化性(夹持仪器及降温装置已省略)。已知:①次氯酸的浓溶液呈黄色
②
 为棕黄色气体,极易溶于水并迅速反应生成
为棕黄色气体,极易溶于水并迅速反应生成

回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为 的结构式为
的结构式为 俗称
俗称(2)制备
 时要打开
时要打开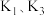 ,关闭
,关闭 ,待装置
,待装置 中反应结束时再通入一段时间
中反应结束时再通入一段时间 。
。①仪器
 中制备
中制备 时,发生反应为
时,发生反应为 ,该反应的氧化剂为
,该反应的氧化剂为②仪器B、D中的试剂分别为
a.浓
 b.饱和食盐水、
b.饱和食盐水、 c.饱和食盐水、浓
c.饱和食盐水、浓
③搅拌器的作用主要是
(3)验证
 的氧化性时要向
的氧化性时要向 中加入过量
中加入过量 并充分搅拌,待溶液变澄清时停止搅拌。反应结束时,
并充分搅拌,待溶液变澄清时停止搅拌。反应结束时, 的溶液中含有的离子主要有
的溶液中含有的离子主要有 ,写出反应的离子方程式
,写出反应的离子方程式II.
 是次氯酸工业重要的衍生产品,某实验小组的同学测定
是次氯酸工业重要的衍生产品,某实验小组的同学测定 晶体的纯度过程如下:取样品
晶体的纯度过程如下:取样品 配制成
配制成 溶液,从中取出
溶液,从中取出 ,加入足量
,加入足量 固体和适量稀
固体和适量稀 ,再滴加几滴淀粉溶液,(已知:
,再滴加几滴淀粉溶液,(已知: ),然后用
),然后用 标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为
标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为 (已知:
(已知: )。
)。(4)下列滴定操作会导致测量结果偏低的是
a.锥形瓶洗涤后没有干燥 b.滴定时锥形瓶中有液体浅出
c.滴定终点时俯视读数 d.滴定管滴定前有气泡,滴定后气泡消失
(5)样品中
 的纯度为
的纯度为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
2 . 某温度下,恒容密闭容器内发生反应:H2(g)+I2 g)  2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
 2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是
2HI(g) △H<0, 该温度下,K=43,某时刻,测得容器内 H2、I2、HI的浓度依次为0.01 mol/L、0.01 mol/L、0.02 mol/L。一段时间后,下列情况与事实相符的是| A.混合气体颜色变深 | B.混合气体密度变大 |
| C.容器内压强变小 | D.氢气的体积分数变小 |
您最近一年使用:0次
2023-10-21更新
|
689次组卷
|
25卷引用:天津市河北区2020届高三年级“停课不停学”期间线上测试化学试题
天津市河北区2020届高三年级“停课不停学”期间线上测试化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期末检测化学试题北京市海淀区2020届高三上学期期末考试化学试题北京市海淀区2021~2022学年高二上学期期末化学试题(已下线)第04练 化学平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)安徽省舒城中学2021-2022学年高二下学期第一次月考化学试题吉林省汪清县汪清四中2021-2022学年高二上学期第一次阶段考试化学试题四川省南充市2021-2022学年高二下学期期末考试化学试题 陕西省咸阳市武功县2021--2022学年高二上学期质量调研化学试题北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题湖北省宜昌英杰学校2022-2023学年高二上学期10月测试化学试题北京市第三十五中学2022-2023学年高二上学期10月月考化学试题甘肃省兰州第一中学2022-2023学年高二上学期期末考试化学试题天津市南开区2023届高三下学期质量监测 ( 二 ) 化学试题陕西省洛南中学2022-2023学年高二上学期10月月考化学试题(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)天津市第一中学2023-2024学年高二上学期10月月考化学试题北京市海淀区2023-2024学年高二上学期期中考试化学试题北京市和平街第一中学2023-2024学年高二上学期10月阶段性练习化学试题北京市第五十中学2023-2024学年高二上学期期中考试化学试题北京市广渠门中学2023-2024学年高二上学期期中考试化学试题 北京市第一六一中学2023-2024学年高二上学期10月月考化学试题安徽省合肥卓越中学2023-2024学年高二上学期期中考试化学试题北京市北京师范大学附属中学平谷第一分校2023-2024学年高二上学期期中考试化学试题天津市南开中学2023-2024学年高三下学期第四次月考化学试卷
3 . 科学家在1925年发现了铼(Re)元素,由于铼可应用在高效能喷射引擎及火箭引擎,所以在军事战略上十分重要。 是制备高纯度Re的重要中间体。
是制备高纯度Re的重要中间体。
I. 的纯度测定
的纯度测定
称取wg 样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用
样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用 的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用
的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用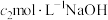 标准溶液滴定过剩的HCl,达到终点时消耗
标准溶液滴定过剩的HCl,达到终点时消耗 溶液。
溶液。

(1)仪器a是___________ (填名称)。
(2)冰盐水的作用是___________ 。
(3)根据下表,滴定操作时宜选用___________ (填一种指示剂名称);滴定终点的现象是___________ 。
部分指示剂变色的pH范围如下表:
(4)样品中 [已知
[已知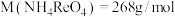 ]的质量分数为
]的质量分数为___________ (填表达式)。
II.高纯度铢的制取
从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉的流程如图:

已知:过铼酸铵( )是白色片状晶体,微溶于冷水,溶于热水。
)是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(5)“碱浸”时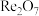 和
和 与NaOH发生以下反应:
与NaOH发生以下反应: ;
; ,则“滤渣I”的成分为
,则“滤渣I”的成分为___________ 。
(6)“沉铼”时,加入热 溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净的
溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净的 晶体,“操作I”包括
晶体,“操作I”包括___________ 、___________ 、洗涤、干燥。
(7)“热解”时,发生反应的化学方程式为___________ 。
 是制备高纯度Re的重要中间体。
是制备高纯度Re的重要中间体。I.
 的纯度测定
的纯度测定称取wg
 样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用
样品,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用 的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用
的盐酸标准溶液吸收,蒸氨结束后取下接收瓶。取吸收液用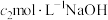 标准溶液滴定过剩的HCl,达到终点时消耗
标准溶液滴定过剩的HCl,达到终点时消耗 溶液。
溶液。
(1)仪器a是
(2)冰盐水的作用是
(3)根据下表,滴定操作时宜选用
部分指示剂变色的pH范围如下表:
| 指示剂名称 | 变色的pH范围 | 酸色 | 中性色 | 碱色 |
| 甲基红 | 4.4—6.2 | 红 | 橙 | 黄 |
| 酚酞 | 8.2—10.0 | 无 | 浅红 | 红 |
 [已知
[已知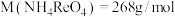 ]的质量分数为
]的质量分数为II.高纯度铢的制取
从辉钼矿氧化焙烧后的烟道灰(主要成分有SiO2、Re2O7、MoO3、CuO、Fe3O4)中提取铼粉的流程如图:

已知:过铼酸铵(
 )是白色片状晶体,微溶于冷水,溶于热水。
)是白色片状晶体,微溶于冷水,溶于热水。回答下列问题:
(5)“碱浸”时
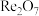 和
和 与NaOH发生以下反应:
与NaOH发生以下反应: ;
; ,则“滤渣I”的成分为
,则“滤渣I”的成分为(6)“沉铼”时,加入热
 溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净的
溶液至产生白色沉淀,为使沉淀充分析出并分离得到纯净的 晶体,“操作I”包括
晶体,“操作I”包括(7)“热解”时,发生反应的化学方程式为
您最近一年使用:0次
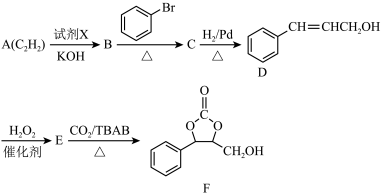
4 . 物质F是用于制造有机离子导体的重要原料,F的一种合成路线可以表示如下:
已知:①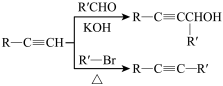
②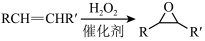
回答下列问题:
(1)试剂X的名称为___________ ,B中官能团的名称为___________ 。
(2)C物质的分子式为___________ ,E→F的反应类型为___________ ,D→E的化学方程式为___________ 。
(3)符合下列条件的D的同分异构体有___________ 种。
①属于芳香族化合物 ②能发生银镜反应 ③含有6种不同化学环境的氢
(4)结合上述合成路线,设计由3-溴-1-丁醇为起始原料制备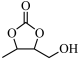 的合成路线
的合成路线___________ 。

已知:①

②

回答下列问题:
(1)试剂X的名称为
(2)C物质的分子式为
(3)符合下列条件的D的同分异构体有
①属于芳香族化合物 ②能发生银镜反应 ③含有6种不同化学环境的氢
(4)结合上述合成路线,设计由3-溴-1-丁醇为起始原料制备
 的合成路线
的合成路线
您最近一年使用:0次
5 . 元素周期表中,铍(Be)与铝处于对角线的位置,它们的性质相似。试回答:
(1)Be元素在元素周期表中的位置:___________ ,有关Be性质的推断不正确的是___________ (填序号)。
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时, 溶液的
溶液的
(2)已知: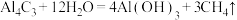 ,写出
,写出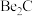 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):___________
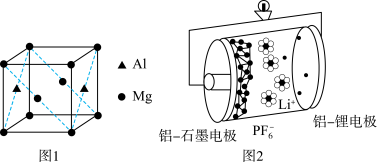
(3)基态铝原子的价电子排布式为___________ ,镁铝合金经过高温淬火获得一种储钠材料,用___________ 法测定其晶胞结构如图1所示,图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为___________ ,该立方晶胞的晶胞的密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为___________ pm。(列出计算式,可不化简)。
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为: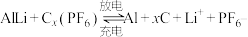 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为___________ ,充电时,应将铝-石墨电极与外接电源的___________ 极相连。
(1)Be元素在元素周期表中的位置:
a.Be是一种轻金属,能与冷水反应
b.氧化铍具有高熔点,能耐酸碱
c.常温时,
 溶液的
溶液的
(2)已知:
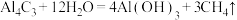 ,写出
,写出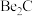 与NaOH溶液反应的离子方程式(铍酸根离子为
与NaOH溶液反应的离子方程式(铍酸根离子为 ):
):(3)基态铝原子的价电子排布式为
 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则该晶胞中镁铝之间的最近距离为
,则该晶胞中镁铝之间的最近距离为
(4)铝石墨双离子电池是一种全新的低成本、高效能电池,反应原理为:
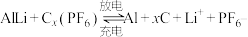 ,电池结构如图2所示。放电时,正极反应式为
,电池结构如图2所示。放电时,正极反应式为
您最近一年使用:0次
名校
6 . 有机物F是重要的医药合成中间体,其一种合成路线如下:

已知:
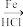

回答下列问题:
(1)物质A的名称为_______ ,核磁共振氢谱有_______ 组峰,最多有_______ 个原子共平面;B的结构简式_______ 。
(2)物质D中官能团的名称为羰基和_______ 。
(3)B→C的反应类型为_______ ,D→E的反应类型为_______ 。
(4)E→F的化学方程式为_______ 。
(5)C有多种同分异构体,同时满足下列条件的同分异构体有_______ 种(不考虑立体异构),
①能发生银镜反应又能发生水解反应;②苯环上一元取代产物有两种:
写出一种核磁共振氢谱有5组峰且峰面积比为3∶2∶2∶2∶1的结构简式_______ 。
(6)参照上述合成路线,以苯和冰醋酸为原料合成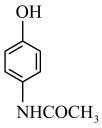 的路线为(无机试剂任选)。
的路线为(无机试剂任选)。_______ 。

已知:

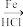

回答下列问题:
(1)物质A的名称为
(2)物质D中官能团的名称为羰基和
(3)B→C的反应类型为
(4)E→F的化学方程式为
(5)C有多种同分异构体,同时满足下列条件的同分异构体有
①能发生银镜反应又能发生水解反应;②苯环上一元取代产物有两种:
写出一种核磁共振氢谱有5组峰且峰面积比为3∶2∶2∶2∶1的结构简式
(6)参照上述合成路线,以苯和冰醋酸为原料合成
 的路线为(无机试剂任选)。
的路线为(无机试剂任选)。
您最近一年使用:0次
解题方法
7 . 铁系纳米复合材料可以去除水体中的硝酸盐污染物。
(1)Fe-Ag金属复合材料去除某 的废水中
的废水中 的反应历程如图所示(吸附在金属复合材料表面的物种用*标注)
的反应历程如图所示(吸附在金属复合材料表面的物种用*标注)

①如图中 的去除机理可描述为
的去除机理可描述为_______ 。
②其他条件一定,反应相同时间,溶液的pH越大, 的去除率越低的原因是
的去除率越低的原因是_______ 。
(2)控制其他条件一定,反应相同时间,不同Ag负载比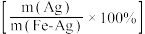 的Fe-Ag金属复合材料对
的Fe-Ag金属复合材料对 的去除率影响如图所示。Ag负载比小于3%时,
的去除率影响如图所示。Ag负载比小于3%时, 的去除率较低的原因是
的去除率较低的原因是_______ 。

(3)其他条件一定,反应相同时间,分别用含铁质量相等的纳米铁粉、Cu负载比为4%的Fe-Cu金属复合材料、Ag负载比为3%的Fe-Ag金属复合材料去除溶液中 ,反应后残留的
,反应后残留的 、生成的
、生成的 和
和 的物质的量如图所示。
的物质的量如图所示。

①与其他材料相比,Fe-Ag金属复合材料去除 的优点是
的优点是_______ 。
②用纳米铁粉去除 时,反应过程中的物种及能量变化如图所示,用纳米铁粉去除
时,反应过程中的物种及能量变化如图所示,用纳米铁粉去除 时生成
时生成 的量极少的原因是
的量极少的原因是_______ 。

(1)Fe-Ag金属复合材料去除某
 的废水中
的废水中 的反应历程如图所示(吸附在金属复合材料表面的物种用*标注)
的反应历程如图所示(吸附在金属复合材料表面的物种用*标注)
①如图中
 的去除机理可描述为
的去除机理可描述为②其他条件一定,反应相同时间,溶液的pH越大,
 的去除率越低的原因是
的去除率越低的原因是(2)控制其他条件一定,反应相同时间,不同Ag负载比
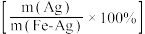 的Fe-Ag金属复合材料对
的Fe-Ag金属复合材料对 的去除率影响如图所示。Ag负载比小于3%时,
的去除率影响如图所示。Ag负载比小于3%时, 的去除率较低的原因是
的去除率较低的原因是
(3)其他条件一定,反应相同时间,分别用含铁质量相等的纳米铁粉、Cu负载比为4%的Fe-Cu金属复合材料、Ag负载比为3%的Fe-Ag金属复合材料去除溶液中
 ,反应后残留的
,反应后残留的 、生成的
、生成的 和
和 的物质的量如图所示。
的物质的量如图所示。
①与其他材料相比,Fe-Ag金属复合材料去除
 的优点是
的优点是②用纳米铁粉去除
 时,反应过程中的物种及能量变化如图所示,用纳米铁粉去除
时,反应过程中的物种及能量变化如图所示,用纳米铁粉去除 时生成
时生成 的量极少的原因是
的量极少的原因是
您最近一年使用:0次
解题方法
8 . 磷酸铁( )主要用于制造磷酸铁锂电池材料。以硫铁矿烧渣(主要成分是
)主要用于制造磷酸铁锂电池材料。以硫铁矿烧渣(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的工艺流程如下:
)为原料制备磷酸铁的工艺流程如下:

(1)焙烧。将硫铁矿烧渣与蔗糖(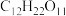 )一起焙烧,可生成FeO与
)一起焙烧,可生成FeO与 。写出焙烧时
。写出焙烧时 所发生反应的化学方程式:
所发生反应的化学方程式:_______ 。
(2)还原。将焙烧后的固体用稀硫酸浸取,所得溶液主要含 ,还含少量
,还含少量 和
和 。向酸浸后所得溶液中加入
。向酸浸后所得溶液中加入 固体,充分搅拌至溶液中
固体,充分搅拌至溶液中 全部被还原并生成
全部被还原并生成 。理论上完全反应需要消耗的
。理论上完全反应需要消耗的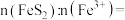
_______ 。
(3)制备 。向
。向 溶液中加入足量的30%
溶液中加入足量的30% 溶液与
溶液与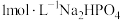 溶液,控制溶液的pH约为1.5,充分反应可得
溶液,控制溶液的pH约为1.5,充分反应可得 沉淀。
沉淀。
①写出生成 反应的化学方程式:
反应的化学方程式:_______ 。
②反应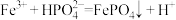 的平衡常数
的平衡常数
_______ 。[已知: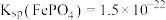 ,
,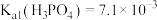 ,
,
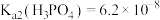 ,
,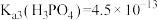 ]
]
(4)其他条件一定,制备 时测得Fe的有效转化率
时测得Fe的有效转化率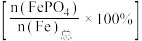 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。

①pH<1.5时,pH越大,Fe的有效转化率越大的原因是_______ 。
②pH>1.5时,pH越大,Fe的有效转化率越低的原因是_______ 。
 )主要用于制造磷酸铁锂电池材料。以硫铁矿烧渣(主要成分是
)主要用于制造磷酸铁锂电池材料。以硫铁矿烧渣(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的工艺流程如下:
)为原料制备磷酸铁的工艺流程如下:
(1)焙烧。将硫铁矿烧渣与蔗糖(
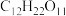 )一起焙烧,可生成FeO与
)一起焙烧,可生成FeO与 。写出焙烧时
。写出焙烧时 所发生反应的化学方程式:
所发生反应的化学方程式:(2)还原。将焙烧后的固体用稀硫酸浸取,所得溶液主要含
 ,还含少量
,还含少量 和
和 。向酸浸后所得溶液中加入
。向酸浸后所得溶液中加入 固体,充分搅拌至溶液中
固体,充分搅拌至溶液中 全部被还原并生成
全部被还原并生成 。理论上完全反应需要消耗的
。理论上完全反应需要消耗的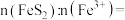
(3)制备
 。向
。向 溶液中加入足量的30%
溶液中加入足量的30% 溶液与
溶液与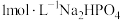 溶液,控制溶液的pH约为1.5,充分反应可得
溶液,控制溶液的pH约为1.5,充分反应可得 沉淀。
沉淀。①写出生成
 反应的化学方程式:
反应的化学方程式:②反应
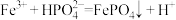 的平衡常数
的平衡常数
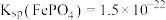 ,
,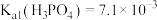 ,
,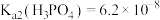 ,
,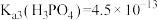 ]
](4)其他条件一定,制备
 时测得Fe的有效转化率
时测得Fe的有效转化率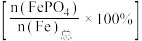 与溶液pH的关系如图所示。
与溶液pH的关系如图所示。
①pH<1.5时,pH越大,Fe的有效转化率越大的原因是
②pH>1.5时,pH越大,Fe的有效转化率越低的原因是
您最近一年使用:0次
名校
解题方法
9 . 利用甲醇 制备一些高附加值产品,是目前研究的热点。
制备一些高附加值产品,是目前研究的热点。
(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.

反应Ⅱ.

反应Ⅲ.

①
_________  。
。
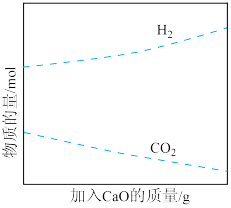
②工业上采用 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入
吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入 提高氢气产率的原因:
提高氢气产率的原因:_________ 。
(2) 和
和 充入一定体积的密闭容器中,在两种温度下发生反应:
充入一定体积的密闭容器中,在两种温度下发生反应: ,测得
,测得 的物质的量随时间的变化如图。
的物质的量随时间的变化如图。

①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为
_________  。(填“>”或“=”或“<”)
。(填“>”或“=”或“<”)
②一定温度下,在容积为 的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
若甲中平衡后气体的压强为开始的0.8倍,则乙容器起始时反应速率
_________  。(填“>”“<”或“=”)。
。(填“>”“<”或“=”)。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是_________ 。
a.容器中压强不变
b. 的体积分数不变
的体积分数不变
c.
d.容器中密度不变
e.2个 断裂的同时有3个
断裂的同时有3个 断裂
断裂
(3)已知电离常数 :
: ,
, :
: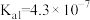 ,
, ,则向
,则向 溶液中通入少量
溶液中通入少量 时的离子方程式为
时的离子方程式为_________ 。
(4)利用人工光合作用,借助太阳能使 和
和 转化为
转化为 ,如图所示,在催化剂b表面发生的电极反应为:
,如图所示,在催化剂b表面发生的电极反应为:_________ 。

 制备一些高附加值产品,是目前研究的热点。
制备一些高附加值产品,是目前研究的热点。(1)甲醇和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ.


反应Ⅱ.


反应Ⅲ.


①

 。
。②工业上采用
 吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入
吸附增强制氢的方法,可以有效提高反应Ⅰ氢气的产率,如图所示,请分析加入 提高氢气产率的原因:
提高氢气产率的原因:
(2)
 和
和 充入一定体积的密闭容器中,在两种温度下发生反应:
充入一定体积的密闭容器中,在两种温度下发生反应: ,测得
,测得 的物质的量随时间的变化如图。
的物质的量随时间的变化如图。
①曲线Ⅰ、Ⅱ对应的平衡常数大小关系为

 。(填“>”或“=”或“<”)
。(填“>”或“=”或“<”)②一定温度下,在容积为
 的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。| 容器 | 甲 | 乙 |
| 反应物投入量 |  、 、 |  、 、 、 、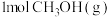 、 、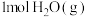 |

 。(填“>”“<”或“=”)。
。(填“>”“<”或“=”)。③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是
a.容器中压强不变
b.
 的体积分数不变
的体积分数不变c.

d.容器中密度不变
e.2个
 断裂的同时有3个
断裂的同时有3个 断裂
断裂(3)已知电离常数
 :
: ,
, :
: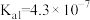 ,
, ,则向
,则向 溶液中通入少量
溶液中通入少量 时的离子方程式为
时的离子方程式为(4)利用人工光合作用,借助太阳能使
 和
和 转化为
转化为 ,如图所示,在催化剂b表面发生的电极反应为:
,如图所示,在催化剂b表面发生的电极反应为:
您最近一年使用:0次
名校
解题方法
10 . 有机物H是合成某种药物的中间体,一种合成路线如图。
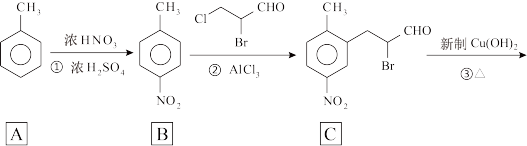

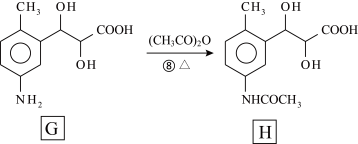
回答下列问题:
(1)有机物B的化学名称为_________ 。
(2)写出C中的含氧官能团的名称_________ 。
(3)判断反应类型为②_________ ,⑦_________ 。
(4)反应④所需试剂、条件分别为_________ 。
(5)写出H的分子式_________ 。
(6)写出反应③的化学方程式_________ 。
(7)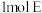 与
与 完全加成生成
完全加成生成 ,W有多种同分异构体,其中属于
,W有多种同分异构体,其中属于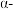 氨基酸、分子中含两个羧基、且苯环上有两个取代基的W的可能结构共有
氨基酸、分子中含两个羧基、且苯环上有两个取代基的W的可能结构共有_________ 种(不考虑立体异构),其中核磁共振氢谱为五组峰,峰面积比为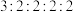 的结构简式为
的结构简式为_________ 。



回答下列问题:
(1)有机物B的化学名称为
(2)写出C中的含氧官能团的名称
(3)判断反应类型为②
(4)反应④所需试剂、条件分别为
(5)写出H的分子式
(6)写出反应③的化学方程式
(7)
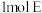 与
与 完全加成生成
完全加成生成 ,W有多种同分异构体,其中属于
,W有多种同分异构体,其中属于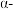 氨基酸、分子中含两个羧基、且苯环上有两个取代基的W的可能结构共有
氨基酸、分子中含两个羧基、且苯环上有两个取代基的W的可能结构共有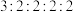 的结构简式为
的结构简式为
您最近一年使用:0次



